
Los inhaladores de polvo seco (IPS) son dispositivos que permiten la aerolización y entrega de medicamentos para el tratamiento de las enfermedades respiratorias, sin necesidad del empleo de propelentes. Se caracterizan por ser de fácil manejo, portátiles y duraderos. Según el mecanismo de fluidización que emplean se pueden dividir en 2 clases, activos y pasivos. Se describen las características del diseño de algunos de los dispositivos pasivos más empleados comercialmente para la administración de formulaciones de polvo para inhalación. Se mencionan además, las técnicas empleadas para la realización de los estudios in vitro y los resultados de algunos estudios realizados con estos dispositivos.
Palabras clave: Inhalador de polvo seco (IPS), diseño, estudios in vitro.
En el mundo el tratamiento por inhalación se administra, fundamentalmente, mediante los inhaladores de dosis metrada presurizados (IDMp), en Europa ellos constituyen aproximadamente el 80 % de los inhaladores prescritos, el 20 % restante corresponde a los inhaladores de polvo seco (IPS) y en una proporción mucho menor los nebulizadores. Sin embargo, en algunos países, principalmente, en Escandinavia y los países Bajos, donde el gobierno ha fomentado el desarrollo de la tecnología de polvo para inhalación, su empleo se encuentra muy extendido con un uso de hasta el 85 % de los pacientes asmáticos ( Diario Oficial de las Comunidades Europeas (98/C355/02). 1998. p. 6).
Los IPS son dispositivos que permiten la aerolización y entrega de fármacos para el tratamiento de las enfermedades respiratorias, sin necesidad del empleo de propelentes. Se caracterizan por ser de fácil manejo, portátiles y duraderos. Los dispositivos de inhalación de polvo seco, según el mecanismo de fluidización que emplean, se pueden dividir en 2 clases, activos y pasivos.1,2
Los dispositivos activos han estado en etapa de investigación durante los últimos 10 años, pero hasta la fecha no se ha aprobado ningún dispositivo activo por la Food and Drug Administration (FDA); similares a los IDMp, utilizan una fuente externa de energía, que puede ser aire comprimido ó una batería que almacena energía y luego es liberada para facilitar la dispersión de los polvos. Los dispositivos activos tienen la ventaja de reducir la dependencia de la uniformidad de la dosis a la capacidad de inspiración del paciente. Sin embargo, sin un mecanismo de retroalimentación para la fuente de energía, es todavía posible que diferentes pacientes reciban diferentes dosis, además de ser complejos y costosos.3,4
Los dispositivos pasivos dependen exclusivamente del flujo de inspiración del paciente, en ellos el fármaco es suministrado en coordinación con la inhalación del paciente. La fracción de partículas finas que llegan a los pulmones se ve enormemente influenciada por la capacidad de inhalación del paciente, y la posibilidad de lograr un flujo de aire óptimo que permita la fluidización del fármaco.4,5
Existe gran variedad de diseños en los dispositivos pasivos, los primeros que surgieron en la década de los 70, fueron los IPS de dosis única. El primero en comercializarse fue el Spinhaler ® (Fisons), seguido del Rotahaler® (GlaxoSmithKline). Para todos los dispositivos de dosis única, e l reservorio empleado para contener la formulación es una cápsula de gelatina dura.6,7
El Turbo-inhaler® Meheco (fig. 1), tiene un diseño análogo al (Spinhaler®) Fisons, está constituido por 3 partes fundamentales: una boquilla con aguja de acero inoxidable, hélice y el cuerpo con un tubo deslizante. El dispositivo se desarma y se coloca la boquilla hacia abajo, la boquilla tiene una aguja de acero inoxidable en la que se coloca la hélice. La cápsula es colocada en un molde que la sostiene dentro de la hélice. Con la boquilla hacia abajo se coloca el cuerpo y se enrosca. El cuerpo del dispositivo contiene 2 agujas que actúan perforando la cápsula cuando el paciente desliza el tubo en sentido descendente por el cuerpo y luego lo lleva a su posición original. El diseño del dispositivo, con orificios que permiten la entrada del aire, unido al movimiento de rotación y vibración generado por la hélice durante la inspiración del paciente permite la dispersión y aerolización de los polvos.8
]]>
Fig. 1. Turbo-inhaler® cortesía de Meheco (China).
Aunque existen una gran variedad de dispositivos de dosis única patentados, el fundamento para su aplicación medicamentosa es, generalmente, muy análogo. El Aerolizar® Novartis, está constituido por una tapa y el cuerpo del dispositivo, al girar la boquilla hacia la derecha queda libre el reservorio moldeado en forma de cápsula, 4 pequeñas agujas que se activan cuando el paciente presiona 2 muelles que se encuentran ubicados a ambos lados del dispositivo perforan la cápsula, la dispersión de los polvos en este caso se ve favorecida por una malla colocada entre la boquilla y el reservorio que permiten su desagregación. El Nebulasma® es otro dispositivo patentado que utiliza un émbolo percutor para perforar la cápsula.9
El Rotahaler® GlaxoSmithKline (fig. 2), es un dispositivo de dosis única que se diferencia de los anteriores en que no presenta ningún estilete ó aguja para perforar la cápsula, está constituido por dos piezas: una superior que contiene un orificio para la introducción de la cápsula y una inferior en forma de boquilla con una malla y un deflector. Cuando el paciente rota el dispositivo, la tapa de la cápsula, colocada en el orificio, se separa del cuerpo producto de la presión que ejerce el deflector, el polvo liberado pasa a través de la malla para ser inspirado por el paciente.10,11
Fig. 2. Rotahaler® cortesía de Glaxo Wellcome (UK).
El Diskhaler® de GlaxoSmithKline es un dispositivo de plástico moldeado con una tapa protectora. Se caracteriza por contener discos recargables, el paquete dosificador o Rotadisk contiene de 4 a 8 dosis, según el principio activo a administrar. Las dosis se almacenan en blister de aluminio foliado que protege de la humedad la formulación, el Rotadisk es cargado dentro de un portadisco el cual se desliza en la parte exterior del cuerpo.12,13
El Diskus® o Accuhaler® de GlaxoSmithKline (fig. 3), al igual que su antecesor retiene el principio activo en blister de aluminio pero tiene la ventaja de contener un número mayor de dosis, para al menos un mes, sin sustitución del paquete dosificador. El paquete dosificador está basado en una tecnología de doble capa en forma de cinta enrollada con 60 blister. Los blister están conformados en frío en una lámina de aluminio y posteriormente son llenados con la formulación y sellados con una tapa de aluminio.
Fig. 3. Diskus®/Accuhaler® cortesía de Glaxo Wellcome (UK).
]]> Dentro del cuerpo del dispositivo hay 3 ruedas las cuales son accionadas desde la parte exterior por una leva. Una rueda dentada guía la cinta y asegura que cada vez que se realice una operación con la leva, el blister sea abierto en el pasaje de aire de forma consistente y reproducible. Cuando el blister está correctamente alineado, la tapa de aluminio es levantada y separada de la base, la cinta vacía es enrollada por una rueda constrictora que la colapsa de forma progresiva, manteniendo el alineamiento dentro del dispositivo. El segmento de cinta gastado es enrollado dentro de un compartimiento separado o cámara receptora que almacena la cinta vacía; este compartimiento está diseñado para retener cualquier polvo residual resultante de una inhalación incompleta.Este dispositivo ha sido diseñado para tener baja resistencia al flujo de aire, durante la inspiración el aire es canalizado hasta llegar al blister abierto, aerolizando su contenido y permitiendo que la droga llegue a la boquilla; un aire adicional entra al dispositivo bucal por 2 agujeros facilitando la formación de turbulencia. El dispositivo en forma de disco totalmente de plástico moldeado debe ser utilizado en un plano horizontal. La cubierta exterior se abre y se cierra al presionar con el dedo pulgar, su principal función es la protección de la boquilla y la leva.
Una vez que se abre la cubierta protectora se debe deslizar hacia atrás la leva tan lejos como pueda llegar, un sonido de click señala que el blister ha caído en el lugar adecuado, simultáneamente una rueda indicadora se mueve y permite leer entonces en el cuerpo del dispositivo el número de dosis disponibles. Después de esta operación el dispositivo está listo para que el paciente realice una inhalación rápida y profunda a través de la boquilla. El cierre de la cubierta exterior, automáticamente, lleva la leva a su posición original.12,14
El Turbohaler® de Astra Zeneca (fig. 4), está constituido por 13 componentes plásticos y un muelle de acero, contiene además un indicador que le señala al paciente cuando le quedan 20 dosis o menos. El reservorio plástico puede contener 60, 100 y hasta 200 dosis del principio activo sólo o mezclado con un transportador. El nuevo Symbicort® M3 Turbuhaler incorpora además un contador de dosis.
Fig.4. Turbohaler® o Turbuhaler® cortesía de Astra Zeneca (Suecia).
El Turbuhaler debe ser colocado en una posición superior a los 45° de la horizontal y una vez cargado puede ser utilizado en cualquier ángulo. Una dosis es cargada cuando la rueda en la base es, totalmente, girada en una dirección y llevada a su posición original. Esta acción llena un depósito en forma cónica en el disco de metraje, unos raspadores eliminan cualquier cantidad excesiva del fármaco. El número y el tamaño de los depósitos del disco de metraje son cambiados de acuerdo con las especificaciones del fármaco y la dosis requerida. En estos sistemas la garantía de la dosis está determinada en el metraje por un proceso volumétrico de forma tal que son medidas cantidades de polvo inferiores a 0,5 mg.12,14
La inhalación a través de la pieza bucal expulsa las partículas hacia el canal de inhalación, 2 canales en forma de espiral ubicados entre el canal de inhalación y la pieza bucal permiten la desagregación de las partículas. Estos canales en forma de espiral están diseñados aerodinámicamente para crear un flujo de turbulencia que ayuda a la dispersión del fármaco. Una cantidad adicional de aire penetra por aberturas que se encuentran justo debajo de la pieza bucal, reduciendo la caída de presión e incrementando la velocidad lineal del aire. El dispositivo se compone, además, de una cubierta que protege al producto de la humedad.12,15
El Clickhaler®, de Innovata Biomed/Celltech, es un inhalador tipo reservorio multidosis, que libera un máximo de 200 dosis. El dispositivo contiene 16 componentes (14 componentes plásticos y 2 muelles de compresión). El sistema de metraje consiste en un cono metrado, un reservorio para el almacenamiento del fármaco y un muelle que comprime el cono y garantiza una rotación pareja de este. El cono se encuentra situado debajo del reservorio y posee en su superficie una serie de aberturas metradas las cuales se llenan por gravedad. Cuando el cono se rota, el polvo se traslada hacia el pasaje de inhalación. El pasaje de inhalación consiste en una estructura de fijación principal y una boquilla diseñada para minimizar la resistencia al flujo de aire. Este dispositivo contiene un reservorio de desecho, el cual permite que solo una dosis metrada esté presente al activar el mecanismo de operación, su función es remover el polvo desechado y evitar que se administre una doble o múltiple dosis. El mecanismo de operación incluye un botón deslizante que se empuja hacia abajo, un segundo muelle de compresión y un mecanismo de leva dentada. Este mecanismo convierte el movimiento lineal hacia abajo del botón en un movimiento circular de rotación del cono de metraje que traslada el polvo hacia el pasaje de inhalación. Un contador unido al mecanismo de operación indica el número de dosis, la ventana del contador es rallada en rojo cuando solo quedan 10 dosis remanentes. Después que la última dosis ha sido utilizada, el botón deslizante se tranca para prevenir su uso. El dispositivo se comercializa sellado en una bolsa de aluminio para protegerlo de la humedad ambiental, después de retirada esta protección el tiempo de vida útil se estima en aproximadamente 6 meses.16-20
El Easyhaler® de Orion Pharma (fig. 5), al igual que el Clickhaler® está diseñado para imitar en su forma y operación a los IDMp. El dispositivo está constituido de 7 partes plásticas y un muelle de acero níquel. El reservorio permite contener hasta 200 dosis. El dispositivo para ser cargado debe ser colocado en posición vertical hacia arriba, cuando se presiona la pieza superior o sobrecubierta, rota el cilindro de metraje y libera la dosis. Un contador de dosis conectado al cilindro de metraje permite al paciente visualizar el número de dosis que aún le queda al inhalador. La próxima dosis llena la cavidad por gravedad, ya que el cono de metraje se encuentra ubicado, justamente, debajo del reservorio. En este dispositivo no existe un depósito o cámara de desechos para los polvos residuales, eventualmente la dosis no utilizada es devuelta al reservorio. Al igual que el dispositivo anterior el diseño garantiza la desagregación y entrega de la dosis durante la inspiración del paciente. Contiene, además, una cubierta protectora que tiene el objeto de disminuir la penetración de la humedad.12,19,20
]]>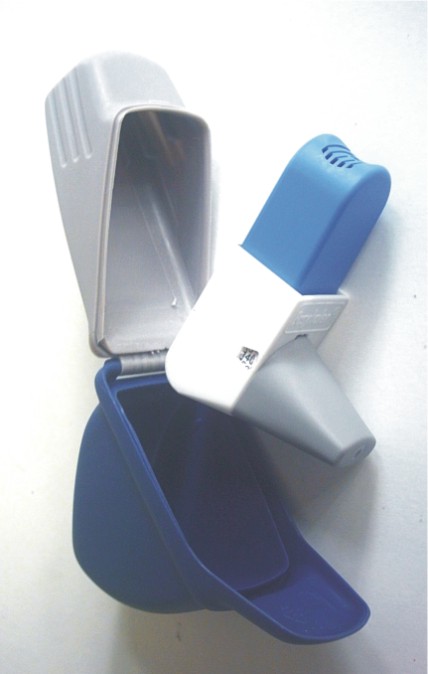
Fig. 5. Easyhaler® cortesía de Orion Pharma (Finlandia).
Las pruebas in vitro para los IPS se han desarrollado durante años y sus métodos están publicados en la Farmacopea de los Estados Unidos (USP) y la Farmacopea Europea (UK).21,22
Para que cualquier medicamento sea seguro y eficaz, el principio activo debe alcanzar el sitio de acción en una concentración apropiada con niveles aceptables de impurezas. Para las formas farmacéuticas inhaladas, se utilizan pruebas típicas como identificación, apariencia, contenido de humedad, análisis del tamaño de partículas, relación de impurezas y límite microbiano, pero, además, deben realizarse pruebas específicas como la determinación de la dosis emitida (DE) y la fracción de partículas finas (FPF) o respirables.23
El método de la determinación de la deposición de la DE se basa en una técnica de impacto inercial. Esto implica dirigir una corriente de aire laminar cargada con partículas a una superficie de impacto que desvía el aire en 90 º y cuantificar la cantidad de material que pasa o choca en la superficie. Las partículas grandes con inercia suficiente, chocan en la superficie, mientras las partículas menores evitan el impacto y fluyen por el sistema para ser colectadas.22,24
La dosis entregada al pulmón por cualquier dispositivo inhalador es conocida como FPF o respirables. Se ha propuesto un intervalo de definición que incluye aquellas partículas con un diámetro menor de 5,0 µm. La FPF se cuantifican in vitro a través del material que se recupera de las etapas apropiadas de los dispositivos utilizados, comercialmente, para su determinación.16,23
Los aparatos estándar para la determinación de la DE se dividen en impactadores de una sola etapa y los multietapas.
Dentro de los impactadores de una sola etapa se puede mencionar el Twin Impinger (TI) y el Metal Impinger (MI); ellos solo determinan la masa de droga menor que el tamaño de partícula aerodinámico, para el TI la masa de partículas con diámetro de corte efectivo (DCE) menor de 6,4 µm y para el MI es la masa de partículas con DCE menor de 9.8 µm.
Dentro de los multietapas se encuentran: el impactador Marple-Miller (IMM), el impactador de cascada Andersen (ICA) y el multietapas líquido Impinger (MLI). Ellos permiten determinar la masa media de diámetro aerodinámico (MMDA) y la desviación estándar geométrica (DSG). El IMM contiene 5 etapas de impactación con un diámetro de corte efectivo DCE a 60 L/min entre 10 y 0,625 µm y un filtro final que retiene las partículas inferiores a 0,625 µm. El ICA contiene 8 etapas de impactación con un DCE a 28,3 L/min entre 9 y 0,4 µm, un preseparador que colecta partículas grandes y un filtro final. El MLI contiene 4 etapas de impactación y un filtro final, estas etapas tienen un DCE a 60 L/min entre 13 y 1,7 µm.21,23
Todos estos sistemas comercialmente disponibles tienen la desventaja de que deben ser calibrados a un flujo de aire fijo, el cual no siempre es representativo de los flujos típicamente alcanzados por el paciente durante la administración del medicamento.23
La liberación a los pulmones a partir de los inhaladores de polvo seco de dosis única se incrementa al aumentar el rango de flujo de aire, con deposiciones en el pulmón in vivo y valores de FPF in vitro en rangos de 6 a 14 % de la dosis nominal. El Rotahaler® muestra valores de FPF del orden del 11 %, las comparaciones clínicas sugieren que es la mitad de las deposiciones obtenidas utilizando los IDMp.6,27,28
El Diskus® tiene una resistencia al flujo de aire similar al Diskhaler® pero no consiguió igualar la FPF en flujos de aire de 90, 60, y 30 L/min. Para el Diskhaler ® los valores son de 47, 40 y 25 % en comparación con los obtenidos para el Diskus® de 28, 26 y 19 % de la dosis declarada de salbutamol. En un estudio realizado con beclometasona de 400 mg se sugiere que una relación de 2 a 1 era requerida para obtener equivalencia clínica entre el Diskhaler® y los IDMp.12
Se comparó la eficiencia del propionato de fluticasona Diskus® y la budesonida Turbuhaler® en un estudio de simulación con niños asmáticos entre 4 y 8 años. Se reportaron valores de FPF de 15 a 18 % con propionato de fluticasona Diskus® y 21 a 23 % con el Turbohaler® de budesonida. Las proporciones de partículas fueron de 72 a 71 % para el Diskus® y 30 a 35 % con el Turbohaler®. Por lo tanto el Diskus® fue capaz de proveer una emisión más consistente del fármaco pero el Turbohaler® produjo una mayor proporción de partículas finas indicando una mayor eficiencia potencial de entrega del medicamento a los pulmones.29
El Turbohaler® en un estudio de simulación del uso del paciente que se realizó removiendo la cubierta protectora 4 veces durante 2 min a 30 ºC y 72 % de humedad relativa durante 40 días, mostró una progresiva reducción en la dosis emitida y la FPF a un flujo de 28 L/min pero no se observó está reducción en las pruebas realizadas a un flujo de 60 L/min.30
En un ensayo clínico multicentro, aleatorio con 31 pacientes adultos con asma, se obtuvo como resultado una mayor eficiencia con el empleo del Bricanyl Turbohaler® en comparación con su similar IDMp de terbutalina.1
El Clickhaler® tiene una resistencia media al flujo de aire, en un estudio realizado con el salbutamol de 110 µg se determinó la FPF empleando 2 impactadores diferentes, se obtuvo un 43 % de FPF con el impactador de cascada Andersen comparado con el 45 % en el Twin Impinger. Las FPF no mostraron diferencias estadísticamente significativas al ser calibrados a 30 y 60 L/min en el TI. El Clickhaler® ha demostrado in vitro que opera eficientemente en un intervalo de flujo de 15 a 60 L/min con valores de DE y FPF esencialmente consistentes.16,31
En un estudio clínico multicentro, aleatorizado, a doble ciego, participaron 61 niños con asma moderada en un intervalo de edades entre 6 y 17 años, durante 4 semanas. Se comparó la eficacia, tolerabilidad y aceptabilidad del salbutamol Clickhaler® de 100 µg con el IDMp de salbutamol Ventolin® empleando una cámara espaciadora Volumatic®, y se demostró la equivalencia terapéutica en la respuesta broncodilatadora.32
El Easyhaler® ha mostrado una buena uniformidad en la entrega de la dosis in vitro a un intervalo de flujo de 28 L/min. Se determinaron los niveles de FPF con este dispositivo en formulaciones de 200 µg de salbutamol a un flujo de aire de 60, 40 y 28 L/min; las fracciones respirables fueron de 47, 37 y 32 % respectivamente.12
Un estudio clínico, aleatorizado, a doble ciego, se realizó en 5 instituciones Alemanas, con 40 pacientes adultos, con asma de diferentes grados de severidad, en un intervalo de edades entre 18 y 78 años. En este estudio se concluyó que el salbutamol Easyhaler® de 100 µm puede ser considerado clínicamente equivalente a los IDMp. Además, el tiempo de máxima respuesta y la duración de la actividad broncodilatadora también se consideraron equivalentes.20
]]> Por último, podemos concluir que esta nueva generación de IPS se puede considerar equivalente a los IDMp, pues los resultados de los estudios in vitro e in vivo así lo han demostrado.The dry powder inhalers (DPI) are devices that allow the aerosolization and delivery of medications for the treatment of respiratory diseases, without the use of propellants. They are easy handling, portable and durable. According to their fluidization mechanism they can be divided into two kinds: active and passive. The characteristics of the design of some of the most commercially used passive devices for the administration of powder formulations for inhalation are described in this paper. The techniques applied to conduct the in vitro studies, as well as the results of some studies undertaken with these devices are also mentioned.
Key words: Dry powder inhalers (DPI), devices, design, in vitro studies.
1. Ekström T. Dose potency relationship of terbutaline inhaled via Turbuhaler or via a pressurized metered dose inhaler. Ann Allerg Asth Immunol 1995;74(4):328-32.
2. Hickey AJ, Dunbar C.A. A New Millennium for Inhaler Technology. Pharm Technol. 1997;21(6):116-25
3. Crowder T.M . An Odyssey in Inhaler Formulation and Design. Pharm Technol. 2001;7:99-113.
4. Crowder TM. Tecnología de vibración para los iInhaladores de activo en polvo. Pharm Technol en español. 2004;julio/agosto:10-5.
5. Woodhouse RN, Cummings RH, Feinberg TN. The Pharmacutical Development of Inhalation Medicines and the Value of Outsourcing. Pharm Technol. 2002;5:90-5.
6. Hetzel M, Clark T . Comparison of salbutamol Rotahaler with conventional pressurized aerosol. Clin Allergy. 1977;7:563-8.
7. Edmund AT, McKenzie S, Tooley M, Godfrey S. A clinical comparison of beclomethasone dipropionate delivered by pressurized aerosol and as a powder from a rotahaler. Arch Dis Child. 1979;54:233-5.
8. Concessio NM, Hickey AJ. Analysis of the Patterns of Particle Dispersion from a dry powder Inhaler. Pharm Technol. 1996; 6:50 -9.
9. • Faulí C. Aerosoles. En: Tratado de Farmacia Galénica. Madrid: Luzan 5, SA; 1993.
10. Hickey AJ. Factors Influencing the Dispersion of Dry Powders as Aerosols. Pharm Technol. 1994;18(9):58-82.
11. Ganderton D. Dry powder inhaler. Adv Pharm Sci. 1992;6:165-91.
12. Smith IJ, Parry M.. The inhalers of the future? A review of dry powder devices on the market today. Pulm Pharmacol Terap. 2003;16:79-95.
13. Drepaul BA, Payler DK, Qualtrough JE. Becotide or Becodisks? A controlled study in general practice. Clin Trials J. 1989;26:335-44.
14. Brindley A, Sumby BS, Smith IJ, Prime D, Haywood PA, Grant AC. Design, manufacture and dose consistency of the Serevent Diskus inhaler. Pharm Technol Eur. 1995;7(1):14-22.
15. Liljas B, Sthahl E, Pauwels RA. Cost-effectiveness analysis of a dry powder inhaler (Turbuhaler) versus a pressurized metered dose inhaler in patients with asthma. Pharmacoeconomics. 1997;12:267-77
16. Barnes PJ. Clickhaler. An innovation in pulmonary drug delivery. Monograph Innovata Biomed Limited. London: The Respiratory Division of ML Laboratories PLC; 1998. p. 14-7.
17. Newhouse MT . Clickhaler (a novel Dry Powder Inhaler) Provides Similar Bronchodilation to Pressurized Metered Dose Inhaler, Even at Low Flow Rates. CHEST. 1999;115 (4):952-6.
18. Morice AH, Andrews B, Taylor M. Comparison of the effect on bronchial hyperresponsiveness of Beclomethasone Dipropionate Administered via a Novel Multidose Dry Powder Inhaler or a Conventional Pressurized Metered Dose Inhaler. Respiration. 2000;67:298-305.
19. Malinen A, Laurikainen K, Silvasti M, Toivanen P, Nieminen NM . New model of Easyhaler is clinically equally effective as compared with the former model. Eur Respir J. 1997;10(Suppl. 25):127.
20. Vidgren M, Silvasti M, Vidgren P. Easyhaler multiple dose powder inhaler-practical and effective alternative to the pressurized MDI. Aer Sci Technol. 1995;22:335-45.
21. Aerodynamic Assessment of Fine Particles - Fine Particle Dose and Particle Size Distribution. Appendix XII F. British Pharmacopoeia. Version 4.1 en CD Rom ; 2000.
22. XXVI, Aerosols (601). US Pharmacopeia. The US Pharmacopeias Convention, Rockville , MD (vesión en CD Rom). 2003.
23. Van Oort M. In vitro testing of dry powder inhaler. Aer Sci Technol. 1995;22:364-373.
24. Hindle M, Byron PR. Dose emissions from marketed dry powder inhalers. International J Pharm. 1995;116:169-77.
25. Clark A.R, Hollingworth A.M. The relationship between powder inhaler resistance and peak inspiratory conditions in healthy volunteer-Implications for in-vitro testing. J. Aerosol Med. 1993;6:99-110.
26. Byron PR, Kelly EL, Kontny MJ, Lovering EG, Poochikian GK, Sethi S. Recommendations of the USP advisory panel on aerosols on the USP general chapters on aerosols (601) and uniformity of dosage units (905). Pharm Forum. 1994;20:7477-503.
27. Auty RM, Brown K, Neale MG, Snashall PG. Respiratory tract deposition of sodium cromoglycate is highly dependent upon technique of inhalation using the Spinhaler. Br J Dis Chest. 1987;81:371-80.
28. Pitcairn GR, Hunt HMA, Dewberry H, Pavia D, Newman SP. A comparison of in vitro drug delivery from two dry powder inhalers, the Aerohaler® and the Rotahaler®. STP Pharm Sci. 1994;4(1):33-7.
29. Bisgaard H, Klug B, Sumby BS, Burnell PKP. Fine particle mass from the Diskus inhaler and Turbuhaler inhaler in children with asthma. Eur Respir J. 1998;11:1111-5.
30. Meakin BJ, Cainey JM, Woodcock PM. Effect of exposure to humidity on terbutaline sulphate delivery from Turbohaler dry powder inhalation devices. Eur Respir J. 1993;6:760-3.
31. Barrowcliffe J, McGlynn P, Tickle S, Sandbank F, Wong T. The in vitro evaluation of a novel multidose dry powder inhaler. Drug delivery to the lung VII. London : The Aerosol Society; 1996. p. 82-5.
32. O'Callaghan C, Everard ML, Bush A, Hiller EJ, Ross-Russell R, O'Keefe P, et al. Salbutamol dry powder inhaler: efficacy, tolerability, and acceptability study. Pediatr Pulmonol. 2002; 33:189-93.
Recibido: 5 de enero de 2006. Aprobado: 14 de febrero de 2006.
MSc. Adriana Muñoz Cernada. Centro de Investigación y Desarrollo de Medicamentos (CIDEM). Ave. 26 No. 1605 entre Puentes Grandes y Boyeros, municipio Plaza de la Revolución, CP 10 600, Ciudad de La Habana, Cuba. Correo electrónico: cidem@infomed.sld.cu