Loipa Galán Martínez,1 Yamila Verdecia Reyes,2 Estael Ochoa Rodríguez,2 Esperanza Salfrán Solano,2 Blavet Barriet,3 Margarita Suárez Navarro4 y Julio L. Álvarez González5
Se prepararon cinco hexahidroquinoleínas por una síntesis en un solo paso, a partir de un aldehído aromático, el ß -aminocrotonato de alquilo (enamina) y dimedona en etanol absoluto como disolvente. Se caracterizaron los efectos de las cinco hexahidroquinoleínas sobre la contractilidad en anillos de aorta de conejo y sobre la contractilidad de músculos papilares de ventrículo derecho de rata, de manera comparativa con la clásica nifedipina. Todas las hexahidroquinoleínas inhibieron la actividad contráctil tanto en músculo liso vascular como en músculo cardíaco, y mostraron efectos característicos de compuestos antagonistas del calcio, aunque con menor potencia de acción que la nifedipina. Sin embargo, dos de las hexahidroquinoleínas estudiadas presentaron cierta vasoselectividad, aunque no marcada.
Palabras clave: Antagonistas del calcio, hexahidroquinoleínas, dihidropiridinas, vasoselectividad.
Los antagonistas del calcio son compuestos que inhiben la contracción muscular al bloquear el influjo de calcio a través de los canales de calcio, tanto en músculo liso como en músculo cardíaco, y se utilizan ampliamente en el tratamiento de diversas enfermedades cardiovasculares como la hipertensión, la angina y algunos tipos de arritmias.1 Las acciones relativas de estos compuestos difieren sobre los diferentes tejidos cardiovasculares y esto es lo que define la función terapéutica de ellos. La potencia de acción de estos agentes en el tejido liso vascular contra la potencia en miocardio es el valor que predice sus indicaciones terapéuticas.2 Por ejemplo, los antagonistas del calcio clásicos como el verapamil (fenilalquilamina), la nifedipina (1,4-dihidropiridina) y el diltiazem (benzotiazepina), todos tienen propiedades vasodilatadoras, aunque la nifedipina y otras 1,4-dihidropiridinas (1,4-DHP), son cuantitativamente más potentes. Generalmente el verapamil y el diltiazem se clasifican como antagonistas no selectivos, y la nifedipina y otras, 1,4-DHPs se describen como vasoselectivas.1,2
Las 1,4-DHP, por sus características estructurales de fácil manejo y por su efecto vasodilatador dominante, son el grupo de antagonistas del calcio más estudiado y difundido en clínica, donde han demostrado gran efectividad.1,2 A pesar de que las 1,4-DHP son los antagonistas del calcio mejor caracterizados,2 actualmente se sigue trabajando en la búsqueda de nuevas modificaciones estructurales, con el objetivo de encontrar una mayor vasoselectividad, para así evitar los efectos colaterales sobre el miocardio durante la terapia antihipertensiva a largo plazo.1,3 Se debe señalar que, aunque varios estudios sobre antagonistas del calcio reportan algunas acciones favorables también para compuestos como el verapamil y el diltiazem,3 estos no poseen los perfiles de vasoselectividad de las 1,4-DHP, que es lo que las hace tan atractivas para evitar efectos cardíacos indeseables.
A partir de la estructura base de las 1,4-DHP, han surgido nuevos compuestos químicos sintéticos con propiedades antagonistas del calcio como las hexahidroquinoleínas, grupo químico con potencialidades farmacológicas. Existen referencias que demuestran acciones antagonistas del calcio de compuestos derivados de hexahidroquinoleínas,4-11 lo cual da evidencias de que compuestos de este tipo de estructura pueden ser estudiados para la búsqueda de nuevos fármacos antihipertensivos.
Sobre la base del tema de investigación desarrollado en el Laboratorio de Síntesis Orgánica de la Facultad de Química de la Universidad de La Habana, de obtener compuestos sintéticos que tengan el grupo farmacofórico de las 1,4-DHPs y evaluar la modificación del perfil farmacológico inducido por la introducción de otro ciclo fusionado a este, el propósito de este trabajo fue la evaluación de la actividad antagonista del calcio de cinco nuevas hexahidroquinoleínas y caracterizar la posible selectividad vascular, con el objetivo de encontrar agentes antagonistas del calcio vasoselectivos. Concretamente verificamos sus acciones sobre la contracción de los músculos liso vascular y cardíaco, precisando para cada uno las propiedades antagonistas del calcio y el índice de vasoselectividad.
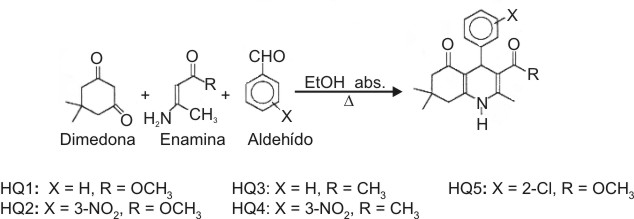
En un balón de 150 mL se mezclaron cantidades equimolares (10 mmol) de dimedona (5,5-dimetil-1,3-ciclohexanodiona), del correspondiente derivado enamínico y del aldehído aromático correspondiente en 50 mL de etanol absoluto. Se reflujó durante 6 h, se enfrió y la mezcla de reacción se virtió sobre agua-hielo. El sólido que precipitó se filtró y se purificó de etanol (fig. 1).
]]> Fig. 1. Síntesis de 4-aril-5-oxo-2,7,7-trimetil-1,4,6,6,8,8-hexahidroquinoleínas sustituidas.Los puntos de fusión se determinaron en tubos capilares en un Electrothermal C14500. Los espectros de resonancia magnética nuclear (RMN) se registraron a 250 MHz en un espectrómetro Bruker AC-250F en DMSO-d6. Los desplazamientos químicos d, se refirieron en ppm utilizando tetrametilsilano como estándar interno. Los espectros infrarojo (IR) se registraron con un instrumento Bruker IRS48 en pastillas de bromuro de potasio. Las reacciones se monitorearon por cromatografía de capa delgada realizadas en placas de sílica gel (Merck 60-F) y se utilizó como eluente benceno:metanol (4:1). Los espectros de masa se registraron en un equipo NERMAG R 10-10 usando ionización química (NH 3 ).
Los compuestos sintetizados (fig. 1) fueron:
HQ1: 3-carbonilmetoxi-2,7,7-trimetil -4 -fenil-5-oxo-1,4,6,6,8,8,hexahidroquinoleína.
HQ2: 3-carbonilmetoxi-2,7,7,-trimetil-4-(3'-nitrofenil)-5-oxo-1,4,6,6,8,8,hexahidroquinoleína.
HQ3: 3- acetil-2,7,7,-trimetil-4-fenil-5-oxo-1,4,6,6,8,8,hexahidroquinoleína.
HQ4: 3- acetil-2,7,7,-trimetil-4-(3'-nitrofenil)-5-oxo-1,4,6,6,8,8,hexahidroquinoleína.
HQ5: 3- carbonilmetoxi-2,7,7,-trimetil-4-(2'-clorofenil)-5-oxo-1,4,6,6,8,8,hexahidroquinoleína .
Se registró la fuerza de contracción de forma comparativa en músculo liso vascular (anillos de aorta abdominal de conejo) y en músculo ventricular (papilares de ventrículo derecho de rata).12
Los anillos de aorta abdominal fueron extraídos de conejos Nueva Zelandia machos con pesos corporales entre 2 000 y 3 000 g, y los músculos papilares de ventrículo derecho se extrajeron de ratas Wistar machos con pesos corporales entre 150 y 180 g. Todos los animales fueron suministrados por el Centro Nacional para la Producción de Animales de Laboratorio (CENPALAB) y sometidos a condiciones ambientales y de manejo convencionales, alimentados con pienso estándar para ratas suministrado por CENPALAB y recibieron agua ad libitum .
]]> Los animales fueron anestesiados con pentobarbital sódico (30 mg/kg) y heparinizados con heparina sódica (5 000 UI/kg) por vía intraperitoneal. Los anillos y los papilares se fijaron por un lado a un transductor fuerza-desplazamiento TB-612T (Nihon Kohden) y por otro, al fondo de una cámara de perfusión por la que fluía continuamente (10 mL/min) una solución Tyrode de la siguiente composición (mmol/L): NaCl, 140; KCl, 4; CaCl2 , 2; MgCl2, 0,5; hidroxietilpiperazina- N'- 2- ácido etanosulfónico (HEPES), 10 y glucosa, 5 (pH = 7,4, gaseada con O2). La contracción en los anillos de aorta fue inducida sustituyendo el NaCl por KCl (140 mmol/L) o adicionando noradrenalina (10 µmol/L) a la solución Tyrode, dejándose estabilizar de 8-10 min antes de la aplicación de los fármacos. Los papilares fueron estimulados eléctricamente mediante electrodos de campo de Ag/AgCl, con pulsos de 2 ms de duración y a una frecuencia de 1,25 Hz (ciclo básico de 800 ms) y de intensidad 2 veces el umbral diastólico; los pulsos fueron suministrados por un estimulador electrónico SEN 7103 (Nihon Kohden). Los experimentos se realizaron a una temperatura de 35 ºC.Los resultados fueron analizados mediante el ensayo-t de Student para muestras pareadas, tomando como nivel de significación p < 0,05 y se expresan como medias y errores estándar de las medias.
Las hexahidroquinoleínas sintetizadas (fig. 1) son cristales sólidos estables y se obtuvieron con muy buenos rendimientos (60-80 %).
HQ1: 3-carbonilmetoxi-2,7,7-trimetil -4 -fenil-5-oxo-1,4,6,6,8,8,hexahidroquinoleína. Este compuesto se obtuvo siguiendo el procedimiento general (fig. 1), usando b -aminocrotonato de metilo y benzaldehído. Rendimiento: 66 %. t.f: 268-270 oC. IR (KBr, cm-1): 3 270 (NH); 1 709 (C=O); 1 657 (C=O); 1 625 (C=C); 1 206 (C-O). RMN-1H (DMSOd6) d (ppm): 9,05 (s, 1H, NH); 7,21-7,12 (m, 5H, H2', H3', H4', H5', H6'); 5,15 (s, 1H, H4); 3,69 (s, 3H, OCH 3 ); 2,45 (d, 1H, H8a, J =16,1); 2.36 (d, 1H, H8b, J =16,1); 2,31 (s, 3H, CH3); 2,27 (d, 1H, H6a, J =16,5); 2,01 (d, 1H, H6b, J =16,5); 1,16 (s, 3H, CH3 ); 1,01 (s, 3H, CH3). RMN-13C (DMSOd6) d (ppm): 195,4 (CO); 167,9 (COO); 147,8 (C8a); 144,5 (C2); 144,1 (C1'); 128,1 (C6', C2'); 127,7 (C5', C3'); 126,4 (C4'); 112,5 (C4a); 105,8 (C3); 51,0 (OCH3); 50,7 (C6); 40,9 (C8); 36,4 (C4); 32,7 (C7); 29,4 (CH3-C7); 27,2 (CH3-C7); 19,3 (CH3). EM (IE) m/z (intensidad %): 325 (M+, 12); 293 ([M+CH3OH]+, 4); 248 ([M+C6H5]+, 100). Análisis elemental . Calculado para C20H23NO3 (325,41): C: 73,84; H: 7,12; N: 4,30. Determinado C: 73,87; H: 7.10; N: 4,36.
HQ2: 3-carbonilmetoxi-2,7,7,-trimetil-4-(3'-nitrofenil)-5-oxo-1,4,6,6,8,8,hexahidroquinoleína. Este compuesto se obtuvo siguiendo el procedimiento general (fig. 1), usando b -aminocrotonato de metilo y 3-nitrobenzaldehído. Rendimiento: 75 %. tf: 223-225 ºC. IR (KBr, cm-1) 3 270 (NH); 1 710 (C=O); 1 685 (C=O); 1 635 (C=C); 1 530 (nas NO2); 1 335 (ns NO2); 1 205 (C-O). RMN- 1H (DMSOd6) d (ppm): 9,28 (s, 1H, NH); 7,99 (s a, 2H, H2', H4'); 7,67 (d, 1H, H6', J =7,9); 7,53 (t, 1H, H5', J =7,8); 5,00 (s, 1H, H4); 3,54 (s, 3H, OCH3); 2,41 (d, 1H, H8a, J =17,0); 2,30 (d, 1H, H8b, J =17,0); 2,28 (s, 3H, CH3); 2,18 (d, 1H, H6a, J =16,1); 1,99 (d, 1H, H6b, J =16,1); 1,02 (s, 3H, CH3); 0,83 (s, 3H, CH3). RMN-13C (DMSOd6) d (ppm): 194,3 (CO); 166,9 (COO); 150,1 (C8a); 149,4 (C3'); 147,5 (C2); 145,2 (C1'); 134,8 (C6'); 130,0 (C5'); 122,1 (C2'); 120,9 (C4'); 109,2 (C4a); 102,2 (C3); 50,7 (OCH3); 49,9 (C6); 39,3 (C8); 36,1 (C4); 32,1 (C7); 28,2 (CH3-C7); 26,0 (CH3-C7); 18,3 (CH3). Análisis elemental: Calculado para C20H22N2O5 (370,41) C: 64,86; H: 5,94; N: 7,56. Determinado C: 64,92; H: 5,99; N: 7,53.
HQ3: 3-acetil-2,7,7,-trimetil-4-fenil-5-oxo-1,4,6,6,8,8,hexahidroquinoleína. Este compuesto se obtuvo siguiendo el procedimiento general (fig.1), usando 4-aminopent-3-en-2-ona y benzaldehído. Rendimiento: 72 %. tf: 212-214 ºC. IR (KBr, cm-1): 3 280 (NH); 1 710 (C=O); 1 680 (C=O); 1 620 (C=C). RMN-1H (DMSOd6) d (ppm): 9,09 (s, 1H, NH); 7,20-7,21 (m, 5H, H2', H3', H4', H5', H6'); 4,95 (s, 1H, H4); 2,37 (s, 3H, COCH3); 2,40 (d, 1H, H8a, J =16,0); 2,32 (d, 1H, H8b, J =16,0); 2.29 (s, 3H, CH3); 2,27 (d, 1H, H6a, J =16,3); 2,01 (d, 1H, H6b, J =16,3); 1,01 (s, 3H, CH3); 0,78 (s, 3H, CH3). RMN-13C (DMSOd6) d (ppm): 197,1 (COCH3); 194,2 (CO); 148,9 (C8a); 146,2 (C2); 144,3 (C1'); 127,9 (C6', C2'); 127,4 (C5', C3'); 125,8 (C4'); 112,4 (C4a); 103,7 (C3); 50,2 (C6); 39,4 (C8); 36,2 (C4); 32,0 (COCH3); 32,1 (C7); 29,7 (CH3-C7); 26,2 (CH3-C7); 19,0 (CH3). EM (IE) m/z (intensidad %): 309 (M+, 12); 272 (40); 232 ([M+C6H5]+. Análisis elemental: Calculado para C20H23NO2 (309.17) C:77,66; H: 7,44; N: 4,53.Determinado C: 77,70; H: 7,42; N: 4,52.
HQ4: 3- acetil-2,7,7,-trimetil-4-(3'-nitrofenil)-5-oxo-1,4,6,6,8,8,hexahidroquinoleína. Este compuesto se obtuvo siguiendo el procedimiento general (fig. 1), usando 4-aminopent-3-en-2-ona y 3-nitrobenzaldehído. Rendimiento: 81 %. tf: 199-202 ºC. IR (KBr, cm-1) : 3 295 (NH); 1 716 (C=O); 1 685 (C=O); 1 625 (C=C). RMN-1H (DMSOd6) d (ppm): 9,15 (s, 1H, NH); 8,13 (d, 2H, H3', H5', J =7,9); 7,49 (d, 2H, H2', H6', J =7,9); 5,23 (s, 1H, H4); 2,45 (s, 3H, COCH3); 2,38 (d, 1H, H8a, J =17,1); 2,25 (d, 1H, H8b, J =17,1); 2,21 (d, 1H, H6a, J =16,3); 1,97 (d, 1H, H6b, J =16,3); 2,15 (s, 3H, CH3); 1,10 (s, 3H, CH3); 0,85 (s, 3H, CH3). RMN-13C (DMSOd6) d (ppm): 197,1 (COCH3); 194,2 (CO); 153,1 (C8a); 148,2 (C4'); 144,2 (C2); 143,3 (C1'); 129,5 (C6', C2'); 124,2 (C5', C3'); 112,4 (C4a); 105,7 (C3); 50,2 (C6); 40,5 (C8); 39,0 (C4); 34,5 (C7); 32,1 (COCH3); 25,7 (CH3-C7); 24,2 (CH3-C7); 19,0 (CH3 ). EM (IE) m/z (intensidad %): 354 (M+, 28); 272 (40); 232 ([M+C6H4NO2]+ , 190 (20). Análisis elemental: Calculado para C20H22N2O4 (354,41): C: 67,79; H: 6,26; N: 7,90. Determinado C: 67,85; H: 6,18; N: 7,96.
HQ5: 3- carbonilmetoxi-2,7,7,-trimetil-4-(2'-clorofenil)-5-oxo-1,4,6,6,8,8,hexahidroquinoleína . Este compuesto se obtuvo siguiendo el procedimiento general (fig. 1), usando b -aminocrotonato de metilo y 2-clorobenzaldehído. Rendimiento: 63 %. tf: 248-250 ºC. IR (KBr, cm-1): 3 280 (NH); 1 710 (C=O); 1 658 (C=O); 1 625 (C=C); 1 200 (C-O). RMN-1H (DMSOd6) d (ppm): 9,15 (s, 1H, NH); 7,35 (m, 1H, H3'); 7,25 (m, 2H, H4', H5'); 7,10 (m, 1H, H6'); 5,39 (s, 1H, H4); 3,59 (s, 3H, OCH3); 2,40 (d, 1H, H8a, J =16,2); 2,33 (d, 1H, H8b, J =16,2); 2,30 (s, 3H, CH3); 2,28 (d, 1H, H6a, J =16,1); 2,05 (d, 1H, H6b, J =16,1); 1,05 (s, 3H, CH3); 0,93 (s, 3H, CH3). RMN- 13C (DMSOd6) d (ppm): 195,6 (CO); 168,6 (COO); 147,3 (C8a); 144,4 (C2); 138,7 (C1'); 132,3 (C2'); 130,0 (C3'); 128,6, 127,5 (C4', C5'); 126,4 (C6'); 111,3 (C4a); 105,1 (C3); 51,8 (OCH3); 50,7 (C6); 40,9 (C8); 35,6 (C4); 32,5 (C7); 27,2 (CH3-C7); 29,4 (CH3-C7); 19,1 (CH3). EM (IE) m/z (intensidad %): 359/361 (M+, 15/6); 327/329 ([M+CH3OH]+, 3/1); 324 (M+,-Cl, 12); 248 ([M+C6H4-Cl]+, 100). Análisis elemental: Calculado para C20H22ClNO3 (359,85): C: 67,76; H: 6,16; N: 3,89. Determinado C: 67,84; H: 6,21; N: 3,69.
A todos estos compuestos se les evaluaron las acciones farmacológicas cardiovasculares y se compararon con la clásica nifedipina. Se estudiaron las acciones sobre la actividad contráctil de músculo cardíaco (papilares de ventrículo derecho de rata) y liso vascular (anillos de aorta abdominal de conejo), buscando cuáles de ellas tenían potencialidades vasodilatadoras. En el caso de los compuestos con actividad vasodilatadora, se prestó especial atención a la vasoselectividad de estos.
Todos los compuestos mostraron acciones antagonistas del calcio, son inotropo-negativos y vasorelajantes que se resumen en la tabla.
]]> Tabla . Efectos de las hexahidroquinoleínas y de la nifedipina sobre las contracciones cardíaca y aórtica.| Compuesto | IC50 corazón | IC50 aorta | IVS |
| Nifedipina | 0,03 | 0,007 | 4,28 |
| ]]> HQ1 | 1,66 | 1,7 | 0,98 |
| HQ2 | 1,22 | 1,15 | 1,06 |
| HQ3 | 6,01 | ]]> 0,32 | 18.78 |
| HQ4 | 4,06 | 0,54 | 7.52 |
| HQ5 | 1,88 | 1,87 | 101 |
Se expresan las concentraciones (µmol/L) inhibitorias en el 50 % (IC50) y los índices de vasoselectividad (IVS = IC50 corazón/IC50 aorta).
Los valores expresados son los IC50 obtenidos por el ajuste de las medias experimentales (n= 7 para cada concentración entre 0,001 y 100 µmol/L) a una función de Hill Y= 100/[1+(x/IC50)N], donde Y es el porcentaje de inhibición, x es la concentración del compuesto, N es el número de Hill e IC50 es la concentración que induce el 50 % de inhibición.
Dos compuestos de esta serie tienen ciertas potencialidades como vasodilatadores, la HQ3 y la HQ4 (fig. 2), debido a que sus valores de concentración que inhiben el 50 % de las contracciones (IC50) sobre corazón son mayores que los valores de IC50 sobre músculo liso vascular, presentando cierta vasoselectividad, aunque no marcada.
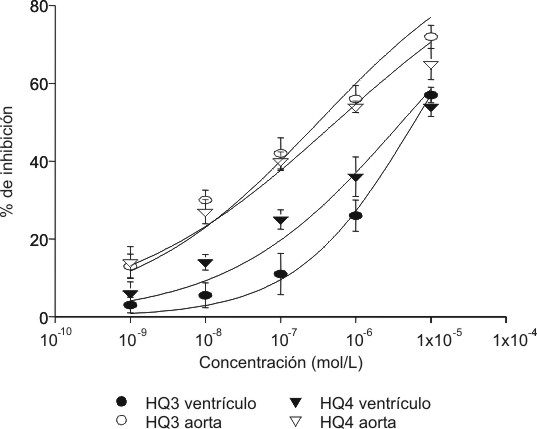
Fig. 2. Efectos de las hexahidroquinoleínas HQ-3 y HQ-4 sobre la fuerza cotráctil. Influencia de la concentración de HQ-3 y HQ-4 sobre la contracción incluida por KCl en anillos de aorta de conejo y sobre la fuerza contráctil de papilares de ventrículo derecho de rata. Los puntos representan las medias ± desviaciones estándar de al menos 5 experimentos para cada concentración. Las curvas están ajustadas a las medias esperimantales sobre la base de la función de Hill.
Puede demostrarse con estos resultados que la serie de las hexahidroquinoleínas posee actividad de tipo antagonista del calcio vasodilatadora. No obstante son compuestos con poca potencia de acción. En particular la HQ3 y la HQ4 son compuestos que muestran la mayor vasoselectividad y son comparables con la nifedipina en este sentido, aunque menos potentes. El resto de los compuestos de esta serie carece de interés por cuanto sus acciones sobre músculo liso y corazón son equipotentes.
Todos los compuestos estudiados en esta serie carecen de acciones significativas (p < 0,05) sobre la contracción aórtica inducida por noradrenalina (10 µmol/L), incluida la nifedipina.
En los espectros IR de todos los compuestos se observan señales de acetona carbonílica alrededor de 1710 cm-1 y muestran bandas aromáticas a 1 580 y 1 470 cm-1 y para los compuestos HQ1, HQ2 y HQ7 se observa la banda COOMe a 1 720 cm-1. Los espectros de RMN 1H de todos los compuestos mostraron los protones sobre C6 y C8 como parte de un sistema AB a 2,1-2,4 ppm. Los espectros de RMN 13C de los compuestos mostraron las señales para los carbonos olefínicos C3 y C4a (d ~ 102.-112. ppm), y C2 y C8a (d ~ 144-153 ppm), a valores de d diferentes a los valores típicos de desplazamiento químico de olefinas (d ~ 125 ppm), lo que se debe al efecto push-pull presente en estos sistemas, donde los grupos carbonilos de éster o cetona se encuentran conjugados a los dobles enlaces endocíclicos de la 1,4-DHP.
Desde el punto de vista conformacional, en estos compuestos y derivados análogos han sido estudiados, tanto por difracción de rayos X como mediante modelación molecular empleando métodos mecánico-cuánticos. Estos estudios han revelado que el anillo de 1,4-DHP presenta una conformación de bote aplanado, donde el sustituyente arilo de la posición 4 se ubica pseudoaxial y en un plano que bicepta al plano de la 1,4-DHP. El grupo éster de la posición 3 se encuentra conjugado al doble enlace endocíclico de la 1,4-DHP.13,14 Estas características conformacionales coinciden con las descritas para compuestos análogos con probada actividad biológica.
Los resultados indican que 2 compuestos de esta serie tienen ciertas potencialidades como antagonistas del calcio vasodilatadores, la HQ3 y la HQ4. Ambas muestran índices de vasoselectividad similares al reportado 2,15 y el obtenido por este estudio para la nifedipina, y está en los órdenes de magnitud de los obtenidos para 1,4-DHP de nuevas generaciones.1-3,12 No obstante, HQ3 y HQ4 son menos potentes que la nifedipina en al menos 2 órdenes de magnitud de concentración.
Aunque no existe en la literatura una relación estructura-actividad definida para las hexahidroquinoleínas y con el número de compuestos evaluados, en este estudio no es factible establecerla tampoco por el reducido número de compuestos evaluados, sí se puede señalar que resulta de interés continuar la investigación sobre la base de las estructuras de las HQ3 y HQ4. Si el incremento en la liposolubilidad de estos compuestos aumenta la potencia de acción y la vasoselectividad, como se ha definido con las 1,4-DHP, 1-3 estructuras derivadas de HQ3 y HQ4 pudieran constituir moléculas alternativas que se incorporarían al arsenal de los antagonistas del calcio.
Five hexahydroquinolines were prepared through one-step synthesis from an aromatic aldehyde called ß- alkyl aminocrotonate (enamin)and dimedone in pure ethanol as solvent. The effects of the five hexahydroquinolines on contractility of rabitt´s aorta rings and on contractility of papillar muscles of rat´s right ventricle were characterized in a comparative way to classical nifedipine. All hexahydroquinolines inhibited the contractile activity of both vascular smooth muscle and cardiac muscle, and they showed effects that are characteristic of calcium antagonist compounds, although with less potent action than nifedipine. However, two of the studied hexahydroquinolines presented some mild vasoselectivity.
Key words: Calcium antagonists, hexahydroquinolines, dihydropyridines, vasoselectivity.
1. Sica DA. Calcium channel blocker class heterogeneity: select aspects of pharmacokinetics and pharmacodynamics. J Clin Hypertens ( Greenwich ). 2005;7(4 Suppl 1):21-6.
2. Triggle DJ. The pharmacology of ion channels with particular reference to voltage-gated Ca 2+ channels. Eur J Pharmacol. 1999;375:311-25.
3. Basile J. The role of existing and newer calcium channel blockers in the treatment of hypertension. J Clin Hypertens ( Greenwich ). 2004;6(11):621-29;quiz 630-1.
4. Rose U. Hexahydroquinolines with calcium-modulatory effects: synthesis and pharmacologic action. Arch Pharm. 1990;323:281-6.
5. ______. Vinylogous and coupled hexahydroquinolines and dihydropyridines with calcium modulating effects. Phram Acta Helv. 1990;65:178-85.
6. Rose U, Drager M. Synthesis, configuration and calcium modulatory properties of enantiomerically pure 5-oxo-1,4,5,6,7,8-hexahydroquinoline-3-carboxylate. J Med Chem. 1992;35:2238-43.
7. Safak C, Erdemli I, Sunal R. Synthesis of some 1,4,5,6,7,8-hexahydroquinoline derivatives and their calcium antagonistic activity. Arzneim Forsch. 1993;43:1052-5.
8. Safak C, Ozkanli F, Erol K, Aktan Y. 3- Acetyl- 4-aryl-5 -oxo- 2,7,7-trimethyl- 1,4,5,6,7,8- hexahydroquinoline derivatives and their calcium antagonistic activities. Arzneim Forsch. 1995;45:1154-6.
9. Simsek R, Safak C, Erol K, Sirmagul B. Synthesis of hexahydroquinoline derivatives possessing calcium antagonistic activity. Pharmazie. 2001;56(8):665-6.
10. Simsek R, Safak C, Erol K, Ataman S, Ulgen M, Linden A. Synthesis, evaluation of the calcium antagonistic activity and biotransformation of hexahydroquinoline and furoquinoline derivatives. Arzneimittelforschung. 2003; 53(3):159-66.
11. Kismetli E, Safak C, Erol K, Sirmagul B, Linden A. Studies on 3-diethylaminocarbonyl-1,4,5,6,7,8-hexahydroquinoline derivatives and their calcium channel antagonistic activities in vitro. Arzneimittelforschung. 2004; 54(7):371-5.
12. Galán L, Talavera K, Vassort G, Alvarez JL. Characteristics of Ca2+ channel blockade by oxodipine and elgodipine in rat cardiomyocytes. Eur J Pharmacol. 1998;357:93-105.
13. Duque J, Pomes R, Suárez M, Ochoa E, Punte G, Echevarría G. Crytal structure of methyl-2,7,7-trimethyl-4-phenyl-5-oxo-1,4,5,6,7,8-hexahydroquinoline-3-carboxylate. Bol Soc Chil Quím. 2000;45:175-80.
14. Suárez M, Verdecia Y, Ochoa E, Martín N, Martínez R, Quinteiro M, et al. Synthesis and structural study of novel 1,4,5,6,7,8/hexahydroquinolines. J Heterocycl Chem. 2000;37:735-42.
15. Godfraind T, Eglème C, Finet M, Jaumin P. The actions of nifedipine and nisoldipine on the contractile activity of human coronary arteries and human cardiac tissue in vitro. Pharmacol Toxicol. 1987;61:79-84.
Recibido: 31 de mayo de 2006. Aprobado: 3 de julio de 2006.
Dra. C. Loipa Galán Martínez . Laboratorio de Electrofisiología, Departamento de Investigaciones, Instituto de Cardiología y Cirugía Cardiovascular. Calle 23 No. 654, Vedado, CP 10 400, Ciudad de La Habana, Cuba. Correo electrónico: logama@infomed.sld.cu
1Doctora en Ciencias Farmacéuticas. Investigadora Agregada.
2Doctor en Ciencias Químicas. Profesor Asistente. Laboratorio de Síntesis Orgánica. Facultad de Química. Universidad de La Habana.
3Técnica en Química. Laboratorio de Síntesis Orgánica. Facultad de Química. Universidad de La Habana.
4Doctora en Ciencias Químicas. Profesora Titular. Laboratorio de Síntesis Orgánica. Facultad de Química. Universidad de La Habana.
5Doctor en Ciencias. Investigador Titular.