ARTÍCULO ORIGINAL
Incremento de disolución de un derivado del furano mediante la técnica de secado por atomización
Improvement of Furane derivate dissolution rate using spray drying technique
]]>
MSc. Antonio Iraizoz Barrios,I Dr. C. Bernard Bataille,II Dr. C. Nilo Castanedo Cancio,III Dr. C. Antonio Iraizoz Colarte,IV Dra. C. Grosmaire Lidwine,V Dra. C. María Aurora Barrios Álvarez,IV Téc. Giles BaylacVI
I Centro de Investigación y Desarrollo de Medicamentos (CIDEM). La Habana, Cuba.
II Laboratorio de Farmacia Galénica, Universidad de Montpellier 1, Francia.
III Centro de Bioactivos Químicos, Universidad Central de Las Villas. Las Villas, Cuba.
IV Instituto de Farmacia y Alimentos, Universidad de La Habana. La Habana, Cuba.
V Laboratorio de Física Molecular y Estructural, Universidad de Montpellier 1. Francia.
VI Universidad de Montpellier 1. Francia.
]]>
RESUMEN
Objetivo: incrementar la solubilidad en agua del 2-bromo-5-(2-bromo-2-nitrovinyl)-furano (G1), un ingrediente farmacéuticamente activo sintetizado por el Centro de Bioactivos Químicos de la Universidad Central de Las Villas, con potente acción bactericida y fungicida, mediante la elaboración de macropartículas de dispersiones sólidas utilizando un proceso de secado por atomización.
Métodos: se realizó un ensayo preliminar de secado por atomización de la suspensión de G1, compuesta por: 10 g de G1, 1 g de Aerosil (Aerosil®, Degusa, Bélgica), 1 g de laurilsulfato de sodio y 100 mL de agua. La atomización se efectuó en un equipo de laboratorio (Buchi Mini Dryer spray) a 90 ºC. La dispersión sólida obtenida fue caracterizada físico-químicamente mediante difracción de rayos X, granulometría láser por el método de difracción angular, calorimetría diferencial de barrido, microscopia electrónica de barrido y espectrofotometría de absorción infraroja.
Resultados: las partículas obtenidas presentaron un pequeño tamaño, forma esférica y un incremento de la cristalinidad del G-1; no se encontraron interacciones entre los componentes de la dispersión ni presencia de productos de degradación, y la solubilidad del G-1 en agua resultó notablemente incrementada.
Conclusiones: el producto obtenido por la técnica de secado por atomización incrementó apreciablemente la solubilidad del G1 sin afectar los grupos funcionales, responsables de la actividad terapéutica que se le reportan al ingrediente activo estudiado. Estos alentadores resultados sugieren la necesidad de continuar estudios para la optimización del proceso y realizar al producto obtenido ensayos de estabilidad con el objetivo de su futura inclusión en formas farmacéuticas de dosificación.
Palabras clave: 2-bromo-5 (2-bromo-2-nitrovinyl)-furano, secado por atomización, micropartículas, disolución.
ABSTRACT ]]>
Objective: to increase the solubility of 2-bromium-5(2-bromium-2-nitrovinyl)-furane (G1), one pharmaceutically active ingredient with potent bactericidal and fungicidal action, synthesized through the preparation of solid dispersion macroparticles based on spray-drying process in the Center of Chemical Bioactives of the Central University in Las Villas province.Key words: 2-bromium-5(2-bromium-2-nitrovinyl, spray drying, microparticules, dissolution.
INTRODUCCIÓN
Muchos de los ingredientes activos que se obtienen en la actualidad son prácticamente insolubles en agua. Esto ha significado un importante desafío para el especialista farmacéutico que debe desarrollar productos que sean biodisponibles, además de estables y seguros. Es por esto que todo esfuerzo que signifique un aumento de la solubilidad de estas sustancias, constituye un aspecto de especial interés en el desarrollo de nuevas formas de dosificación.1-3 ]]>
El sistema de clasificación de productos biofarmacéuticos (BCS) es una herramienta científica para clasificar un fármaco y esta se basa en la consideración de la solubilidad acuosa y la permeabilidad intestinal.4 La FDA proporciona una guía de gran utilidad para la Industria Farmacéutica en la sustitución de los estudios de bioequivalencia y de biodisponibilidad de los medicamentos sólidos de administración por la vía oral de liberación inmediata.4-6Los medicamentos que clasifican como clase II (con la baja solubilidad y alta permeabilidad) y los clasificados como IV (baja solubilidad y baja permeabilidad) se caracterizan por presentar velocidades de disolución irregulares y consecuentemente baja biodisponibilidad.
La ecuación de Noyes-Whitney modificada7,8 proporciona algunas ideas de cómo pudiera incrementarse la solubilidad de productos pobremente solubles en agua para minimizar la limitación que pueden tener en la biodisponibilidad al administrase por la vía oral.
donde:
dC/dt: velocidad de disolución.
A: área superficial disponible a la disolución.
D: coeficiente de difusión del compuesto.
Cs: solubilidad del producto en el medio de disolución. ]]>
C: concentración de ingrediente activo en el medio al tiempo t.H: espesor de la capa de difusión adyacente a la superficie del compuesto en disolución.
Se han descritos algunos métodos para incrementar la velocidad de disolución basados en estos parámetros. Las principales posibilidades para mejorar la disolución de acuerdo con este análisis son: incrementar el área de superficie disponible para la disolución, mediante la disminución del tamaño de las partículas sólidas y/o por la optimización del las características de humectación de la superficie del compuesto con la finalidad de disminuir las dimensiones de la capa de disolución.9
El molinado es usado para disminuir el tamaño de partícula de materias primas, constituye una práctica ampliamente utilizada en la industria debido a sus ventajas, entre estas el bajo costo de producción y la facilidad de escalado. Otra posibilidad es la complejación/solubilización, usando sustancias superficialmente activas y el empleo de dispersiones sólidas.
En resumen, el proceso de disolución y la solubilidad son mejorados a partir de la reducción del tamaño de partícula, el uso de cosolventes, surfactantes y agentes complejantes.10-12
Una estrategia con renovado interés, lo es la formulación de dispersiones sólidas en las cuales se dispersa un ingrediente activo poco soluble en un vehículo inerte e hidrofílico en el estado sólido. Esta técnica, trae consigo una significativa disminución del tamaño de partícula, posiblemente al nivel molecular en unión con el efecto adicional de que tiene el dispersar el ingrediente activo en el vehículo hidrofílico en la solubilidad, el cual puede reducir el tiempo requerido para la completa disolución en el tracto gastrointestinal. El éxito de una dispersión sólida depende mucho de la elección del excipiente, y es por esto que se han hecho muchos esfuerzos en este sentido para ensayar el potencial de diferentes polímeros de uso farmacéutico, surfactantes y combinación de estos.13-17
El secado por atomización es usado frecuentemente en la preparación de micropartículas de dispersiones sólidas, mientras que pueden producirse también partículas de polvo fino al mismo tiempo.18,19
El 2-bromo-5-(2-bromo-2-nitrovinyl)-furano (G1), es un ingrediente farmacéuticamente activo sintetizado por el Centro de Bioactivos Químicos de la Universidad Central de Las Villas, Cuba. Este es un polvo amarillo claro y las partículas tienen superficie lisa con un olor característico. Es libremente soluble en dimetilformamida, éter etílico, cloroformo, dimetilsufóxido y benceno, soluble en tetracloruro de carbono y polietilenglicol 400, poco soluble en metanol y etanol 90 º, casi insoluble en etanol 70 º, éter de petróleo (40-60 ºC), n hexano, y agua. Tiene una masa molecular de 296,924 y un punto de fusión de aproximadamente 90 ºC, e identificado por espectroscopia UV, por un pico a 389 nm. Es también muy sensible a la luz.
En ensayos in vitro el G1 ha demostrado tener una potente acción bactericida y fungicida comprobada en 908 cepas de bacterias gramnegativas y 119 grampositivas y de ellas solo 11 cepas de 4 series mostraron una concentración mínima inhibitoria de 50 µg/mL. Estas propiedades abren nuevas posibilidades de aplicación en la terapéutica.
Por todos los antecedentes antes mencionados, el objetivo central de este trabajo es incrementar la solubilidad en agua del 2-bromo-5-(2-bromo-2-nitrovinyl)-furano (G1), a partir de la elaboración de micropartículas de dispersiones sólidas mediante un proceso de secado por atomización. ]]>
MÉTODOS
Materiales
2-bromo-5(2-bromo-2-nitrovinyl)-furano (G1) y vitrofural, una dispersión sólida que contiene G1 y 70 % de polietilenglicol 6 000, (Merck- Schuchardt), preparada por método de fusión, que fueron obtenidos en el Centro de Bioactivos Químicos de la Universidad Central de Las Villas. Laurilsulfato de sodio (SLS, de una pureza >99 %) suministrado por Sigma Chemical Company (ST. Louis, MO) Aerosil (Aerosil®, Degusa, Bélgica), agua destilada, desionizada y filtrada, obtenida en el laboratorio.
Caracterización físico-química
Difracción de rayos X ]]>
El G1 de partida, fue sometido a difracción de rayos X, utilizando para ello un difractómetro de la firma Philips (PW 1730, 20KV, 40 Ma). Las muestras fueron evaluadas entre 2 y 30 ºC.
Análisis granulométrico
El G1 inicial, así como el polvo obtenido a partir del molinado, se sometieron a granulometría láser en un Mastersizer modelo x (Malven Instrument Ltd. Malvern UK) por el método de difracción angular. Se analizaron muestras de G1 inicial y G1 molinado, cinco réplicas de cada uno.
Calorimetría diferencial de barrido
La calorimetría diferencial de barrido (DSC) se realizó con un equipo de la firma Perkin, modelo DSC 6, trabajando entre 30 y 295,5 ºC.
]]>
Microscopia electrónica de barrido
Los productos: G1 inicial, molinado y dispersión sólida se observaron en un microscopio electrónico de barrido Hitachi, modelo S-4000, cubriendo las partículas con oro/paladio.
Espectroscopia de absorción infrarroja
Se usó el método de espectroscopia FTIR-ATR (Fourier trasform infrared-attenuated total reflectance) con instalación de diamante ATR (reflección total atenuada). La profundidad de penetración de la onda fue definida por:
l: longitud de onda del rayo incidente
n1: constante óptica del diamante. (n1» 2,38) ]]>
n2: constante óptica de la muestraji: ángulo de incidencia
Se trabajó entre 650 y 4 000 cm-1 a temperatura ambiente.
Métodos para mejorar la solubilidad en medio acuoso
Para mejorar la solubilidad del G1 en medio acuoso se utilizaron los siguientes métodos:
Molinado
Se pesaron 50 g de G1 en balanza Mettler, modelo AE-240 y se molinaron en un molino de bolas Frish, a la velocidad de 200 ciclos x min durante 1 h.
]]>
Dispersión sólida
La dispersión sólida es la mezcla del ingrediente a dispersar en una matriz inerte que tendrá el papel de vehículo o carrier.
Se estudió el vitrofural, una dispersión sólida obtenida en Cuba la que está compuesta por 70 % de polietilenglicol 6 000 y 30 % de G1, preparada por el método de fusión. Los dos componentes que forman esta dispersión fueron mezclados a temperaturas superiores al punto de fusión de ambos compuestos. El resultado de esta cofusión fue solidificado en un recipiente de vidrio y posteriormente molinado y tamizado.
Secado por atomización
Se realizó un ensayo preliminar de secado por atomización de la suspensión de G1, compuesta por: 10 g de G1, 1 g de Aerosil (Aerosil®, Degusa, Bélgica), 1 g de SLS y 100 mL de agua.
La atomización fue llevada a cabo en un equipo de laboratorio (Buchi Mini Dryer spray) a 90 ºC.
La solubilidad del producto seco obtenido fue comparada con respecto al Vitrofural, añadiendo 10 mg de cada producto en 1 L de agua a temperatura ambiente y agitando durante 20 min, se filtró por papel y se analizó por espectrometría UV-VIS en un espectrofotómetro Shimadzu, model 1601 a una longitud de onda (l) de 389 nm. ]]>
RESULTADOS
Caracterización físico-química
Difracción de rayos X
Se obtuvieron difractogramas de cristales de G1 sin molinar y del secado por atomización. Estos pueden apreciarse en la figura 1, donde se puede observar un incremento en la cristalinidad.
]]> Análisis granulométrico
Los resultados del análisis granulométrico por difracción de rayos láser se muestran en la tabla, en la que se aprecia que el G1 inicial presenta un tamaño de partícula medio de 188,27 µm, el proceso de molinado permitió una disminución de la talla de las partículas hasta 65,18 µm.
Calorimetría diferencial de barrido
En la figura 2 se reportan los resultados del estudio de la DSC. Este ensayo permitió observar el punto de fusión del G1 en 92,5 ºC y su descomposición 180 ºC o más. No existen diferencias apreciables entre los compuestos estudiados.
]]>
La microscopia electrónica permitió observar los cristales de los diferentes polvos (Fig. 3). Las fotos muestran la estructura cristalina del G1 así como la reducción de talla en el caso del G1 molinado. También es importante observar la forma esférica de las partículas obtenidas en el proceso de secado por atomización (G1, SLS) y la estructura amorfa de las partículas obtenidas en la dispersión sólida PEG-G1. Al realizar las observaciones, se debe tener en cuenta la diferencia de resolución en las microfotografías.
Espectroscopia de absorción infrarroja
Mediante este método se analizaron muestras de G1, su producto de degradación (monobromado), el producto secado por atomización y los excipientes utilizados.
El espectro de absorción IR obtenido para el G1 se muestra en la figura 4, además del espectro FTIR-ATR de los productos de degradación del G1 en la región de 700 a 1 700 cm-1. La parte correspondiente a las vibraciones de elongación de los enlaces C-H (alrededor de 3 000 cm-1 no se ve representada, pero no se observan diferencias significativas entre el G1 y sus productos de degradación. En la región correspondiente a las longitudes de onda más bajas (Fig. 4), el espectro muestra considerables diferencias, como la desaparición de bandas asociadas al modo vas NO2 para el producto de degradación (monobromado). Esto no resulta coherente con la estructura supuesta de este compuesto y parece indicar la sustitución del grupo NO2. Para llegar más lejos en estas consideraciones se hace necesario obtener más información sobre la reacción de degradación y sobre las dosificaciones después de la reacción. ]]>
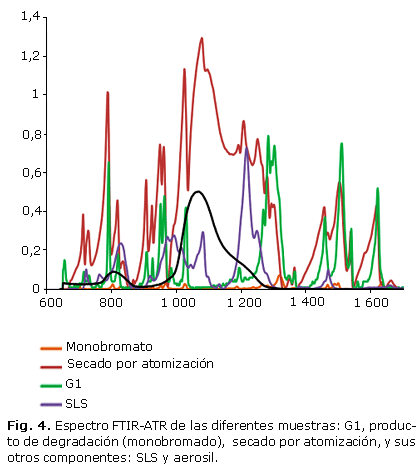
Sin embargo, la degradación del compuesto de G1 traería consigo la sustitución del bromo por el hidrógeno en el grupo vinilo.
Parece, de acuerdo con los espectros obtenidos, que la posición de los modos de C=C (vinilo) para el monobromado se corre hacia longitudes de onda más altas C=C (G1): 1 620 cm-1 y C=C (monobromado): 1 633 cm-1. De hecho, por el efecto de masa y de atracción electrofílica, un grupo de Br sustituido en un C sp2, tiene tendencia a disminuir la frecuencia de vibración del doble enlace C=C.
El espectro FTIR-ATR del producto obtenido por secado por atomización también se muestra en la figura 4, en la que se presenta el espectro IR a bajas longitudes de onda (700-1 700 cm-1) para facilitar el análisis comparativo del producto obtenido y sus elementos constituyentes.
El espectro del producto obtenido por secado por atomización, muestra las principales bandas asociadas al SD claramente: 2 918, 2 850,1 661, 1 249, 1 206 y 833 cm-1.
El espectro del aerosil presenta dos grandes macizos centrados en 1 067 y 806 cm-1. Estos son fácilmente identificables en el espectro del producto obtenido por secado por atomización y provoca un desplazamiento de la vibración de las bandas en relación con la línea base de los dos dominios correspondientes.
Por otra parte, los modos de vibraciones relativas en el G1 no sufren desplazamiento después de la atomización, lo que sugiere que no hay interacción entre el ingrediente activo y los excipientes utilizados en dicho proceso.
]]>
El espectro UV de los diferentes polvos estudiados se muestran en la figura 5, en la que se puede observar el comportamiento de la solubilidad en agua en las tres opciones utilizadas para mejorar esta propiedad del G1; se puede apreciar que el producto secado por atomización en presencia de un agente hidrofílico permite incrementar en más de 20 veces la solubilidad del 2-bromo-5(2-bromo-2-nitrovinyl)-furano, por lo que queda demostrado el interés del secado por atomización en el mejoramiento de la solubilidad del G1 en agua.
DISCUSIÓN
En el ensayo de difracción de rayos X se pudo apreciar que la intensidad de los picos correspondiente al G1 se veía incrementada sin variación en la forma, lo cual puede asumirse como un aumento en la cristalinidad después del proceso de secado por atomización. El proceso de molinado del G1 de partida causó una disminución del tamaño de partícula apreciable.
La DSC permitió definir la temperatura a la cual es posible trabajar con el ingrediente activo, en el proceso de secado por atomización, sin correr el riesgo de que ocurra una degradación causada por el proceso.
Las fotos obtenidas en el estudio de las partículas mediante microscopia electrónica de barrido, ayudaron a la comprensión del perfil de disolución de las partículas, en las que la forma y el tamaño tienen una influencia notable.
Los resultados de la espectroscopia infrarroja, están de acuerdo con los obtenidos en DSC y en la difracción de rayos X. ]]>
El producto obtenido por la técnica de secado por atomización incrementó apreciablemente la solubilidad del G1 sin afectar los grupos funcionales, responsables de la actividad terapéutica que se le reportan al ingrediente activo estudiado. Estos alentadores resultados sugieren la necesidad de continuar estudios para la optimización del proceso y realizar al producto obtenido ensayos de estabilidad con el objetivo de su futura inclusión en formas farmacéuticas de dosificación.
REFERENCIAS BIBLIOGRÁFICAS
1. Wilkarsa S, Durand D, Delarbre JL, Bayllac G, Bataille B. The improvement of Ibuprofen dissolution rate through microparticles spray drying processed in an aqueous system. Drug Develop Ind Pharm. 2008;34:485-91.
2. Bittner B, Mountfield RJ. Intravenous administration of poorly soluble new drug entities in early drug discovery: the potential impact of formulation on pharmacokinetic parameters. Current Opin Drug Discov Develop. 2002;5:59-71.
3. Bittner B, Mountfield RJ. Formulations and related activities for the oral administration of poorly water-soluble compounds in early discovery animal studies. Pharm Ind. 2002;64:800-7. ]]>
4. Amidon G, Lennernas H, Shah VP, Crison JR. A Theoretical basis for a biopharmaceutical drug classification, the correlation of in vitro drug product dissolution and in vivo bioavailability. Pharm Res. 1995 ;12:413-20.
5. FDA Guidance for industry. Waiver of in vivo Bioavailability and Bioequivalence Studies for Immediate Release Solid Oral Dosage Forms Based on a Biopharmaceutics Classification System CDER/FDA. Silver Spring, MD: FDA;2000.
6. Ching-Ling Ch, Laurence XYu, Hwei-Ling L, Chyun-Yu Y, Chang-Sha L, Chen-His Ch. Biowaiver extension potential to BCS Class III high solubility-low permeability drugs: bridging evidence for metformin immediate-release tablet. Eur J Pharm Sci. 2004;22:297-304.
7. Noyes AA, Whitney WR. The rate of solution of solid substance in their own solutions. J Am Chem Soc. 1897;19:930-4.
8. Nernst, W. Theorie der reaktionsgeschwindigkeit in heterogenen Sistemen. Zeitschrift F Physik Chemie. 1904;47:52-5. ]]>
9. Leuner C, Dressman J. Improving drug solubility for oral delivery using solid dispersions. Eur J Pharma Biopharm. 2000;50:47-60.
10. Branchu S, Rogueda PG, Plumb AP, Cook W.G. A decision-support tool for the formulation of orally active, poorly soluble compounds. Eur J Pharm Sci. 2007;32:128-39.
11. Stegemann S, Leveiller F, Franchi D, de Jong H, Lindén H. When poor solubility becomes an issue: from early stage to proof of concept. Eur J Pharm Sci. 2007;31:249-61.
12. Pouton CW. Formulation of poorly water-soluble drugs for oral administration: physicochemical and physiological issues and the lipid formulation classification system. Eur J Pharm Sci. 2006;29:278-87.
13. Wang X, Michoel A, Van den Mooter G. Solid state characterisation of ternary solid dispersions composed of PVPVA 64, Myrj 64 and itraconazole. Int J Pharm. 2005;303:54-61. ]]>
14. Six K, Leuner C, Dressman JB, Verreck G, Peeters J, Blaton N, et al. Thermal properties of hot-stage extrudates of itraconazole and Eudragit E100, phase separation and polymorphism. J Therm An Cal. 2002;68:591-601.
15. Broman E, Khoo C, Taylor LS. A comparison of alternative polymer excipients and processing methods for making solid dispersions of a poorly water soluble drug. Int J Pharm. 2001;222:139-51.
16. Janssens S, Anné M, Rombaut P, Van den Mooter G. Spray drying from complex solvent systems broadens the applicability of Kollicoat IR as a carrier in the formulation of solid dispersions. Eur J Pharm Sci. 2009;37:241-8.
17. Kawakami K, Oda N, Miyoshi K, Funaki T, Ida Y. Solubilization behavior of a poorly soluble drug under combined use of surfactants and cosolvents. Eur J Pharm Sci. 2006;28:7-14.
18. Chauhan B, Shimpi S, Paradkar A. Preparation and evaluation of glibenclamide-polyglycolized glycerides solid dispersions with silicon dioxide by spray drying technique. Eur J Pharm Sci. 2005;26:219-30. ]]>
19. Kim EJ, Chun MK, Jang JS, Lee IH, Lee KR, Choi HK. Preparation of a solid dispersion of felodifine using a solvent wetting method. Eur J Pharm Biopharm. 2006;64:200-5.
Recibido: 28 de noviembre de 2011.
Aprobado: 19 de enero de 2012.
]]>
Antonio Iraizoz Barrios. Centro de Investigación y Desarrollo de Medicamentos (CIDEM). Ave. 26 No. 1605 entre Boyeros y Puentes Grandes. CP 10 600. Plaza de la Revolución, La Habana, Cuba. Correo electrónico: antonio.iraizoz@infomed.sld.cu ]]>