Formulación de cápsulas duras de Tamarindus indica L.
Formulation of hard capsules from Tamarindus indica L.
DrC. Jesús Rafael Rodríguez Amado,I Lic. Liana Pérez Rondón,I MSc. Ariadna Lafourcade Prada,I DrC. Julio César Escalona Arranz,I DrC. Antonio Iraizoz ColarteII
I Facultad de Ciencias Naturales. Universidad de Oriente. Santiago de Cuba. Cuba.
II Instituto de Farmacia y Alimentos. Universidad de La Habana. Cuba.
RESUMEN
Objetivo: formular cápsulas duras a partir de extracto blando de Tamarindus indica L.
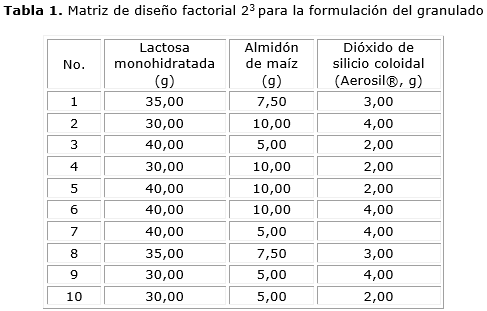
Métodos: se seleccionaron las cantidades de los excipientes lactosa monohidratada, almidón de maíz y dióxido de silicio coloidal (Aerosil®), utilizando un diseño factorial 23. Se seleccionó para envasar en cápsulas, el granulado con mejor fluidez y menor humedad residual. Se evaluó la calidad de las cápsulas duras.
Resultados: la formulación escogida fue lactosa monohidratada 35,0 g, Aerosil® 3,0 g y almidón de maíz 7,5 g, pues mostró buena fluidez y una humedad residual de 4,17 %. Las cápsulas duras formuladas, presentaron buena calidad tecnológica.
Conclusiones: se obtuvieron cápsulas duras que pueden ser preparadas, a pequeña escala, a nivel dispensarial.
Palabras clave: tamarindo, cápsulas, diseño factorial, extracto natural.
ABSTRACT
]]> Objective: to formulate hard capsules from Tamarindus indica L. soft extract. Key words: tamarind, capsules, factorial design, natural extract.
INTRODUCCIÓN
Desde la antigüedad, las especies vegetales han sido utilizadas con fines terapéuticos, para el tratamiento de diferentes enfermedades. En la actualidad, hay un retorno mundial a la utilización de los productos naturales, en especial de las plantas medicinales.1
Cuba cuenta con una variada y abundante flora medicinal. Dentro de esta, se encuentra el Tamarindus indica L. (Caesalpinaceae) o tamarindo como comúnmente se conoce. Esta es la planta medicinal más utilizada por la población, para el tratamiento de las enfermedades hepáticas,2 pues en el Sistema de Salud Cubano, no se cuenta con medicamentos hepatoprotectores. En este sentido, los pacientes consumen diariamente, de 4 a 6 L de decocción de las hojas, para tratar estas enfermedades.3
]]> A nivel dispensarial, se prepara el extracto fluido de tamarindo, pero su utilización se ve limitada en las hepatopatías por su alto contenido de etanol, además de producir leve irritabilidad de la mucosa bucal.4 Se ha informado la formulación de tabletas a partir del extracto fluido y blando de tamarindo EBT.5 Sin embargo, su producción industrial se ve limitada por la disponibilidad de material vegetal. El objetivo de este trabajo es realizar un estudio de formulación de cápsulas duras a partir del extracto blando estandarizado1 de las hojas de la especie Tamarindus indica L.
MÉTODOS
OBTENCIÓN Y CARACTERIZACIÓN DEL EXTRACTO BLANDO DE TAMARINDO
Se realizó la colecta y procesamiento del material vegetal, así como la obtención y caracterización de los extractos fluido y blando de tamarindo (EBT), utilizando los procedimientos informados por Rodríguez y otros.6
PREPARACIÓN DEL GRANULADO
Se pesaron y se colocaron en un mortero las cantidades pesadas de lactosa monohidratada (Contero Excipientes, Nueva Zelanda), almidón de maíz (Blanver, Brasil) y de dióxido de silicio coloidal (Aerosil®; Degusa A-200, Suiza). Se mezclaron y trituraron cuidadosamente hasta homogeneizar y posteriormente se pasaron por una maya de 250 µm. Se colocaron nuevamente en el mortero y se le añadió la cantidad prefijada de extracto blando de tamarindo y se mezcló, con ayuda del pistilo, hasta formar una masa uniforme. Se granuló manualmente pasando esta masa por una maya de 0,355 mm y se secó a 40 ± 2 ºC en estufa de vacío (Sartorius, Alemania) por espacio de 3 h. Se dejó enfriar y se degranuló triturando la masa seca en el mortero, hasta que toda la masa pasó por una maya de 250 µm.
DISEÑO EXPERIMENTAL
EVALUACIÓN DE LA CALIDAD DE LOS GRANULADOS
- Propiedades organolépticas: las propiedades organolépticas (olor, color y sabor) fueron evaluadas mediante inspección del material, utilizando los órganos de los sentidos.
- Determinación del índice de Hausner y el de compresibilidad: las densidades de vertido y asentamiento se determinaron a través del método de las probetas y se calcularon los índices de compresibilidad y de Hausner.7
- Tamaño de partículas: se realizó por tamizado, empleando tamices de 355, 250, 180 y 160 μm de apertura de malla. Se utilizó un equipo vibrador THYL-1 (Rusia) y un tiempo de tamizado de 15 min.8,9
- Evaluación de la forma: se tomaron microfotografías del granulado con un microscopio óptico (NOVEL, China), utilizando un aumento de 10x.10,11 Se utilizó para el procesamiento y captura de las imágenes el sistema automatizado EDn-2 2.0.4. China.
- Determinación de la velocidad de flujo y ángulo de reposo: la velocidad de flujo se determinó por el método del embudo9 y el ángulo de reposo por el método propuesto por la farmacopea estadounidense.7
- Determinación de la humedad residual: se realizó por el método gravimétrico,7 utilizando una balanza gravimétrica Sartorius (SA 325, Alemania).
]]>Se procedió por el método de Folin Ciocalteu adaptado por Rodríguez y otros.12
SELECCIÓN DE LA MEJOR FORMULACIÓN DEL GRANULADO
Se seleccionó como mejor proporción, la que presentó mejores propiedades de flujo y compresibilidad y menor humedad residual. Del granulado seleccionado, se prepararon tres lotes, siguiendo el mismo procedimiento descrito anteriormente, para proceder a su caracterización, evaluando los mismos parámetros evaluados en el diseño experimental.
SELECCIÓN DEL TAMAÑO DE CÁPSULA APROPIADO
Se utilizó el método clásico, dividiendo la masa de granulado a envasar entre la densidad de asentamiento del mismo y seleccionando posteriormente el tamaño de cápsula apropiado.9
]]> PREPARACIÓN DE LAS CÁPSULAS DURAS DE TAMARINDO
El llenado de las cápsulas duras se realizó por el método manual a nivel dispensarial, descrito por Iraizoz y colaboradores.9
PREPARACIÓN DE LAS CÁPSULAS DURAS DE TAMARINDO
Propiedades organolépticas: se evaluó la uniformidad de color, olor y la apariencia de las cápsulas utilizando los órganos sensoriales.
Uniformidad de peso: se realizó utilizando el método descrito en la USP 30.7
Tiempo de desintegración de las cápsulas duras: se utilizó un equipo desintegrador de cesta (GMB, Alemania), con un volumen de 900 mL de agua destilada a una temperatura de 37 ± 1 ºC. Se tomaron seis cápsulas duras. Se colocó una cápsula en cada uno de los 6 tubos del equipo y se hizo funcionar a una velocidad de 50 r.p.m. durante 15 min. Todas las cápsulas deberán desintegrar antes de 5 min.
RESULTADOS
EVALUACIÓN DE LA CALIDAD DEL EXTRACTO BLANDO
]]> El EBT obtenido contiene 51,01 ± 1,23 % de sólidos totales, con una densidad relativa de 1,226 ± 0,033 g/mL y un pH de 2,8 ± 0,18. El contenido de polifenoles fue de 5,25 ± 0,11 % y de cenizas totales 2,14 ± 0,14 %.EFECTO DE LOS EXCIPIENTES SOBRE LAS PROPIEDADES DE LOS GRANULADOS
En todos los casos se obtuvo un granulado de color carmelita claro, con olor a fruta madura de tamarindo y con un sabor ligeramente ácido.
La tabla 2 presenta la matriz de datos obtenida, durante la evaluación del diseño experimental.
La figura 1 presenta el efecto de las cantidades de los excipientes de la formulación, sobre las propiedades del granulado.
ÍNDICE DE COMPRESIBILIDAD E ÍNDICE DE HAUSNER
El índice de compresibilidad (Fig. 1) (A), tuvo tendencia a aumentar cuando se incrementó la cantidad de lactosa monohidratada en la formulación. Sin embargo, se afectó poco al aumentar la cantidad de almidón de maíz, con una ligera tendencia a disminuir. Cuando la cantidad de Aerosil® aumentó en la formulación, disminuyó notablemente el índice de compresibilidad. Esta variable se ajustó a un modelo cuadrático (ecuación 1), con magnífico valor de R2 ajustado, pero sin capacidad de predicción.
]]>
VELOCIDAD DE FLUJO Y ÁNGULO DE REPOSO
En la figura 1 (C) puede observarse que la cantidad de lactosa monohidratada en la formulación, prácticamente no alteró la fluidez del granulado. Por el contrario, el Aerosil® y el almidón de maíz, cuando están en el nivel máximo de adición, aumentan la fluidez del granulado. Del mismo modo, en la figura 1 (D) puede observarse que la lactosa monohidratada tuvo una discreta influencia en la variabilidad del ángulo de reposo. No obstante, se observó una tendencia a aumentar este, cuando aumentó la cantidad de lactosa en la formulación. Se observó que al aumentar las cantidades de Aerosil® y de almidón de maíz en la formulación, el ángulo de reposo disminuyó.
La raíz cuadrada de la velocidad de flujo se ajustó a un modelo cuadrático, con buena relación entre la bondad de ajuste (R2 -Aj) y la bondad de predicción (R2predicho) y un bajo valor de PRESS (ecuación 2).
El modelo ajustado para el ángulo de reposo presentó mejores estadísticos que el de la velocidad de flujo (ecuación 3)
HUMEDAD RESIDUAL Y TAMAÑO DE PARTÍCULAS
La humedad residual (Fig. 1) (E) no se modificó apreciablemente al variar la cantidad de lactosa monohidratada en la formulación. No se observó lo mismo con el almidón de maíz y el Aerosil®. En estos se observó que, al incrementar las cantidades de ambos excipientes, aumentaron los valores de humedad residual en el granulado. Se observó menor humedad residual en las corridas 1 y 8 (4.23 % y 4,27 %, respectivamente), una es réplica de la otra. La ecuación 4 presenta el modelo ajustado que describe esta variable.
En la figura 1 (F) se muestra la influencia de los excipientes en la variabilidad del tamaño de partícula de los granulados. Se observó que al incrementar la cantidad de lactosa monohidratada en el granulado, el tamaño de las partículas aumentó. El efecto contrario se observó, al aumentar las cantidades de Aerosil® y almidón de maíz en la formulación.
Al evaluar la influencia del tamaño de partícula sobre las propiedades de flujo de los granulados (tabla 2), se observó que las formulaciones que presentaron mayor tamaño de partículas, fueron las que presentaron menor fluidez. Esta variable no se ajustó a modelo alguno.
]]>Se seleccionó, para envasar en las cápsulas, la formulación preparada en la corrida número 1, que se corresponde con las cantidades siguientes: lactosa monohidratada 35,0 g; almidón de maíz 7,5 g y Aerosil® 3,0 g.
La tabla 3 presenta los resultados de la evaluación de la calidad del granulado seleccionado para ser envasado en las cápsulas.
La figura 2 presenta una microfotografía del granulado seleccionado.
SELECCIÓN DEL TAMAÑO Y EVALUACIÓN DE LA CALIDAD DE LAS CÁPSULAS DURAS
Se obtuvieron cápsulas duras con un peso promedio de 601 ± 1,53 mg, tiempo de desintegración de 133 ± 11,32 s y un contenido de polifenoles de 1,48 %.
DISCUSIÓN
Todos los parámetros evaluados al extracto blando de tamarindo se encontraron dentro de los límites establecidos para el extracto blando estandarizado.6
Los resultados observados para el IC y el IH, así como para la velocidad de flujo y el ángulo de reposo se corresponden con lo informado sobre del comportamiento de estos excipientes en formulaciones de granulados.8,13 Con la adición de almidón de maíz y de Aerosil® a la formulación, y sobre todo de este último, se logra la formación de un grano más esférico, que hace que disminuya el rozamiento y la adhesividad, lo que mejora la fluidez y la compresibilidad.
El aumento de la cantidad de Aerosil® (partículas pequeñas) en la formulación, hace que al unirse con el extracto blando, se tiendan a rellenar las irregularidades que se forman en el grano, lo que lo hace más esférico (Fig. 2). Por otro lado, un mayor contenido de almidón de maíz, hace que el grano sea más duro y esto, conjugado con una distribución normal del tamaño de partícula (Estadístico de Kolmogorov-Smirnov= 0,1574; p valor= 0,9273), permiten que el granulado fluya y se acomode mejor por su propio peso.7,8
Al realizar examinar los granos al microscopio óptico (Fig. 2), se observaron unas partículas traslúcidas, adheridas a la superficie exterior del grano, que se corresponden con el Aerosil®. Esto, sin duda, favorece la fluidez de los granos.
La humedad residual tiene gran influencia sobre las propiedades reológicas de los polvos y granulados. La naturaleza química del almidón de maíz y del Aerosil® (dióxido de silicio coloidal), les confiere la capacidad de retener humedad. Por eso, al aumentar la cantidad de estos excipientes en la formulación, tiende a aumentar la humedad residual (Fig. 1) (E). La significación estadística y la magnitud de los coeficientes del almidón de maíz, del Aerosil® y de la interacción entre ambos, en el modelo cuadrático ajustado (ecuación 4), evidencian la influencia de estos excipientes sobre la humedad residual del granulado.
El modelo cuadrático obtenido para la humedad residual presentó excelente bondad de ajuste y una magnífica bondad de predicción, con un valor de PRESS muy pequeño (ecuación 4).
]]> Las formulaciones que presentaron mayor tamaño de partículas, fueron las que mostraron menor fluidez, probablemente, porque estas contienen mayor cantidad de lactosa monohidratada y menores cantidades de Aerosi®l y almidón.Cuando se formulan cápsulas duras, es muy importante tener en cuenta el contenido de humedad de los materiales que se pretenden encapsular. La humedad residual es un factor crítico, pues si es alta, puede humedecer la gelatina y afectar la estabilidad de la forma terminada. En este trabajo se seleccionó la formulación de la corrida número 1, para envasarse en las cápsulas pues, además de poseer buenas propiedades de flujo y compresibilidad, presentó el menor valor de humedad residual.
Al evaluar la calidad de los tres lotes de granulados que se prepararon utilizando la formulación seleccionada, para realizar su caracterización física mecánica y química, se obtuvieron valores muy cercanos en todas las variables. En ninguno de los lotes, ni en ninguna de las características evaluadas, se encontraron diferencias estadísticas significativas entre las medias, con p valores de la prueba F> 0,05 (data no reportada).
Las cápsulas duras obtenidas, mostraron buenas propiedades tecnológicas, que cumplen con las regulaciones internacionales y pudieran ser elaboradas en farmacias dispensariales y en los centros de producción local.
REFERENCIAS BIBLIOGRÁFICAS
1. Sharapin N. Fundamentos de tecnología de productos fitoterapéuticos. Santa Fe de Bogotá: Secretaría Ejecutiva Convenio Andrés Bello; 2000.
2. Roig JT. Plantas Medicinales, Aromáticas y Venenosas de Cuba. La Habana: Ed. Científico-Técnica; 1988. p. 888.
3. Ministerio de Salud Pública. Dirección Provincial de Salud Santiago de Cuba. Informe sobre consumo de medicamentos. La Habana: Ministerio de Salud Pública; 2005.
4. Rodríguez AJR. Evaluación de la actividad antioxidante y hepatoprotectora de una nueva formulación de tabletas, obtenida a partir del extracto blando estandarizado de las hojas de Tamarindus indica L. [tesis doctoral]. La Habana: IFAL, Universidad Médica de La Habana; 2012 [citado 4 Dic 2012]. Disponible en: http://tesis.repo.sld.cu/547/
5. Rodríguez AJR, Lafourcade PA, Escalona JC. Formulación de comprimidos de tamarindo por el método de granulación húmeda. Rev Cubana Farm. 2011;45(3):414-22.
6. Rodríguez AJR, Pérez RR, Escalona AJC, Lafourcade PA, Sierra GG. Standardization of the quality control parameters of the Tamarindus indica L. soft extract. Rev Cubana Plant Med. 2012:17(1):108-14.
7. United States Pharmacopeia. USP 30. United States Pharmacopeia Convention. Rockville: Mack Printing; 2007.
8. Lieberman H, Lachman L. Pharmaceutical Dosage Forms. Tablets. (II). New York: Marcel Dekker; 1981.
9. Iraizoz A, Bilbao RO, Barrios MA. Conferencias de Tecnología Farmacéutica II. La Habana: IFAL, Universidad de La Habana; 1992.
10. Corcoran TE, Hitron R, Humphreys W, Chigier N. Optical measurement of nebulizer sprays: a quantitative comparison of diffraction, phase Doppler interferometry and time of flight techniques. J Aerosol Sci. 2000;31:35-50.
11. Smith W, Murdande S. Nanosizing for improving the delivery of drugs with poor solubility. Pharm Res. 2006;22(4):225-9.
12. Rodríguez AJR, Lafourcade-Prada A, Escalona AJC, Iraizoz CA. Preformulación de tabletas de Tamarindus indica L. Rev Cubana Farm 2011;45(4):553-62.
13. Rowe RC. Handbook of Pharmaceutical Excipient. New York: Pharmaceutical Press & American Pharmacists Association; 2009. p. 888.
]]>
Recibido: 27 de septiembre de 2013.
Aprobado: 13 de noviembre de 2013.
Jesús Rafael Rodríguez Amado. Facultad de Ciencias Naturales. Universidad de Oriente. Avenida Patricio Lumumba, s/n. Santiago de Cuba, Cuba. Correo electrónico: jimmy@cnt.uo.edu.cu