Actividad in vitro contra Leishmania y permeación en piel humana de liposomas ultradeformables de miltefosina
In vitro activity against Leishmania and human skin permeation of miltefosine ultradeformable liposomes
MSc. Indira Paola Hernandez,I PhD. Jorge Aníbal Martinetti Montanari,II PhD. Patricia Escobar RiveroI
I Centro de Investigación en Enfermedades Tropicales (CINTROP), Escuela de Medicina. Departamento de Ciencias Básicas, Universidad Industrial de Santander. Bucaramanga, Colombia. ]]> II Laboratorio de Biomembranas, GBEyB, IMBICE-CONICET. Universidad Nacional de Quilmes, Bernal. Buenos Aires, Argentina.
RESUMEN
Introducción: los liposomas ultradeformables de miltefosina (LUD-MIL) constituyen una opción para el tratamiento tópico en leishmaniasis cutánea penetrando los estratos de la piel hasta la dermis, sitio donde habita el parásito.
Objetivo: diseñar LUD-MIL y determinar su actividad contra L. (Viannia) panamensis y L. (V.) braziliensis y la permeación en piel humana.
Métodos: los LUD-MIL, liposomas convencionales de fosfatidilcolina (LConv) y LUD-MIL-fluorescente (LUD-MIL-Fluo) fueron preparados por el método de rehidratación de película lipídica. Se caracterizaron fisicoquímicamente y se determinaron: la liberación en membrana semisintéticas, la retención en las capas de la piel y la permeación en piel humana. La citotoxicidad en THP-1 fue determinada por el ensayo colorimétrico de MTT y la actividad en promastigotes y amastigotes intracelulares por recuento microscópico.
Resultados: el tamaño, índice de polidispersión, potencial Z y concentración de fosfolípidos de los LUD-MIL fue de 100,7 nm, 0,147, -12,0 mV y 53,24 mM respectivamente. El flujo de MIL a través de la membrana fue mayor con LUD-MIL que con MIL-libre. El tratamiento con LUD-MIL indujo menor acumulación de la MIL en el estrato corneo y mayor permeación que el tratamiento con MIL libre. Los LUD-MIL y los LConv-MIL mantuvieron la actividad de la MIL en los parásitos y células. Los LUD-MIL fueron más tóxicos para las células que los LConv y la MIL y más activos en amastigotes intracelulares de L. (V.) braziliensis.
Conclusión: los LUD-MIL preparados conservaron la actividad anti-Leishmania de la MIL y permitieron la liberación del compuesto en membranas y piel humana. Ensayos en modelos experimentales de leishmaniasis cutánea para evaluar la actividad de estas formulaciones son urgentes de realizar.
Palabras clave: leishmaniasis cutánea, liposomas ultradeformables, tratamientos tópicos, miltefosina, celdas de difusión de Franz.
Introduction: miltefosine ultradeformable liposomes (MIL-LUD) are an option for the topical treatment of cutaneous leishmaniasis penetrating the skin layers to the dermis where the parasite inhabits.
Objective: to design MIL-LUD and determine their in vitro activity against L. (Viannia) panamensis and L. (V.) braziliensis and to determine human skin permeation.
Methods: MIL-LUD, phosphatidylcholine liposomes (MIL-LConv) and fluorescent MIL-LUD (MIL-LUD-Fluo) were prepared by lipid film rehydration method. They were physicochemically characterized to determine drug release in semisynthetic membrane, retention in skin layers and permeation on human skin membranes. Cytotoxicity in THP-1 was determined by the MTT colorimetric test and activity in promastigotes and intracellular amastigotes by microscopic counting.
Results: the size, the polydispersion index, the Zeta potential and phospholipid content were 100.7 nm, 0.147, -12.0mV and 53.24mM, respectively for MIL-LUD. MIL flow through the semisynthetic membrane was greater with MIL-LUD than MIL-free treatment. MIL-LUD treatment induced lower MIL accumulation in the stratum corneum and increased permeation than MIL free treatment. The MIL-LUD and MIL-Conv maintained MIL activity in parasites and cells. The MIL-LUD was more toxic to cells than MIL-Conv and more active against intracellular amastigotes of L. (V.) braziliensis.
Conclusion: prepared LUD -MIL retained the anti-leishmanial activity of the MIL and allowed the compound release in human skin and membranes. Testing of experimental cutaneous leishmaniasis models to evaluate the activity of these formulations are urgently needed
Key words: cutaneous leishmaniasis, ultradeformable liposomes, topical treatment, miltefosine, Franz diffusion cells.
INTRODUCCIÓN
]]> La leishmaniasis es un conjunto de enfermedades producidas por diferentes especies de protozoarios del género Leishmania y transmitidos al hombre por la picadura de insectos flebótomos. Está directamente relacionada con la pobreza siendo endémica en 98 países y territorios.1-2 Presenta diferentes formas clínicas: visceral, cutánea, mucocutánea, siendo la leishmaniasis cutánea (LC) la más común resultante de la infección de los macrófagos de la dermis. Se calcula que anualmente se producen entre 0,7 y 1,3 millones de casos nuevos.1-2El tratamiento se basa en el uso de antimoniales pentavalentes seguido de pentamidina, miltefosina (MIL), anfotericina B (AmB) y paromomicina. Dado los inconvenientes de los tratamientos sistémicos (i.e. reacciones secundarias, falta de eficacia, disponibilidad, costos), los tratamientos locales en forma de cremas o ungüentos, o tratamientos físicos como termoterapia o terapia fotodinàmica constituyen una buena alternativa especialmente en casos tempranos de LC.3
La MIL es un medicamento desarrollado originalmente contra el cáncer con actividad contra protozoarios, bacterias y hongos.4 Su mecanismo de acción se relaciona con su capacidad de perturbar el metabolismo lipídico de la membrana del parásito, inducir mecanismos similares a la apoptosis y modular la respuesta de los macrófagos.5-6 A pesar de los resultados con MIL en leishmaniasis, se reportan efectos teratogénicos y efectos secundarios en el tracto gastrointestinal.7 Igualmente la inducción de cepas resistentes a MIL en condiciones de laboratorio es preocupante8 y se ha demostrado una disminución significativa en su eficacia en ciertas zonas endémicas.9
El uso tópico de la MIL en LC ha sido poco explorado. La formulación de uso tópico Miltex®, utilizada tópicamente en el tratamiento de cáncer, ha sido efectiva en el modelo murino de LC, sin embargo, reactivación de las lesiones en diferentes órganos ha sido observado.10
Los liposomas ultradeformables (LUD) o transferosomas son un tipo de liposomas capaces de alcanzar las capas internas de la piel por debajo del estrato córneo (EC).11 El EC es una barrera impermeable para otros tipos de liposomas que sólo pueden funcionar como vectores de medicamentos permaneciendo en las capas superficiales epidérmicas. La adición de un surfactante de membrana en una determinada proporción respecto del lípido matricial principal, permite a la matriz adquirir ultradeformabilidad.11 Así, se logran vesículas capaces de atravesar poros 10 veces menores, manteniendo su estructura y reteniendo su contenido interno. Una vez atravesado el EC, los LUD son reconocidos y endocitados como sistemas particulados por macrófagos cutáneos accediendo al fagolisosoma, sitio en donde anida el parásito.
El objetivo de este trabajo fue diseñar LUD de MIL y determinar su actividad anti-Leishmania contra L. (V.) panamensis y L. (V.) braziliensis in vitro. Igualmente se determinó la liberación en membranas semisintéticas de aceticelulosa y la permeación en piel humana.
MÉTODOS
Compuestos, preparación y caracterización de liposomas
Prueba de la liberación de MIL en membrana sintética
La liberación de MIL de los LUD-MIL-Fluo se evaluó utilizando las celdas de Franz y membranas semisintéticas de acetil-celulosa. Se colocaron 100 µg/mL de LUD-MIL-Fluo y la MIL-Fluo libre en un volumen de 300 µL de Tris-HCL, pH 7,4, en la cámara donadora. El medio receptor (buffer fosfato salino, PBS, pH 7.2) se mantuvo a 33 °C. Se extrajeron 300 µL del medio receptor a las 0, 2, 4, 8 y 12 horas. El flujo de medicamento se expresó en µg/cm2 teniendo en cuenta la masa de la MIL cuantificada sobre el área de la celda (0,1963 cm2). La MIL-Fluo se cuantificó por espectrofluorimetría (l Ex-Em: 529-539 nm). La concentración de MIL-Fluo se determinó teniendo en cuenta una curva de calibración en etanol. Cada muestra se evaluó por triplicado en dos experimentos.
Ensayos de permeación y retención en piel (Experimentos ex vivo)
Fueron realizados en celdas de Franz utilizando piel humana como membrana.16 La piel utilizada fue obtenida de mujeres sanas que se sometieron a cirugía estética y que no presentaban enfermedades dermatológicas. La piel fue lavada, el tejido graso removido y la piel fue almacenada a -20 °C hasta su uso. Se utilizó el mismo procedimiento descrito anteriormente en el ensayo de liberación. La retención de MIL en estrato córneo fue determinada por el método de cinta adhesiva. Quince (15) cortes de cinta pegante fueron adheridos a la piel que estuvo en contacto con las formulaciones. La MIL de cada cinta se extrajo con etanol y se cuantificó por espectrofluorimetría. Para determinar la retención en epidermis y dermis (E+D) se maceró el fragmento y se adicionó etanol. Los resultados fueron expresados en ng/cm2 de MIL.
Parásitos y células de mamífero
Los promastigotes de L. (V.) panamensis (MHOM/PA/71/LS94) y L. (V.) braziliensis (MHOM/BR/75/M2903) fueron cultivados en medio Schneider suplementado con 10 % de suero bovino fetal inactivado con calor a 28 °C. Los amastigotes intracelulares de Leishmania fueron obtenidos infectando células THP-1 (ATCC TIB-202), previamente transformadas a su fenotipo adherente con forbol miristato acetado (40 ng/mL) por 72 horas, con promastigotes en una proporción parásito: célula de 5:1 por 48 horas a 33 °C.
]]>Las células THP-1 se trataron con diluciones seriadas de las formulaciones por 72 horas. Células controles se mantuvieron sin tratamiento. La toxicidad se determinó por el método de MTT. La densidad óptica se determinó por espectrofotometría a 580 nm y el porcentaje de citotoxicidad fue calculado mediante la fórmula: % citotoxicidad =100 * (DO grupo control-DO grupo tratado)/ DO grupo control. La actividad de las formulaciones se expresó como la concentración citotóxica para 50 % de las células (CC50).
Ensayos de actividad en parásitos
Los promastigotes (5 x 105 parásitos/mL) de L. (V) panamensis o L. (V) braziliensis en fase exponencial de crecimiento fueron tratados con diluciones seriadas 1:3 de las formulaciones disueltas en medio de cultivo, a concentraciones entre 3,7-100 μg/mL por 72 horas a 28 °C. Los parásitos control (control de crecimiento) fueron mantenidos en medio de cultivo sin la formulación. La inhibición del crecimiento de los parásitos fue determinada microscópicamente por conteo directo de parásitos vivos en cámara de Neubauer utilizando eosina amarilla al 0,25 %.17
Los amastigotes intracelulares de los parásitos fueron tratados con diluciones 1:3 de las formulaciones a concentraciones entre 3,7-100 µg/mL por 120 horas a 33 °C. Los porcentajes de infección fueron determinados por conteo microscópico de células infectadas y no infectadas en preparaciones fijadas con metanol y coloreadas con Giemsa. Como controles de crecimiento, los parásitos se mantuvieron sin compuesto. La actividad se determinó por recuento microscópico. Los resultados se expresaron como % de inhibición del crecimiento del parásito y la actividad del compuesto como la concentración que inhibe el 50 % (CI50) parásitos.17
Análisis estadístico
Se utilizó la t de Student, el análisis de varianza (ANOVA) de una vía, y el test de Bonferroni para hallar diferencias significantes entre los subgrupos. Se utilizó el software estadístico Graphpad Prism version 5.0 (GraphPad Software, Inc, La Jolla, USA). Valores de p< 0,05 fueron considerados estadísticamente significativos. El Índice de Selectividad se calculó dividiendo la CC50 obtenida en células THP-1 sobre las CI50 obtenidas en los parásitos. Formulaciones con IS mayores a 3 fueron consideradas como selectivas para los parásitos.17
]]>RESULTADOS
Caracterización de los liposomas
Los resultados de la caracterización fisicoquímica de los liposomas se muestran en la tabla. La relación medicamento: lípido fue de 4,15 mg/g tanto para los LUD-MIL como para los LConv. Los LUD-MIL fueron tan flexibles como los LUD vacíos en términos de ultradeformabilidad. Los perfiles termotrópicos de los LUD-MIL y LUD vacios muestran un pico endotérmico (Tm,) de -22,84 °C y -22,73 °C y una ΔHcal de 0,025 J/g y 4,443 J/g respectivamente.
Liberación de MIL en los LUD
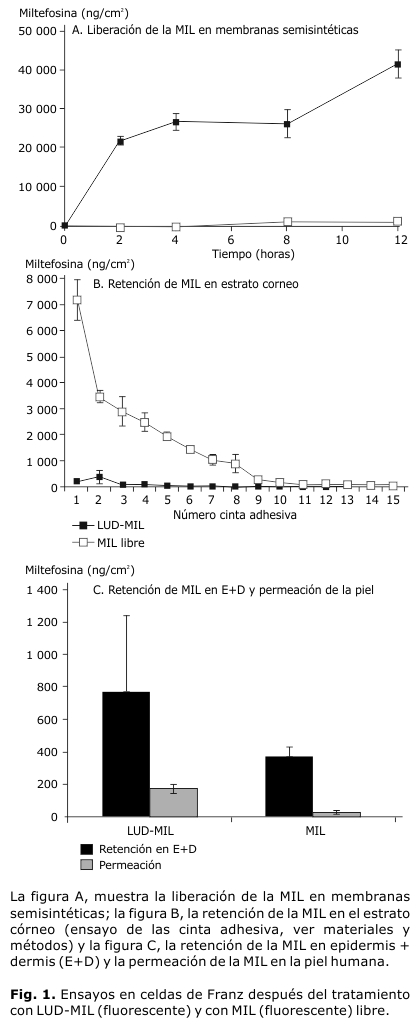
La liberación de la MIL a través de la membrana fue mayor en LUD-MIL (p< 0,05) que en MIL-libre (figura 1A). El flujo de MIL a través de la membrana semisintética fue mayor con LUD-MIL (p< 0,05) que con MIL-libre (10687,0 versus 104,3 ng/cm2 hora respectivamente).
]]> Retención y permeación de la MIL en piel
Tratamiento ex vivo con LUD-MIL indujo significativamente (p< 0,05) una menor retención de la MIL en el estrato córneo (EC) y una mayor permeación en piel que el tratamiento con MIL libre. Después del tratamiento ex vivo con MIL libre, una mayor concentración de MIL libre fue observada en las primeras ocho capas del EC la cual desciende en las posteriores capas (cintas 9-15) (figura 1B). La cantidad de MIL después del tratamiento con MIL libre en el EC fue significativamente mayor (p< 0,05) que la detectada con LUD-MIL con valores de 22143±2851 versus 986±407 ng/cm2. No se observaron diferencias estadísticamente significativas (p< 0,05) en la retención de la MIL en E+D después de ambos tratamientos con valores de 776,6±462 ng/cm2 y de 373,9±55 ng/cm2 para tratamiento con LUD-MIL y MIL libre respectivamente (figura 1C). El tratamiento con LUD-MIL indujo una mayor permeación de MIL que el tratamiento con MIL libre (p< 0,05) con valores de 179±28 y 33,6± 9,9 ng/cm2 respectivamente (figura 1C).
Citotoxicidad de los LUD y LConv vacíos (Vehículos)
Los LUD vacíos fueron más tóxicos para las células THP-1 que los LConv (p< 0,05) mostrando una CC50 entre 0,52±0,01-1,04±0,16 mM de fosfólipidos. Los LConv a la máxima concentración de fosfolípidos evaluada de 10 mM presentaron menos del 25 % de citotoxicidad.
Citotoxicidad de los liposomas con MIL
Los LUD-MIL fueron más tóxicos para las células THP-1 que los LConv-MIL y la MIL libre (p< 0,05) (figura 2). Teniendo en cuenta tanto la concentración de MIL presente en los liposomas como la concentración de fosfolípidos presentes en la membrana de los liposomas, la actividad de los LUD-MIL contra las células THP-1 fue entre CC50 de 5,65±0,15-7,19±0,29 µM de MIL y entre CC50 de 0,11-0,12 mM de fosfolípidos. Las actividades de los LConv-MIL estuvieron en el rango de CC50 9,71±0,05 y 13,33±0,48 µM de MIL y CC50 0,19-0,26 mM de fosfolípidos. La actividad de la MIL libre mostró valores entre CC50 14,06±1,60 -19,74±1,16 µM. (figura 2)
Actividad de los liposomas y la MIL libre en promastigotes
]]> En promastigotes de L. (V.) panamensis el rango de actividades de la MIL incorporada en las diferentes formulaciones fue: LUD-MIL entre CI 50 19,65±0,37 a >20 µM, LConv entre 17,23±0,88 a >20 µM. La actividad de la MIL libre estuvo entre CI50. 11,30±2,74 y 15,70±1,52 µM.En L. (V.) braziliensis fue: LUD-MIL entre CI50 19,6±0,73 a >20 µM, LConv entre CI50 19,16±0,52 a >20 µM. La actividad de la MIL libre estuvo entre 11,73±0,27 y 13,75 µM. Los IS para los LUD-MIL y LConv en ambos parásitos fueron menores a 1. Los IS de la MIL fueron de 1,4. En concentraciones de 20 µM, la MIL libre fue significativamente más activa para los promastigotes de ambos parásitos que los LUD-MIL y LConv-MIL (figura 3). Para todos los casos la concentración de fosfolípidos de los LUD-MIL y LConv-MIL fue menor a 0,03 mM (figura 3)
Actividad de los liposomas y la MIL libre en amastigotes intracelulares
Los LUD-MIL y los LConv-MIL fueron más activos para amastigotes intracelulares de L. (V.) braziliensis que para L. (V.) panamensis. En amastigotes intracelulares de L. (V.) panamensis el rango de actividades de la MIL en las diferentes formulaciones fue: LUD-MIL entre CI 50 13,26±0,46 y 13,63±1,44, LConv entre CI5010,66±0,75 y 18,17±0,70 y MIL libre entre CI50. 12,94±0,80 y 14,10±0,59 µM. En L. (V.) braziliensis fue: LUD-MIL entre CI50 1,28±0,21 y 1,29±0,03, LConv entre CI501,53±0,20 y 2,07±0,02 y MIL libre entre 2,85±0,30 y 10,25±0,49 µM. Los IS para los LUD-MIL y LConv en amastigotes intracelulares de L. (V.) panamensis fueron menores a 1, sin embargo los IS en amastigotes de L. (V.) braziliensis estuvieron en el rango de 4-6. Los IS de la MIL libre fueron de 1-2. Los LUD-MIL y los LConv-MIL presentaron actividades similares, sin embargo ambos fueron más activos para L. (V.) braziliensis que para L. (V.) panamensis. (figura 4).
DISCUSIÓN
Los liposomas ultradeformables (LUD o transferosomas) son vesículas lipídicas elásticas o deformables debido a la incorporación de fosfatidilcolina al colato de sodio (NaChol) en su membrana, que sirven como sistemas de liberación tópica y transdermica de medicamentos incluidos estos ya sea en la fase acuosa interna o integrados en su fase lipídica.18 Por sus características fisicoquímicas constituyen un sistema excelente para el transporte a través de piel en LC ya que pueden atravesar el estrato corneo de la piel y ser endocitados por los macrófagos, célula hospedera de la Leishmania.13 La mayoría de trabajos donde se proponen formulaciones liposomales en leishmaniasis están orientados al modelo de LV, siendo la anfotericina B (AmB) liposomal (AmBisome) aplicada parenteralmente el mayor éxito.19 En este caso, la AmB se encuentra encapsulada en liposomas unilaminales de <100 nm constituidos por colesterol y otros fosfolípidos. Su uso y eficiencia en LC se encuentra en estudio. Recientemente pacientes con LC mostraron un 84 % de cura al tratamiento con Ambisome aplicado i.v., sin embargo los autores sugieren que el costo, la toxicidad media que se presenta y la falta de un protocolo óptimo de dosificación podría limitar su uso en LC.20
En este trabajo se diseñaron LUD-MIL como candidatos para ser utilizados en el tratamiento tópico de la LC. La incorporación de MIL no afectó la formación de los liposomas ni su estabilidad, tal como surge de los experimentos de dispersión de luz dinámica, en la que la presencia del activo no tuvo influencia significativa en el tamaño de las vesículas obtenidas en el proceso, ni se observó un aumento mayor en el tamaño promedio en el tiempo comparado con el control sin MIL. Respecto del potencial Z el módulo del mismo disminuyó levemente en los liposomas conteniendo MIL, pero los valores se mantuvieron dentro de los parámetros de estabilidad media. La calorimetría diferencial de barrido evidenció la asociación a la membrana liposomal de la MIL,14 la cual podría hallarse en la región hidrófoba interna de la membrana. Su presencia, sin embargo, no afectó la ultradeformabilidad, que depende de la presencia del colato de sodio en la membrana actuando como activador de borde.11 Se observó una caída abrupta en el ΔHcal en los LUD-MIL la cual podría deberse a la presencia de MIL en la bicapa, alterando su organización y cooperatividad.21
La captación de material particulado por parte de los macrófagos cutáneos podría permitir la llegada de MIL al mismo compartimiento intracelular donde anidan los parásitos, en vesículas de endocitosis topológicamente externas al citosol celular. Esta posibilidad de direccionamiento, a expensas del diseño del transportador con un tamaño adecuado -una población liposomal monomodal del orden de los 100 nm y con baja polidispersión como se obtuvo en este caso-, podría ser clave para obtener mayores efectos tóxicos para el parásito, utilizándose una vía no invasiva como lo es la tópica incluso con menores dosis,22 y reduciendo “los efectos colaterales”.
]]> La MIL incorporada en LUD o LConv no perdió su actividad anti-Leishmania. El tratamiento con LUD-MIL demostró ser capaz de inhibir el crecimiento de los promastigotes y amastigotes intracelulares de ambas especies de Leishmania con algunas diferencias con respecto a la MIL libre y a la especie de parásito. La actividad no dependió de la fosfatidilcolina o del colato de sodio presentes en los liposomas ya que la concentración final de fosfolípidos fue inactiva para los parásitos. Esto fue siempre una variable manejada en el trabajo ya que se tienen reportes de liposomas vacios de fosfatidilcolina de huevo (PC) y estearilamina (SA) cargados positivamente que fueron activos contra promastigotes y amastigotes intracelulares (IC50 13μg/mL) y en el modelo experimental de L. donovani.23 Aunque liposomas controles de PC (que sería equivalente a los LConv) no mostraron actividad antiparasitaria.23En el presente trabajo reportamos que los LUD-vacíos fueron más tóxicos que los LConv en las células THP-1; este efecto había sido observado anteriormente en promastigotes de Leishmania22 pero no en las células hospedera THP-1; la toxicidad en los LUD-vacíos podría estar relacionada posiblemente por la presencia del NaChol el cual actúa como surfactante y proporciona la deformabilidad de la vesicula liposomal. Debido a sus propiedades el NaChol ha sido evaluado con diversos compuestos para aumentar la permeabilidad a través de la membrana celular,24 el efecto citotóxico del NaChol también ha sido evaluado en diferentes modelos;25,26 de acuerdo con los diferentes reportes, su efecto puede variar según la concentración, el tiempo de incubación y el tipo de células utilizadas en cada experimento, así por ejemplo, se ha observado que el NaChol no tuvo efecto sobre la morfología de células tumorales de cerebro expuestas a 5 µL de NaChol al 1 % durante 72 horas25 y en otro reporte el NaChol fue tóxico a una CC50 de 3,49 mM en células del epitelio nasal causando efectos reversibles sobre la membrana celular.26 En nuestro caso, células THP-1 expuestas a LUD-vacíos durante 24 horas no produjo toxicidad a concentraciones de fosfolípidos menores a 2,83 mM13 pero si causó toxicidad en células THP-1 expuestas a 72 horas (CC50 entre 0,52±0,0-1,04±0,16 mM). Teniendo en cuenta estos resultados las concentraciones de fosfolípidos utilizadas en LUD-MIL no superó en ninguno de los casos una concentración mayor a 0,5 mM.
Exceptuando en los amastigotes de L. braziliensis, los LUD-MIL (ni los LConv-MIL) no mostraron una mayor selectividad por los parásitos, ni fueron más activos que la MIL libre. La necesidad de diseñar liposomas de MIL surgió principalmente para reducir la toxicidad de la MIL libre presentada al tratamiento de cáncer tales como daño gastrointestinal, pérdida de peso corporal y tromboflebitis al ser aplicada sistémicamente y para aumentar el índice terapéutico. Inyecciones i.v. o por vía oral de formulaciones de MIL en liposomas unilaminales compuestos por colesterol, y fosfatidilglicerol redujeron la toxicidad en ratas con tumor mamario14 y liposomas con una bicapa combinada de MIL, colesterol, polietilenglicol y fosfoetanolamina formaron liposomas estables y fueron más eficaces que liposomas convencionales y MIL libre en la reducciones de tumores debido probablemente a un aumento en el tiempo de circulación de la formulación y a una mayor acumulación en tumores.27 En Leishmania, fueron preparados liposomas de MIL(MIL:PC:SA) sin colesterol y con carga positiva,28 similares a los reportados por Dey 2000,22 si bien fueron 1-2 veces más activos que la MIL libre en promastigotes de L. donovani, fueron inactivos en amastigotes intracelulares.27 Contrariamente, en este trabajo reportamos que los LUD-MIL y LConv-MIL fueron activos en amastigotes intracelulares de L. (V.) panamensis y L. (V.) braziliensis. Diferencias entre los dos tipos de liposomas tales como tamaño (150-222 nm versus 100-104 nm), los componentes (SA versus colato de sodio), en el potencial Z (positivo versus negativo), en los tipos de parásitos utilizados, en las células hospederas (macrófagos peritoneales versus THP-1), tiempos de incubación de los ensayos (48 versus 72 horas) pudieron estar implicadas en estas diferencias.
El perfil de liberación de MIL en celdas de Franz nos permitió conocer la velocidad de liberación del compuesto al tratamiento en su forma libre y liposomal. Así mismo, se pudo evaluar el comportamiento de diferentes variables (tiempo, concentración del compuesto, solución receptora, etc) que posteriormente fueron utilizadas en los estudios de permeación y retención en piel. Los resultados mostraron que la difusión a través de la membrana de acetato de celulosa fue 100 veces mejor con la aplicación de LUD-MIL. Se considera que factores relacionados con el diseño de los liposomas (tamaño, solubilidad, potencial zeta, etc.), pudieron favorecer su paso a través la membrana. Ensayos de liberación realizados con diferentes formulaciones liposomales de ketoconazol sugieren que la cinética de liberación depende primariamente de la composición lipídica y la relación compuesto-lipido,29 en otro trabajo también han mostrado la importancia del vehículo y la formulación utilizada en el porcentaje de liberación de la paromomicina en celdas de Franz.30
Como conclusión podemos decir se pudieron diseñar LUD-MIL que conservaron la actividad anti-Leishmania de la MIL in vitro y permitieron la liberación del compuesto en membranas y piel humana. Ensayos en modelos experimentales de LC para evaluar la actividad de estas formulaciones son urgentes de realizar.
CONFLICTO DE INTERESES
Los autores del presente trabajo declaramos que no existió conflicto de intereses en la realización del trabajo.
AGRADECIMIENTOS
]]> Agradecemos al doctor Ulises Acuña del Instituto de Química Física Rocasolano de Madrid, España, por la donación de la MIL fluorescente. Al profesor Eduardo Ricci de la Universidad Federal de Rio de Janeiro, por su apoyo en la estandarización y el análisis de las pruebas de permeación. Este trabajo fue financiado por el Instituto Colombiano para el Desarrollo de la Ciencia y la Tecnología "Francisco José de Caldas" COLCIENCIAS (cod. 1102-459-21643; RC Nº 481 de 2008) y la Universidad Industrial de Santander.
REFERENCIAS BIBLIOGRÁFICAS
1. Organización Panamericana de la Salud (OPS). Pequeñas picaduras grandes amenazas [Citado 1 de septiembre del 2014]. Disponible en: http://www.paho.org/world-health-day-2014/wp-content/uploads/2014/02/ Leishmaniasis-esp.pdf
2. Alvar J, Vélez ID, Bern C, Herrero M, Desjeux P, Cano J, et al. Leishmaniasis worldwide and global estimates of its incidence. PLoS One. 2012;7(5):e35671.
3. Monge-Maillo B, López-Vélez R. Therapeutic options for old world cutaneous leishmaniasis and new world cutaneous and mucocutaneous leishmaniasis. Drugs. 2013;73(17):1889-920.
4. Dorlo TP, van Thiel PP, Huitema AD, Keizer RJ, de Vries HJ, Beijnen JH, et al. Pharmacokinetics of miltefosine in old world cutaneous leishmaniasis patients. Antimicrob Agents Chemother. 2008;52(8):2855-60.
]]>5. Soto J, Soto P. Oral miltefosine to treat leishmaniasis. Biomedica. 2006;26(Suppl 1):207-17.
6. Vincent IM, Weidt S, Rivas L, Burgess K, Smith TK, Ouellette M. Untargeted metabolomic analysis of miltefosine action in Leishmania infantum reveals changes to the internal lipid metabolism. Int J Parasitol Drugs Drug Resist. 2013;4(1):20-7.
7. Berman J, Bryceson AD, Croft S, Engel J, Gutteridge W, Karbwang J, et al. Miltefosine: issues to be addressed in the future. Trans R Soc Trop Med Hyg. 2006;100(Suppl 1):S41-4.
8. Seifert K, Pérez-Victoria FJ, Stettler M, Sánchez-Cañete MP, Castanys S, Gamarro F, et al. Inactivation of the miltefosine transporter, LdMT, causes miltefosine resistance that is conferred to the amastigote stage of Leishmania donovani and persists in vivo. Int J Antimicrob Agents. 2007;30(3):229-35.
9. Rai K, Cuypers B, Bhattarai NR, Uranw S, Berg M, Ostyn B, et al. Relapse after treatment with miltefosine for visceral leishmaniasis is associated with increased infectivity of the infecting Leishmania donovani strain. MBio. 2013;4(5):e00611-13.
]]>10. Schmidt-Ott R, Klenner T, Overath P, Aebischer T. Topical treatment with hexadecylphosphocholine (Miltex) efficiently reduces parasite burden in experimental cutaneous leishmaniasis. Trans R Soc Trop Med Hyg. 1999;93(1):85-90.
11. Cevc G, Blume G. Lipid vesicles penetrate into intact skin owing to the transdermal osmotic gradients and hydration force. Biochim Biophys Acta. 1992;1104(1):226-32.
12. Hornillos V, Carrillo E, Rivas L, Amat-Guerri F, Acuña AU. Synthesis of BODIPY-labeled alkylphosphocholines with leishmanicidal activity, as fluorescent analogues of miltefosine. Bioorg Med Chem Lett. 2008;18(24):6336-9.
13. Hernández IP, Montanari J, Valdivieso W, Morilla MJ, Romero EL, Escobar P. In vitro phototoxicity of ultradeformable liposomes containing chloroaluminum phthalocyanine against New World Leishmania species. J Photochem Photobiol B. 2012;117:157-63
14. Kaufmann-Kolle P, Berger MR, Unger C, Eibl H. Systemic administration of alkylphosphocholines. Erucylphosphocholine and liposomal hexadecylphosphocholine. Adv Exp Med Biol. 1996;416:165-8.
15. Barlett GR. Phosphorous assay in column chromatography. J. Biol. Chem. 1959;234:466-68.
16. Primo FL, Bentley MV, Tedesco AC. Photophysical studies and in vitro skin permeation/retention of Foscan/nanoemulsion (NE) applicable to photodynamic therapy skin cancer treatment. J Nanosci Nanotechnol. 2008;8(1):340-7.
17. Blanco MC, Escobar P, Leal SM, Bahsas A, Cobo J, Nogueras M, et al. Synthesis of novel polysubstituted (2SR,4RS)-2-heteroaryltetrahydro-1,4-epoxy-1-benzazepines and cis-2-heteroaryl-4-hydroxytetrahydro-1H-1-benzazepines as antiparasitic agents. Eur J Med Chem. 2014;86C:291-309.
18. Benson HA. Transfersomes for transdermal drug delivery. Expert Opin Drug Deliv. 2006;3(6):727-37.
19. Matlashewski G, Arana B, Kroeger A, Battacharya S, Sundar S, Das P, et al. Visceral leishmaniasis: elimination with existing interventions. Lancet Infect Dis. 2011;11(4):322-5.
20. Wortmann G, Zapor M, Ressner R, Fraser S, Hartzell J, Pierson J, et al. Lipsosomal amphotericin B for treatment of cutaneous leishmaniasis. Am J Trop Med Hyg. 2010;83(5):1028-33.
21. Montanari J, Vera M, Mensi E, Morilla M, Romero E. Nanoberries for topical delivery of antioxidants. J Cosmet Sci. 2013;64(6):469-81.
22. Montanari J, Maidana C, Esteva MI, Salomon C, Morilla MJ, Romero EL. Sunlight triggered photodynamic ultradeformable liposomes against Leishmania braziliensis are also leishmanicidal in the dark. Control Release. 2010;147(3):368-76.
23. Dey T, Anam K, Afrin F, Ali N. Antileishmanial activities of stearylamine-bearing liposomes. Antimicrob Agents Chemother. 2000;44(6):1739-42.
24. Yu Q, Wang Z, Li P, Yang Q. The effect of various absorption enhancers on tight junction in the human intestinal Caco-2 cell line. Drug Dev Ind Pharm. 2013; 39(4):587-92.
25. Dong L, Witkowski CM, Craig MM, Greenwade MM, Joseph KL. Cytotoxicity effects of different surfactant molecules conjugated to carbon nanotubes on human astrocytoma cells. Nanoscale Res Lett. 2009;4(12):1517-23.
26. Lin H, Gebhardt M, Bian S, Kwon KA, Shim CK, Chung SJ, et al. Enhancing effect of surfactants on fexofenadine. HCl transport across the human nasal epithelial cell monolayer. Int J Pharm. 2007;330(1-2):23-31.
27. Arndt D, Zeisig R, Eue I, Sternberg B, Fichtner I. Antineoplastic activity of sterically stabilized alkylphosphocholine liposomes in human breast carcinomas. Breast Cancer Res Treat. 1997;43(3):237-46.
28. Papagiannaros A, Bories C, Demetzos C, Loiseau PM. Antileishmanial and trypanocidal activities of new miltefosine liposomal formulations. Biomed Pharmacother. 2005;59(10):545-50.
29. Patel RP, Patel H, Baria AH. Formulation and evaluation of liposomes of ketoconazole. Int J Drug Delivery Tech. 2009;1(1):16-23.
30. Ferreira LS, Ramaldes GA, Nunan EA, Ferreira LA. In vitro skin permeation and retention of paromomycin from liposomes for topical treatment of the cutaneous leishmaniasis. Drug Dev Ind Pharm. 2004;30(3):289-96.
Recibido: 28 de mayo de 2014.
Aprobado: 12 de agosto de 2014.
PhD. Patricia Escobar Rivero . Universidad Industrial de Santander, Km 2 vía al Refugio, Sede UIS Guatiguará. Teléfono/Fax: +57-7 6344000 Ext 3565. Correo electrónico: pescobarwww@yahoo.co.uk
]]>