Episodio de Hipotonía e Hiporreactividad posterior a la aplicación de vacunas en Cuba durante el período 2012-2013
Hypotonic-hyporesponsive episodes after the application of vaccines in Cuba during the period 2012-2013
Dra. Belkys María Galindo Santana,I Téc. Damarys Concepción Díaz,I Dr. Miguel Angel Galindo SardiñaII
I Instituto de Medicina Tropical “Pedro Kourí”. La Habana, Cuba.
II Dirección Nacional de Epidemiología del Ministerio de Salud Pública (MINSAP). La Habana, Cuba.
RESUMEN
Introducción: la vacuna contra la difteria, la tos ferina (células enteras) y el tétanos que protege contra estas enfermedades, inició su uso en la década de 1940, logró una disminución considerable de estas enfermedades. Pero también, surgieron numerosos eventos asociados a esta vacuna. Uno de ellos es el “Episodio de Hipotonía e Hiporreactividad”, reportado con menor frecuencia, a las vacunas contra Haemophilus influenzae tipo b y la hepatitis B. Es un evento poco conocido y raro.
Objetivo: mejorar el conocimiento sobre esta entidad.
Métodos: se realizó un estudio observacional retrospectivo de los Episodio de Hipotonía e Hiporreactividad el (según niveles de certeza diagnóstica), reportados durante 2012 y 2013 por el médico de familia al sistema de vigilancia de eventos adversos, procedentes de todas las provincias.
Resultados: fueron reportados 27 Episodio de Hipotonía e Hiporreactividad. El 92,6 % correspondió a la vacuna pentavalente, para una tasa de 3,2 x 105 Dosis Aplicadas. El 74 % se notificaron en las primeras 12 horas. Se observó con mayor frecuencia después de la primera dosis, para un 48 % y el 85,4 % ocurrió en los menores de 6 meses. La fiebre, el llanto persistente, los vómitos, el decaimiento y la somnolencia fueron los síntomas asociados con esta entidad.
Conclusiones: la vigilancia de este episodio ha permitido conocer el tiempo de aparición después de aplicar la vacuna, dosis, edad y si está asociado con otros síntomas. Constituye un primer acercamiento a este evento, para mejorar su conocimiento, lo cual permitirá continuar con la seguridad y confiabilidad del Programa Nacional de Inmunización en Cuba.
Palabras clave: Vacuna DPTe, Episodio de Hipotonía e Hiporreactividad, sistema de vigilancia de eventos adversos, Atención Primaria de Salud.
ABSTRACT
]]> Introduction: the use of the diphtheria, pertussis (whole cells) and tetanus vaccine started in the forties of the twentieth century considerably reduced theses diseases. Many events associated with this vaccine took place also, however. For example, the hypotonic-hyporesponsive episode, reported less frequently, to the Haemophilus influenzae Type B and hepatitis B vaccines. This is a rare and little known event.Keywords: DPTe vaccine, hypotonic-hyporesponsive episode, surveillance of adverse events, primary health care.
INTRODUCCIÓN
]]> Las vacunas se encuentran entre los productos biológicos más seguros, eficaces y con un costo efectividad más favorable para su uso en seres humanos. Asegurar que las vacunas sean seguras, eficaces y de calidad es un elemento decisivo para su desarrollo y distribución.1-5 La vacunación ha sido considerada uno de los hitos más importantes del siglo XX.Como las vacunas son aplicadas en individuos saludables, con el objetivo de prevenir enfermedades, la expectativa del público y de los profesionales de la salud en cuanto a su seguridad, es mayor que la relativa a los medicamentos de uso terapéutico, sean la ocurrencia de los eventos adversos menos tolerada. Por eso, se considera de especial importancia la vigilancia de los eventos adversos después de la vacunación.6,7 Desde 1999, el Programa Nacional de Inmunización de Cuba (PNI) cuenta con un sistema de vigilancia de eventos adversos a la vacunación (SVEAV). En Cuba, este sistema de vigilancia es pasivo, y se basa en las notificaciones recibidas a través del modelo primario de recolección de datos y realizadas por los médicos de familia que trabajan en los consultorios del país. Excepcional, en el caso de la introducción de nuevas vacunas, como por ejemplo con la aplicación de la vacuna Pandemrix en el 2010, el sistema se comportó como un sistema de vigilancia activo.4
La vacuna que protege contra la difteria, la tosferina y el tétanos (DPTe) (vacuna de células enteras), comenzó a aplicarse en la década de 1940, obtiene un descenso importante en la incidencia de esta patología, pero, a su vez, surgieron numerosos eventos adversos asociados a la misma. El componente pertussis es en gran parte, el responsable de las reacciones que ocurren después de la administración de esta vacuna.8-10
Uno de los efectos secundarios asociados a esta vacuna, es el denominado “Episodio de Hipotonía e Hiporreactividad” (EHH) caracterizados por la pérdida súbita del tono muscular asociada a una escasa respuesta a los estímulos y palidez cutánea o cianosis. Este episodio también ha sido reportado pero con menor frecuencia para las vacunas contra Haemophilus influenzae tipo b y el virus de la hepatitis B.11,12
Aún no se conoce, si esto se debe a la corta edad de los vacunados o si se trata de un verdadero efecto inmunológico (o la combinación de ambos efectos). Se desconoce también la patogenia del EHH. Se piensa que en esto influyan tal vez, múltiples, factores, tanto idiosincrásicos del niño como inherentes en la vacuna. La completa recuperación del paciente puede ocurrir en menos de 24 h, sin dejar secuelas, sólo con la administración de oxigenoterapia el cuadro puede ser resuelto. El EEH es de difícil caracterización clínica, entre otras razones por su ocurrencia fugaz, dificulta la evaluación por un profesional capacitado y también por la posible confusión con manifestaciones clínicas de otras enfermedades. La diversidad de términos (“choque”, “síndrome semejante al choque, “colapso”) y de definiciones de caso usados, perjudica la interpretación y la comparación de datos relativos a la ocurrencia, la fisiopatología y las consecuencias de EHH.11 El pronóstico es bueno. Es importante que el médico de la familia, pediatras e intensivistas conozcan bien la definición de caso clínico establecida, y sean capaces de integrar los síntomas y signos que se puedan presentar, para detectar oportunamente esta entidad.
Es importante la existencia de una definición de caso global aceptada. El Centro Estatal de Control de la Calidad de los Medicamentos, Equipos y Dispositivos Médicos trabajan trabajando desde hace 5 años en algunas definiciones de casos establecidas por la Brighton Collaboration.11-16 Este trabajo constituye el primer esfuerzo estructurado para elaborar un consenso internacional sobre un “lenguaje común” necesario para una comprensión científica e adicional de la seguridad de las vacunas. Las normas para recoger, analizar y presentar datos de seguridad, facilitan compartir y comparar los datos de vacunas de diferentes procedencias geográficas entre profesionales de seguridad de las vacunas de todo el mundo.
Exceptuando la tríada de síntomas clínicos, no existen investigaciones adicionales (como exámenes de laboratorio) que permitan confirmar el diagnóstico de EHH. Por tratarse de un evento poco conocido y raro en Cuba, asociado con la administración de las vacunas citadas antes, con una definición nueva, con la que se trabaja hace unos años en la Atención Primaria de Salud, con una mejor familiarización del concepto de esta entidad por parte de nuestros profesionales de la salud, se considera de gran importancia abordar esta temática y presentar los EHH reportados en 2012 y 2013.
MÉTODOS
Se realizó un estudio observacional retrospectivo, para describir el Episodio de Hipotonía e Hiporreactividad, (según niveles de certeza diagnóstica), reportados al sistema de vigilancia de eventos adversos por el médico de familia en el modelo primario de recolección de datos (procedentes de todas las provincias, desde el 1ro de enero de 2012, hasta el 31 de diciembre de 2013. En el Instituto Pedro Kourí se realizó la gestión de la base de datos, el análisis y la emisión de los resultados.
]]> La definición de EHH, utilizada para notificar los casos, es la que se describe a continuación propuesta por la Brighton Collaboration.Para el caso específico del Episodio de Hipotonía Hiporresponsiva, la Brighton Collaboration plantea 3 niveles de certeza diagnóstica:11,12
Nivel 1: Inicio súbito de:
• Hipotonía muscular e.
• Hiporrespuesta (disminución o ausencia de respuesta) y.
• Palidez o cianosis.
Nivel 2: Inicio súbito de:
]]> • Hiporrespuesta (disminución o ausencia de respuesta) y.• Palidez o cianosis y.
• Tono muscular desconocido ó.
• Hipotonía muscular y.
• Hiporrespuesta (disminución o ausencia de respuesta) y.
• Color de piel desconocido.
Nivel 3: Inicio súbito de:
• Hiporrespuesta (disminución o ausencia de respuesta) y.
• Palidez o cianosis y.
]]> • Tono muscular normal ó.• Hipotonía muscular y.
• Palidez o cianosis y.
• Nivel de conciencia desconocido.
Para los casos que no cumplan con los niveles de certeza diagnóstica la Brighton Collaboration establece dos categorías adicionales:11,12
Nivel 4. Evento de EHH notificado que no reúne pruebas suficientes para cumplir la definición de caso.
Nivel 5. No, no es un caso de EHH
Las variables examinadas incluyen tipo de vacuna, sexo, intervalo entre la aplicación de la vacuna y la aparición del evento adverso, edad del paciente, dosis que provocaron el evento y síntomas asociados al EHH.
La fuente primaria de obtención de la información fueron las notificaciones del médico de la familia recogidas a través del modelo primario de recolección de datos (MPRD), los cuales se introdujeron en la base de datos creada en Excel en todas las provincias del país y se enviaron al Instituto “Pedro Kourí”, entidad encargada del proceso de gestión de la base de datos, análisis y emisión de los resultados. Como se establece por el PNI, todos los vacunados deben permanecer 1 h en observación.
Para el análisis de los datos se emplearon frecuencias absolutas, frecuencias relativas (porcentajes) y tasas (generales y específicas). La tasa de eventos adversos se calculó por 100 000 dosis aplicadas (DA) y por años. Los datos se organizaron en tablas y figuras para su análisis.
]]>RESULTADOS
Durante los dos años de estudio, fueron reportados al sistema de vigilancia de eventos adversos a la vacunación, 27 EHH, 6 en el año 2012 y 21 en el año 2013.
El 92,6 % (25) de los EHH, fueron posteriores o estuvieron relacionados con a la vacuna pentavalente (DPT+HB+Hib) para una tasa de 3,2 x 100 000 DA. La tasa general por las tres vacunas fue de 0,7 x 100 000 DA.
Asociados a la DPT, la frecuencia fue de 1/30 992 dosis aplicadas.
Se reportó 1 caso de EHH para la vacuna de toxoide tetánico y uno para la vacuna duple bacteriana, para un 3,7 % para cada una, como se puede observar en la tabla 1.
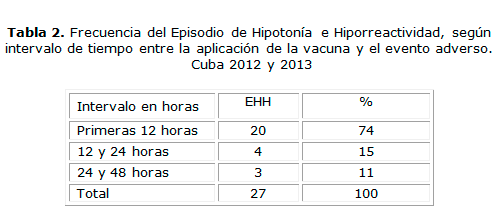
La tabla 2, mostró que el 74 % de EHH se reportó en las primeras 12 h (entre la aplicación de la vacuna y la aparición de este cuadro). 4 casos (15 %) se detectaron entre las 12 y 24 h y en 3 casos (11 %) entre 24 y 48 h.
Según la edad, en el menor de 6 meses se observó con mayor frecuencia (85,4 %) el EHH, seguido del grupo de 7-12 meses y del mayor de 12 meses. (Fig. 1).
]]> La mayor frecuencia de aparición del EHH, ocurrió después de la primera dosis, para un 48,0 %. La ocurrencia de este evento se comportó de manera similar para la segunda y tercera dosis (6 para un 22,0 % en cada una, pero inferior a la primera dosis) (Fig. 2).El 51,8 % de los casos con EHH, correspondió al sexo femenino y el 48,2 % al masculino (datos no mostrados).
La fiebre, el llanto persistente, los vómitos, el decaimiento y la somnolencia fueron los síntomas asociados al EHH, para un 74,0 %. (33,3 %, 14,8 %, 11,1 %, 11, 1 % y 3,7 % en orden). El 26 % de los cuadros de EHH, no reunía pruebas suficientes para incluirse dentro de los tres primeros niveles de certeza diagnóstica, por lo que para este tipo de casos se establecieron dos categorías adicionales, y fueron incluidos en el nivel 4 (tabla 3).
El 33,3 % de los casos de EHH reportaron fiebre. En 4 (14,8 %) de los casos con se reportó el llanto persistente. Los vómitos y el decaimiento se reportaron en 6 casos (3 cada uno), para un 22,2 %.
Siete de los casos, no cumplieron con los 3 primeros niveles de certeza diagnóstica, por lo cual se enmarcaron en una las dos categorías adicionales, específicamente en el nivel 4, que es aquel EHH notificado que no reúne pruebas suficientes para cumplir la definición de caso.
DISCUSIÓN
El EHH se describió por primera vez hace más de tres décadas. Constituye un fenómeno infrecuente, fugaz y muchas veces no presenciado por profesionales de la salud. Ocurre en lo fundamental en niños pequeños. Su diagnóstico es por lo general, retrospectivo a partir de señales descritas por los padres del niño y se basa en la descripción clínica y no, en investigaciones laboratoriales u otras. Es de corta duración, no deja secuelas, de naturaleza benigna, con buena recuperación.17-19
Puede existir confusión con otras manifestaciones clínicas de otras enfermedades.
]]> Ante un EHH se debe realizar el diagnóstico diferencial principal como:•Síncope vasovagal: se caracteriza por la misma tríada de síntomas pero este por lo general se presenta en grupos de edades mayores.9,20
•Convulsión atónica de breve duración: cuadro clínico similar, se caracteriza por la pérdida de conciencia, pérdida del tono de los músculos posturales con frecuencia precedida de una sacudida mioclónica y precipitada por hiperventilación, no alteraciones en cuanto a la coloración de la piel. Se presentan en niños entre 3 meses y 6 años de edad. Es típico asociado a la vacuna DPTe que se aplica en países subdesarrollados por el elevado costo de la DPTa (su ocurrencia en el país contraindica a las dosis siguientes, por lo que en las dosis siguientes se aplica la vacuna DT.9,20
Según reportes internacionales de casos de EHH después de la aplicación de vacuna DPT acelular y DT, aunque la frecuencia de estos eventos en estas circunstancias ha sido menor.
La casuística, mostró que la mayoría de los EHH notificados, ocurrieron después de la aplicación de la vacuna pentavalente (con componente pertussis de células enteras), para una tasa de 3,2 x 100 000 DA. Estudios internacionales, muestran una tasa de incidencia notificada por cada 100.000 dosis aplicadas, observándose con mayor frecuencia, tras la administración de vacunas antitosferínicas celulares, oscila entre 36 a 250 episodios. Con relación a las vacunas antitosferínicas acelulares, varía entre 4 a 140 episodios. Con mayor frecuencia, se presenta en niños menores de 2 años y asociado a la primera dosis.11,12 La tasa se considera baja para este estudio, comparada con lo realizado por Bonhoeffer.11 Un estudio realizado por Cody, mostró una frecuencia de 1/1 750 vacunados.9
El tiempo transcurrido entre la vacunación y la aparición de los síntomas, se produce de inmediato, hasta 48 h después. En el presente estudio, los síntomas acontecieron con mayor frecuencia en las primeras 12 h. Investigaciones realizadas por Cody,9 DuVernoy,19 Goodwin21 y Gold22 arrojan resultados similares. Se refuerza la observación de Monteiro de la necesidad de observación en las primeras 6 h después de la vacunación.23
El EHH se observa con mayor frecuencia en el menor de 1 año de edad, se tiene en cuenta que a estas edades se aplican gran número de vacunas. Estudios realizados por DuVernoy,19 y Ferreira24 observaron que la mayor frecuencia de este episodio, se observa en este grupo de edad.
Tras la administración de la serie primaria de vacunación y en lo particular tras la primera dosis (tanto para vacunas acelulares, como de células enteras) se observa la mayor frecuencia de EHH. Este resultado concuerda con otras investigaciones realizadas.18,21,25,26 No existe explicación para ello, aunque se plantea que deben influir las características de la vacuna y también fenómenos inmunitarios intrínsecos. En un estudio de Monteiro, la mayoría de los casos de EHH ocurrieron después de la tercera dosis.23 Lemos observó un discreto aumento de este episodio en la segunda dosis con relación a la tercera.27
Informes remitidos al Sistema de Notificación de Efectos Adversos de las Vacunas (VAERS) en los Estados Unidos, comprobó que los casos de EHH eran ligeras, más frecuentes (53,0 %) en el sexo femenino. En cambio, en el programa de vigilancia de los Países Bajos se observó una frecuencia ligeramente mayor en el sexo masculino, similar al estudio realizado en el estado de Sao Paulo por Freitas.28-30 En este estudio no se observaron diferencias en cuanto al sexo.
Según Bonhoeffer, en 1 de cada 3 casos de EHH existe la presencia de fiebre;11 estos resultados coinciden con lo encontrado en nuestro estudio.
]]> Las convulsiones no se asociaron con los episodios de HHE notificados en el presente estudio. Sin embargo, otros estudios asocian este episodio con las convulsiones.9,31-33En la gran mayoría de los casos con diagnóstico de EHH, se notifica la presencia de palidez y cianosis. Sin embargo para los casos que no cumplan con los niveles de certeza diagnóstica, la Brighton Collaboration establece la categoría adicional,4 que refiere que es aquel evento de EHH notificado que no reúne pruebas suficientes para cumplir la definición de caso.
Los EHH constituyen un fenómeno infrecuente como consecuencia de la administración de estas vacunas, en lo fundamental con la vacuna DPTe. La dificultad en el diagnóstico, que por lo general es retrospectivo, puede ser una fuente relevante de error, una vez que la caracterización de este síndrome se basa en algunas señales relatadas por los padres, sin evidencias laboratoriales; por lo que es fundamental que el personal sanitario sepa reconocerlos, sobre todo en las siguientes 48 h a la vacunación.
Aunque, en ocasiones, es difícil establecer una relación causal entre la administración de la vacuna y un efecto adverso, debe comunicarse cualquier evento sospechoso.33
Una de las limitaciones de este estudio es que el sistema de vigilancia es pasivo y por las características de este cuadro clínico, que es de difícil reconocimiento, pudieran no reportarse todos los EHH ocurridos en el período de estudio. Además, esto conlleva a un entrenamiento sistemático y continuo de nuestros médicos y enfermeras en la identificación de este episodio.
REFERENCIAS BIBLIOGRÁFICAS
1. Vacunas e inmunización: Situación mundial. 3rd. Geneva: World Health Organization; 2009. p. 16.
]]>2. Escobar A, Valdespino JL, Sepúlveda J. Vacunas. Ciencia y salud. Historia de las vacunas y las vacunaciones. Colección Publicaciones técnicas del INDRE. Cap 2. México DF: Secretaria de Salud, Subsecretaria de Coordinación y Desarrollo; 1992. p. 10–20.
3. Hinman AR. Public health considerations; in Plotkin SA, Mortimer EA (eds) Vaccine Philadelphia, Saunders; 1988. p. 587-611.
4. Iskander J, Gidudu J, Arboleda N, Huang W. Selección de los principales problemas de seguridad de las vacunas. Ann Nestlé. 2008;66:93-102.
5. Whitembury A, Ticona M. Eventos supuestamente atribuibles a vacunación o inmunización. (ESAVI) Rev Peruana Epidemiol. 2009 [citado 14 de diciembre de 2014];13(3). Disponible en: http://censia.salud.gob.mx/contenidos/vacunas/ESAVI_2014.pdf
6. Thacker SB, Berkelman RL. Surveillance of Medical Technologies. J Public Health Policy. 1986;7(1):363-76.
7. Postila V, Kilpi T. Use of vaccine surveillance data in the evaluation of safety of vaccines. Vaccine. 2004;22:2076-79.
8. Cherry JD. Historical review of pertussis and the classical vaccine. Journal of Infectious Disease. 1996;174(supt 3):S259-S263.
9. Cody CL, Baraff LJ, Cherry JD. Nature and rates of adverse reactions associated with DPT and DT immunizations in infants and children. Pediatrics. 1981;68:650-60.
10. Abarca VK, Cerda LJ, Ferreccio RC. Reacciones adversas a vacunas DPT del Programa Nacional de Inmunizaciones. Rev Med Chil. Jan. 2009;137(1):10–7.
11. Bonhoeffer J, Kohl K, Chen R, Duclos P, Heijbel H, Heininger U, et al. The Brighton Collaboration: addressing the need for standardized case defi nitions of adverse events following immunization (AEFI).Vaccine. 2002;21(3-4):298-302.
12. Buettcher M. Hypotonic–Hiporesponsive Episode (HHE).as an adverse event following immunization in early childhood: case definition and guidelines for data collection, analysis and presentation. Vaccine. 2007;25 5875-81.
13. Rüggeberg J, Gold M, Bayas JM, Blum M, Bonhoeffer J, Friedlander S, et al. Anaphylaxis: case definition and guidelines for data collection, analysis and presentation of immunization safety data. Vaccine. 2007;25:5675-84.
14. Bonhoeffer J, Menkes J, Gold M, Souza-Brito G, Fisher M, Halsey N. Generalized convulsive seizure as an adverse event following immunization: case definition and guidelines for data collection, analysis and presentation. Vaccine. 2004;22:557–62.
15. Sejvar J, Kohl K, Gidudu J, Amato A, Bakshi N, Baxter R, et al. Guillain-Barré syndrome and Fisher syndrome: case definition and guidelines for collection, analysis and presentation of immunization safety data. Vaccine. 2011;29 599-612.
16. Bonhoeffer J, Vermeer P, Halperim S, Kempe A, Music S, Shindman J, et al. Persistent crying in infants and children as an adverse event following immunization: case definition and guidelines for data collection, analysis and presentation. Vaccine. 2004;22 586-91.
17. Baraff LJ, Shields WD, Beckwith L, Strome G, Marcy SM, Cherry JD, et al. Infants and children with convulsions and hypotonic-hyporesponsive episodes following diphtheriatetanus- pertussis immunization: follow-up evaluation. Pediatrics. 1988;81:789-94.
18. Vermeer-de Bondt PE, Labadie J, Rümke HC. Rate of recurrent collapse after vaccination with whole cell pertussis vaccine: follow-up study. BMJ. 1998;316:902-3.
19. DuVernoy TS, Braun MM. Hypotonic-hyporesponsive episodes reported to the Vaccine Adverse Event Reporting System (VAERS), 1996-1998. Pediatrics. 2000;106:52.
20. Rosenthal S, Chen R, Hadler S. The safety of acelular pertussis vaccine vs whole-cell pertussis vaccine: a postmarketing assessment. Arch Pediatr Adolesc Med. 1996;150(5):457-60.
21. Goodwin H, Nash M, Gold M. Vaccination of children following a previous hypotonic-hyporresponsive episode. J Paediatr Child Health. 1999;35:549-52.
22. Gold R, Scheiffele D, Halperin S, Dery P, Law B, Lebel M, et al. Hypotonic-hyporresponsive episodes in children hospitalized at 10 Canadian pediatric tertiary-care centers, 1991-1994. Can Commun Dis Rep. 1997;23:73-6.
23. Monteiro, SAMG. Avaliação dos Eventos Adversos Pós-vacina Tetravalente. Brasil, 2002 – 2005. [Dissertação de Mestrado]. Cuiabá: Instituto de Saúde Coletiva, Universidade Federal de Mato Grosso; 2007.
24. Ferreira Lemos MC. Vigilância de eventos adversos após vacinação contra difteria, tétano, coqueluche e haemophilus influenzae tipo b no município do Rio de Janeiro, 1998-2005. Disertación de maestria en Salud Pública; 2007.
25. Gold MS, Kempe A, Osbourn M. A comparison of serious adverse reactions to whole cell and acelular pertussis vaccines in South Australia. Med J Aust. 1999;171:331-32.
26. Vermeer-de Bondt PE, Van der Maas NA. The effect of age and dose number on the risk of collapse (hypotonic-hyporesponsive episode) after pertussis vaccination. Pediatr Infect Dis J. 2008;27:355-7.
27. Blumberg DA, Mink CM, Lewis K. Pathophysiology of reactions associated with pertussis vaccine. Devlop Biol Standard. 1991;73:289-95.
28. Vermeer-de Bondt P. Adverse events following immunisation under the National Vaccination Program of the Netherlands; RIVM reports in 1995. Bilthoven, The Netherlands; 2001.
29. Freitas FRM. Vigilância de Eventos Adversos Pós-Vacina DPT e Preditores de Gravidade. Estado de São Paulo 1984-2001. Epidemiologia e serviços de saúde. 2007 [citado 14 de diciembre de 2014];16(2). Disponible em: http://scielo.iec.pa.gov.br/pdf/ess/v16n2/v16n2a13.pdf
30. Edwards KM, Decker MD. Pertussis vaccine. In: Plotkin SA, OrensteinWA, editors. Vaccines. 4th ed. Philadelphia: Saunders; 2004. p. 515.
31. Stehr K, Cherry JD, Heininger U, Schmitt-Grohé S, Überall M, Laussucq S, et al. A comparative efficacy trial in Germany in infants who received either the Lederle/Takeda acellular pertussis componentDTP (DTaP) vaccine, the Lederle whole-cell component DTP vaccine, or DT vaccine. Pediatrics. 1998;101:1-11.
32. Martins FR, Keico H, Sarmento CH, Figueredo BA, Pacheco MA, Waldman E, et al. Eventos adversos pós-vacina contra a difteria, coqueluche e tétanos e fatores associados a súa gravidade. Rev Saúde Publica. 2007;41(6):1032-41.
]]>33. Brasil, Ministério da Saúde, Secretaria de Vigilância em Saúde. Manual dos Centros de Referência para imunobiológicos especiais. J Pediatr (Rio J). 2007;83(6):523-528.
Recibido: 6 de enero de 2015.
Aceptado: 26 de junio de 2015.
Belkys María Galindo Santana. Instituto de Medicina Tropical “Pedro Kourí”. Km 6 ½ Autopista Novia del Mediodía. La Lisa, La Habana, Cuba.
Correo electrónico: bgalindo@ipk.sld.cu
]]>