ARTÍCULO DE REVISIÓN
Regulación por helmintos de las respuestas inmunitarias del hospedero
Helminth regulation of host immune responses
Luis Fonte Galindo, Jessica Baldriche Acosta, Jorge Sarracent Pérez, Yisel Hernández Barrios, Annia Fong González
Instituto de Medicina Tropical "Pedro Kourí". La Habana, Cuba.
]]>
RESUMEN
Introducción: durante las últimas dos décadas se ha producido una rápida acumulación de conocimientos sobre la inmunología de las helmintosis. La información ahora disponible permite un mejor entendimiento de los mecanismos defensivos del hombre contra la infección por helmintos. Otra área del saber sobre la inmunología de las helmintosis, la relacionada con la regulación de las respuestas inmunitarias del hospedero ejercida por el parásito, con sus muy disímiles implicaciones clínicas y epidemiológicas, también se ha beneficiado de la expansión cognoscitiva de los últimos años.
Objetivos: revisar lo publicado sobre las evidencias, mecanismos y consecuencias de la regulación de las respuestas inmunitarias del hospedero ejercida por los helmintos.
Métodos: con el auxilio de diferentes buscadores electrónicos, se realiza una revisión de los artículos sobre helmintos, helmintosis y regulación de las respuestas inmunitarias del hospedero publicados durante el período 1995-2015. Algunas monografías y artículos originales fechados con anterioridad al intervalo mencionado también fueron consultados.
Resultados: se expone y analiza, y hasta donde es posible se sistematiza, la información colectada sobre los temas seleccionados.
Conclusiones: datos epidemiológicos, clínicos y experimentales evidencian que los helmintos logran modular las respuestas inmunitarias de sus respectivos hospederos y con ello sobrevivir en aquellos. Adicionalmente, la modulación de las respuestas inmunitarias del hospedero tiene importantes consecuencias clínicas y epidemiológicas que, en aras de una práctica médica de mejor calidad, deben ser conocidas por los profesionales relacionados con el diagnóstico, tratamiento y control de estas parasitosis.
Palabras clave: helmintosis; helmintos; inmunoregulación; coinfección; alergia; autoinmunidad.
ABSTRACT
]]> Introduction: the last two decades have witnessed a swift accumulation of knowledge about the immunology of helminthiases. The information now available allows to better understand human defense mechanisms against helminth infection. Another area of knowledge about the immunology of helminthiases which has also benefited from such recent expansion of knowledge is the regulation of host immune responses by the parasite, with its great variety of clinical and epidemiological implications.
]]> INTRODUCCIÓN
Documentos muy antiguos ya describen algunas de las manifestaciones clínicas que pueden tener lugar en el curso de una infección por helmintos.1-3 En correspondencia con ello, abundantes datos arqueológicos evidencian que los helmintos han infectado al hombre desde tiempos ancestrales.4 Por ejemplo, huevos de Trichuris trichiura han sido encontrados en restos de individuos que vivieron en el periodo neolítico (es decir, hace más de 5 000 años).5
Los helmintos, de manera particular los que son transmitidos por el suelo, exhiben un patrón agregado en las poblaciones que parasitan. La denominación de ese patrón, al que alternativamente también se le conoce como de sobredispersión, hace referencia al hecho de que en las áreas endémicas de helmintosis la mayoría de los individuos infectados alcanzan cargas parasitarias de intensidad leve o moderada, mientras que solo una pequeña parte de las personas muestran cargas severas.6-8
El equilibrio que tiene lugar en la mayoría de los individuos infectados por helmintos es el resultado de cientos de millones de años de coevolución de hospederos y parásitos. Ello ha conducido al desarrollo de respuestas defensivas por parte de los primeros y al estímulo de complejos mecanismos inmunomoduladores por parte de los segundos.4,9-17
Inmunidad adquirida tras infección natural por helmintos
Las respuestas inmunitarias a la infección por helmintos son frecuentemente insuficientes en dos aspectos claves: el sistema inmunitario es incapaz de eliminar la infección crónica y la memoria inmunitaria no logra proteger contra la reinfección aún después de la cura mediada por tratamiento farmacológico.10 Es decir, la inmunidad protectora observada tras la infección por patógenos virales y bacterianos rara vez se observa después de la infección por helmintos.
La protección contra la infección por helmintos tarda años en desarrollarse y nunca llega a alcanzar la cura estéril.18 Sin embargo, una inmunidad efectiva que significativamente reduce la carga parasitaria puede lograrse tras la inmunización con larvas o cercarias (y más recientemente, con antígenos recombinantes) en modelos animales de esquistosomosis, ancilostomosis y filariosis.19,20
De lo expresado en los dos párrafos precedentes se puede concluir que la generación de inmunidad en los humanos expuestos a la infección natural por helmintos es deficiente.
Microorganismos patógenos y helmintos estimulan diferentes mecanismos de control
El sistema inmunitario del humano, como también el de otros vertebrados, controla la infección por microorganismos patógenos (virus, bacterias, hongos y protozoos) de manera muy diferente a como lo hace con la infección por helmintos.4
]]> Los microorganismos patógenos, de manera particular los que invaden los tejidos de sus respectivos hospederos, estimulan respuestas inmunitarias tipo 1, las cuales resultan en la secreción de interleuquina 12 (IL-12), IL-23, interferón γ (IFN- γ) e IL-17.4,21 Estas respuestas, que generalmente dan lugar a potentes mecanismos efectores (producción de anticuerpos específicos, estimulación de actividad fagocítica y microbicida de células mononucleares, activación de células T-citotóxicas, entre otros), tienen lugar rápidamente. La premura en el desarrollo de estos procesos es crítica para el control de microorganismos potencialmente letales, que pueden dividirse con celeridad y diseminarse por órganos y tejidos. Estas respuestas, al desencadenar procesos inflamatorios de intensidad variable, pueden tener consecuencias adversas para el hospedero: la producción de daño tisular y, en ocasiones, de secuelas.4Los helmintos, en cambio, estimulan respuestas inmunitarias tipo 2, las que se caracterizan por la secreción de interleuquina 4 (IL-4), IL-5 e IL-13.4,22 Las respuestas generadas, que también dan lugar a potentes mecanismos efectores (variantes de citotoxicidad celular dependiente de anticuerpos contra estadios larvarios, vaciamiento intestinal contra formas adultas, entre otros), tienen lugar más lentamente y en su desarrollo participan células de los sistemas inmunitarios innatos y adquiridos. Estas células, además de actuar en la defensa del hospedero, realizan acciones antiinflamatorias y reparadoras de tejidos. Estas acciones son particularmente importantes si se tiene en cuenta que estos organismos eucariotas pluricelulares migran por tejidos vitales del hospedero causando lesiones en ellos.4,23,24 Los helmintos, además, estimulan poblaciones celulares regulatorias de los sistemas inmunitarios innatos y adquiridos, que funcionan por mecanismos diferentes de los mediados por citoquinas producidas por la subpoblación de células T auxiliadoras Th2 (células auxiliadoras tipo 2)4 y que, incluso, también modulan la actividad de estas últimas.10
En las infecciones por nematodos intestinales, particularmente las producidas por Ascaris lumbricoides, Trichuris trichiura y ancilostomídeos (A. duodenale y N. americanus), las lesiones anatomopatológicas son poco intensas y el proceso infectivo es de larga duración. La infecciones por estos helmintos suelen estar asociadas a niveles superiores de citoquinas como IL-10 y TGF-β (del inglés transforming growth factor-β) y de células Treg.25
El patrón de isotipos de anticuerpos puede ser un indicador del estado de inmunoregulación del hospedero. En las infecciones por helmintos, los niveles relativos de anticuerpos IgG4 e IgE parecen ser el mejor medidor de susceptibilidad a y protección de, respectivamente.25-29 El isotipo IgG4, diferente al IgE, no puede enlazar los receptores Fc sobre basófilos, mastocitos y eosinófilos y, diferente a otras subclases de IgG, no activa el sistema del complemento ni actúa como opsonina. Entonces, un mayor nivel de anticuerpos IgG4 es un marcador de un estado Th2 modificado (no inflamatorio) en el que están bloqueados los anticuerpos citofílicos como la IgE y disminuida la posibilidad de daño por inflamación.30
Mecanismos de Inmunomodulación
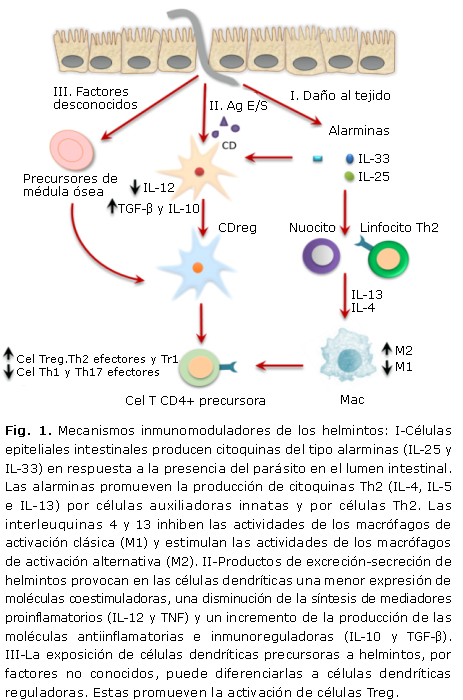
Los helmintos, incluidos los que son transmitidos por el suelo, interfieren en las respuestas inmunitarias de sus respectivos hospederos debido a una compleja madeja de mecanismos regulatorios. Estos, por las secuencias en que tienen lugar, pueden agruparse en tres grandes ejes (sin que ello excluya la posibilidad de interacciones entre componentes de las tres vertientes) (Fig. 1).

A continuación se describen, grosso modo y de forma secuencial, los más trascendentales eventos que tienen lugar en los mencionados ejes regulatorios y, ya finalizando este documento, se hace referencia con más detalles a los principales componentes de cada uno de ellos.
I. Producción de citoquinas del tipo alarminas (IL-25, IL-33 y TSLP) por células epiteliales intestinales en presencia del parásito.
]]>- Las células epiteliales intestinales (y posiblemente otras células en otros órganos y tejidos) producen IL-25, IL-33 y TSLP (del inglés thimic stromal limphopoietin) en respuesta a la presencia del parásito en el lumen intestinal.15,31 IL-25 e IL-33, como se verá más adelante, están involucradas en el estímulo a la producción primaria de mediadores tipo 2. TSLP, en cambio, parece estar más relacionado con la limitación de la producción de IL-12 por células dendríticas.32-33
- Las células CD4+ Th2, protagónicas en las respuestas adaptativas a la infección por helmintos, son las mayores fuentes de citoquinas tipo 2.34 Sin embargo, estudios de la última década han identificado una nueva línea de células innatas en los ganglios linfáticos mesentéricos que producen grandes cantidades de IL-4, IL-5 e IL-13.35-38 Estas células, más frecuentemente denominadas células auxiliadoras tipo 2 innatas,38 responden a las alarminas IL-25 e IL-33 secretadas por las células epiteliales intestinales en presencia del parásito.37-38
- Las interleuquinas 4 y 13 (IL-4 e IL-13) producidas por las células auxiliadoras tipo 2 innatas y por las células CD4 + Th2 modulan las funciones de los macrófagos circundantes de dos maneras: primero, deprimen las actividades proinflamatorias y microbicidas de los macrófagos de activación clásica (M1),4,39 segundo, promueven la secreción de las citoquinas antiinflamatorias e inmunoreguladoras IL-10 y TGF-β por los macrófagos de activación alternativa (M2)4,40. IL-10 y TGF-β regulan respuestas inflamatorias e inmunitarias tanto de tipo 1 como de tipo 2.9
II. Los productos de excreción-secreción de helmintos estimulan cambios en la actividad de las células dendríticas.
La presencia de productos de excreción-secreción de helmintos modifica la actividad presentadora de antígenos de las células dendríticas de dos maneras.4,14-15 A saber:
- La menor expresión en su superficie de moléculas coestimuladoras (CD40, CD80 y CD86) y la disminución de la síntesis de mediadores proinflamatorios, como IL-12 y TNF (del inglés tumor necrosis factor). Ambos hechos traen como consecuencia una supresión de la diferenciación de células Th0 a células Th1 o células Th17.4,10,41-44
- El incremento de la producción de las moléculas antiinflamatorias e inmunoreguladoras IL-10 y TGF-β. Esto, indirectamente, favorece la diferenciación de células Th0 a células Th2.4,10, 45,46
III. La exposición de células dendríticas precursoras a helmintos, por factores no conocidos, puede diferenciarlas a células dendríticas reguladoras.4,10,47-49 Estas, a diferencia de las células dendríticas clásicas, son ineficientes en la presentación antigénica a células T. En lugar de ello, estas células promueven la diferenciación de células Th0 nativas a células Treg o, alternativamente, estimulan la expansión de subpoblaciones de células Treg preexistentes.
]]>
Componentes celulares de la inmunoregulación
Las respuestas inmunitarias contra los helmintos, tanto a nivel sistémico como de mucosas, involucran una amplia variedad de respuestas innatas y adaptativas que tienen como objetivo la inducción y amplificación de potentes mecanismos defensores. La coevolución milenaria entre hospederos y parásitos, que los ha llevado a adaptarse los unos a los otros, y el carácter potencialmente patógeno de muchas de esas respuestas, han resultado en el desarrollo de mecanismos reguladores de las respuestas inmunitarias del hospedero.4,9-17
En la modulación de las respuestas inmunitarias del hospedero participan mediadores solubles, de manera particular IL-10 y TGF-β, y diferentes tipos celulares, también de la inmunidad innata y de la adquirida. A los primeros, ya se hizo referencia en los acápites precedentes. Los segundos, por la necesidad de conocer con detalles complementarios su funcionamiento, se abordan separadamente a continuación.
1. Macrófagos de activación clásica y macrófagos de activación alternativa
Las citoquinas producidas por las células Th1 y Th2 totalmente diferenciadas inducen subpoblaciones de macrófagos funcionalmente diferentes: macrófagos de activación clásica (M1) y macrófagos de activación alternativa (M2), respectivamente.4,15,39 Los macrófagos M1 secretan citoquinas proinflamatorias (IL-12 y TNF, entre otras), producen intensamente formas reactivas de oxígeno y nitrógeno y son efectores claves contra patógenos intracelulares. Los macrófagos M2, en cambio, secretan citoquinas antiinflamatorias (IL-10 y TGF-β), tienen alta expresión de arginasa-1, participan activamente en la resolución de heridas e, indirectamente, toman parte en la resistencia del hospedero a la infección por helmintos.4,22 Los estudios que reportaron que los ratones con macrófagos deficientes de arginasa-1 eran más capaces de controlar la infección por M. tuberculosis4,50 y que los macrófagos tratados in vitro con IL-4 mostraban un incremento en la replicación de micobacteria,4,51 fueron los primeros que indicaron que los macrófagos M2 generados durante la infección por helmintos potencialmente podían reducir la actividad efectora de los fagocitos mononucleares contra los patógenos microbianos.4
Es interesante hacer notar que el papel homeostático de los macrófagos M2 se extiende también, a las respuestas antiparasitarias (es decir, estos macrófagos controlan también el componente inflamatorio de las respuestas inmunitarias tipo 2).10 En ratones cuyos macrófagos están deficientes de arginasa-1 (LysMcre Arg-1-/flox) la infección por esquistosomas resulta en la formación no controlada de granulomas, que alcanzan mayores tamaños que los que se desarrollan en los ratones de un grupo control (que no portan esa deficiencia). En los animales con la deficiencia enzimática en sus macrófagos, las dimensiones de los granulomas no se reducen al pasar la infección a estadios crónicos y mueren por la inflamación mediada por células Th2.52
Actualmente, varios grupos trabajan en la identificación de las vías de activación, los factores de transcripción, las modificaciones epigenéticas y los microRNAs (RNA, del inglés ribonucleic acid) que regulan la polarización de macrófagos M1 a M2.4,53 Evidencias recientes parecen indicar que los macrófagos están en un estado de activación continua entre las dos formas polarizadas, lo cual sugiere la existencia de notable plasticidad en el desarrollo ontogénico de este tipo celular.53 En esta línea de pensamiento, aún debe ser determinado si en hospederos coinfectados los macrófagos recién reclutados al sitio de infección adquieren el fenotipo M2 bajo la influencia de IL-4 e IL-13 o si macrófagos M1 que ya han interiorizado patógenos microbianos son reprogramados a convertirse en macrófagos M2 bajo la influencia de esas citoquinas.4
2. Células dendríticas
]]>Entre las células presentadoras de antígenos, las células dendríticas son fundamentales en la inducción y mantenimiento de respuestas defensivas del hospedero a microorganismos patógenos. La exposición de los receptores TLR (del inglés Toll-like receptor) en la superficie de las células dendríticas a ligandos microbianos (por ejemplo, lipopolisacaridos bacterianos), incrementa en estas la expresión de moléculas coestimuladoras (CD40, CD80 y CD86) y la síntesis de mediadores proinflamatorios, como IL-12 y TNF.42-44,54 Estos eventos dan lugar a respuestas linfocitarias Th1 y T-citotóxicas.55-57
De la misma manera, las células dendríticas son protagónicas en la inducción y mantenimiento de respuestas defensivas del hospedero a parásitos pluricelulares. La depleción de células dendríticas abole las respuestas inmunitarias Th2 a la infección parasitaria y la exposición de esas células a antígenos de helmintos induce ese tipo de respuestas.45,46
El mayor evento regulador de las respuestas Th1 y T-citotóxicas a patógenos intracelulares es la exposición de las células dendríticas del hospedero a la infección por helmintos (o a sus productos de excreción-secreción).4,41 Los mecanismos por los cuales los helmintos (o sus componentes) estimulan cambios en la actividad de las células dendríticas ya fueron descritos en el acápite anterior.
No se conoce si la regulación de las respuestas inmunitarias a los patógenos microbianos es predominantemente consecuencia de la inhibición de la expresión de moléculas coestimuladoras y de la disminución de la producción de mediadores proinflamatorios, o es en mayor grado resultado de la activa promoción de células Treg.4 Aparentemente, el defecto en la coestimulación en las células presentadoras de antígenos en las personas infectadas por helmintos tendría un efecto más profundo durante la iniciación de una respuesta primaria, como serían los casos de la primera dosis de una inmunización y de una primoinfección por un microorganismo patógeno. Por el contrario, un régimen regulatorio negativo impuesto por la expansión y activación de células Treg pudiera tener un papel más prominente en restringir la función de células efectoras de memorias preformadas y ya localizadas en tejidos periféricos.
Los mecanismos por los cuales las células dendríticas inducen respuestas Th1 y Th17 en presencia de patógenos microbianos son bien conocidos (interacción de ligandos microbianos con receptores TLR en las células presentadoras, aumento en la expresión de moléculas coestimuladoras e incremento en la producción de mediadores proinflamatorios). Sin embargo, los mecanismos dendríticos involucrados en la inducción de respuestas Th2 o en la expansión y activación de células Treg en presencia de helmintos son menos entendidos.4,15 Los resultados de dos estudios recientes parecen estar arrojando luz sobre el asunto. El primero, apunta hacia la demostración de que un grupo de moléculas helmínticas inhibe la capacidad de las células dendríticas para responder a ligandos microbianos de receptores TLR y producir IL-12.58-59 El segundo, refiere que el hallazgo de que un grupo de citoquinas del tipo alarminas (por ejemplo, TSLP), que son producidas por las células epiteliales intestinales, deprimen la producción de IL-12 por las células dendríticas.60
3. Células T reguladoras
Las células Treg, cuya participación en el mantenimiento de la tolerancia a lo propio en el humano y en algunos modelos animales ha sido bien demostrada,61 están emergiendo como el más importante fenotipo regulatorio en las infecciones por helmintos.10,15 Al menos, tres subpoblaciones de células Treg han sido identificadas: las células Treg “naturales”, que expresan el factor de transcripción Foxp 3 desde su desarrollo en el timo; las células Treg “inducidas”, que expresan el factor de transcripción Foxp 3 en la periferia; y las células Treg Foxp 3- tipo 1 (tr1).10 Todas las subpoblaciones de células Treg, aunque con diferencias que dependen de las circunstancias en que ejerzan su acción, pueden producir IL-10 y TGF-β.62
Las células Treg son activadas, fundamentalmente, en tres circunstancias: durante toda la vida, para controlar potenciales respuestas autoinmunes,61 durante muchos procesos infecciosos, para modular respuestas protectoras que, en exceso, pudieran se dañinas y para suprimir respuestas cualitativamente patológicas,32 y, en el caso de las infecciones por helmintos, para limitar y modificar las respuestas inmunitarias del hospedero y prolongar la infección en el tiempo.30 Por la existencia de estas diferentes fuentes de activación, un debate sigue en pie: las células Treg emergen de una respuesta homeostática a la inflamación o están dirigidas de una manera selectiva por los patógenos, de manera particular los helmintos, para perpetuar la infección.10
]]> En las infecciones humanas por parásitos transmitidos por el suelo, los hallazgos de evidencias del involucramiento de las Células Treg en el control de las respuestas inmunitarias del hospedero no han sido numerosos. Posiblemente, ello sea consecuencia de que los estudios de linfocitos de sangre periférica, generalmente los más disponibles, no sean un buen reflejo de lo que ocurre con las poblaciones linfocitarias en la pared intestinal. Sin embargo, fue encontrado que individuos infectados por ancilostomídeos mostraban proporciones de linfocitos T circulantes CD4+ Foxp 3+ mayores que las de los controles no infectados.63
4. Células B reguladoras
Es de conocimiento general que los linfocitos B, y las células plasmáticas resultantes de su diferenciación desempeñan papeles protagónicos en la producción de anticuerpos. En los últimos tres lustros una subpoblación de linfocitos B productores de IL-10, cuya función biológica no se conoce con certeza, está recibiendo especial atención.10,15 Algunas evidencias en modelos murinos parecen indicar que estos linfocitos, a los que indistintamente se les ha denominado células Breg o células B10, participan en el control de desórdenes autoinmunes como la encefalitis autoinmune experimental murina64 y en la regulación de respuestas inmunitarias a helmintos.65,66
Células Breg también han sido identificadas en pacientes infectados por helmintos.67 Por otro lado, se ha sugerido que células B productoras de IgG4 asociadas a tolerancia a la infección por filarias de alguna manera podrían derivar de células Breg productoras de IL-10, lo que estaría indicando un posible enlace entre estos dos fenotipos regulatorios.68 Estas evidencias en humanos parecen confirmar que las células Breg, como las células Treg, están involucradas en la supresión de respuestas inmunitarias antihelmínticas.10
5. Consecuencias de la inmunoregulación
]]>La capacidad de los helmintos de modular las respuestas inmunitarias de sus respectivos hospederos, además de permitirles sobrevivir en estos, atenúa los efectos inflamatorios de los mecanismos defensivos de los animales parasitados y, con ello, reduce los daños inmunopatológicos asociados a esas respuestas.10
Sin embargo, la regulación por los helmintos de las respuestas inmunitarias de los hospederos que parasitan puede tener consecuencias clínicas y epidemiológicas adicionales. A saber: incremento en la susceptibilidad a otras infecciones, cambios en la frecuencia e intensidad de fenómenos alérgicos y autoinmunes, insuficiencias en las respuestas a vacunas contra otros microorganismos y, sin que aún esté suficientemente documentado, desarrollo de algunos tipos de tumores4,9-17 (Fig. 2).
1. Incremento en la susceptibilidad a otras infecciones
Los estudios de distribución geográfica de las infecciones por helmintos y por microorganismos patógenos, particularmente aquellos de mayor significación clínica y epidemiológica (virus de la inmunodeficiencia humana -VIH-, Mycobacterium tuberculosis y Plasmodium spp.), han demostrado que estas coexisten en muchas de las áreas geográficas en que están presentes las condiciones socioeconómicas y ambientales que propician su transmisión.4,10,15 Sin embargo, también ha quedado evidenciado que las coinfecciones no son solo consecuencia de la presencia de condiciones comunes para la diseminación de unas y otras. Otro evento, no menos importante, también parece intervenir: las infecciones por helmintos, que con más frecuencia transcurren a edades tempranas, estimulan la producción de citoquinas tipo 2 (IL-4, IL-5 e IL-13) y activan mecanismos T reguladores (células Treg, IL-10 y TGF-β, entre otros) que, en su conjunto, inhiben el desarrollo de respuestas efectoras Th1, necesarias para el control de los microorganismos antes mencionados.4,9-10,69
Paradójicamente, las helmintosis no solo pueden asociarse con mayor susceptibilidad a infecciones por microorganismos patógenos sino también a una menor ocurrencia y severidad de los daños inmunopatológicos relacionados con estos.9 Por ejemplo, si bien la infección por helmintos puede inhibir el desarrollo de inmunocompetencia a la infección por Plasmodium (que en muchos aspectos es mediada por mecanismos efectores Th1) y hacer a los hospederos más susceptibles al desarrollo de la enfermedad, también puede disminuir los riesgos de cuadros severos de malaria cerebral (a esta complicación de la malaria la caracteriza una sobreproducción de citoquinas proinflamatorias y, como ya fuera descrito anteriormente, la infección por helmintos disminuye la producción de esas citoquinas mediante la secreción de los mediadores regulatorios IL-10 y TGF-β).9,70
2. Cambios en la frecuencia e intensidad de eventos alérgicos
]]> 3. Disminución en la frecuencia e intensidad de fenómenos autoinmunesLa prevalencia de eventos alérgicos (tales como asma, rinitis alérgica y dermatitis atópica) se ha incrementado durante las últimas décadas, fundamentalmente en los países industrializados.71,72 Según la hipótesis de la higiene, ejercicio especulativo aún en desarrollo, las razones de ese incremento son varias: mayor proporción de personas viviendo en áreas urbanas, familias más pequeñas, mejores condiciones sanitarias que, entre otras consecuencias, disminuye la transmisión fecal-oral de agentes patógenos y, finalmente, la menor frecuencia o ausencia de infecciones por helmintos.73
Mucha atención ha recibido la demostración de que las infecciones por helmintos podrían ser un factor de importancia mayor en contrarrestar el desarrollo de eventos alérgicos en el mundo económicamente desarrollado.74,75 Por otro lado, algunas publicaciones han reportado que poblaciones con altos índices de infección por helmintos muestran menor propensión a alergias (generalmente evidenciadas por menor positividad a pruebas de reactividad cutánea a alérgenos, tales como el polvo doméstico), particularmente en niños infectados por Schistosoma haematobium76,77 y Schistosoma mansoni.78-80 Otra evidencia de un efecto causal de las infecciones por helmintos en la reducción de fenómenos alérgicos surge de reportes de que el tratamiento antihelmíntico incrementa la positividad a pruebas de reactividad cutánea a alérgenos en niños.81,82
El efecto regulador de las infecciones helmínticas sobre las respuestas Th2/IgE parece ser el mecanismo que explicaría los postulados de la hipótesis de la higiene en su acepción más actual.83 Obviamente, la relación entre eventos alérgicos e infecciones por helmintos no es homogénea en todas las áreas endémicas. Ello dependerá de factores relacionados con el hospedero (fondo genético), el parásito (especies implicadas, frecuencia e intensidad de la infección) y el medio ambiente (clima, higiene). En los países tropicales, por ejemplo, la infección por helmintos puede dar lugar a efectos inmunosupresores (las más de las veces)84 e inmunopotenciadores (por ejemplo, las infecciones de baja intensidad por A. lumbricoides pueden elevar la frecuencia de fenómenos alérgicos).85
Evidencias epidemiológicas y experimentales parecen proporcionar suficiente soporte al postulado de que las infecciones por helmintos podrían proveer alguna protección contra eventos autoinmunes e inflamatorios.86 Por otro lado, algunos estudios han demostrado que las estrategias de higienización, saneamiento ambiental y desparasitación en las áreas urbanizadas han hecho a las personas que en ellas viven más vulnerables al desarrollo de enfermedades autoinmunes y alteraciones inflamatorias.86,87 Aunque la mayoría de los datos epidemiológicos y un cúmulo creciente de resultados experimentales favorecen al mencionado postulado, la comprensión precisa de la relación entre infecciones por helmintos y fenómenos autoinmunes es hoy tema de intensos estudios y punto de partida para prometedoras aproximaciones terapéuticas.10,87
Desde que se obtuvieron las primeras evidencias de que las infecciones por helmintos proporcionan alguna protección contra eventos autoinmunes e inflamatorios, numerosos estudios se han realizado para conocer los mecanismos por los cuales ello ocurre. Los resultados obtenidos han demostrado que esa protección es solo una de las varias consecuencias de un fenómeno más profundo: la compleja regulación de las respuestas inmunitarias del hospedero ejercida por estos parásitos.4,9-10,86,88
4. Disminución de respuestas a vacunas
Estudios en humanos y en animales de experimentación, a los que se hace referencia a continuación, han demostrado que la regulación de las respuestas inmunitarias del hospedero debido a la infección por helmintos puede disminuir la eficacia de algunas vacunas, de manera particular de aquellas que requieren de respuestas Th1:
- Comparados con individuos sanos, pacientes de esquistosomosis desarrollaron respuestas de IFN- γ más débiles a la inmunización con toxoide tetánico.89
- En relación con un grupo control de personas sanas, pacientes de oncocercosis y filariosis linfática también desarrollaron respuestas de IFN- γ más débiles a la inmunización con toxoide tetánico. En estos pacientes se demostró, además, niveles más elevados de la citoquina reguladora IL-10.90,91
- En un trabajo realizado en Ecuador, un grupo de niños infectados por áscaris, al que se trató con albendazol previo a la inmunización con una dosis de la vacuna oral viva atenuada de cólera, respondió con títulos de anticuerpos vibriocidas más altos e índices de seroconversión superiores a los de un grupo control integrado por niños también infectados por ese parásito al que se le administró un placebo.92 Fue muy interesante observar que la respuesta de citoquinas Th1 a la subunidad B de la toxina colérica, un componente de la vacuna empleada, fue más elevada en los niños que recibieron albendazol.93
]]> - Empleando un diseño similar al empleado en Ecuador, un estudio realizado en Etiopia encontró que niños tratados con albendazol antes de la inmunización con BCG desarrollaron mejores respuestas de IFN-γ ante componentes de la vacuna.94- Estudios realizados en modelos animales han reiterado los resultados de los trabajos llevados a cabo en humanos. En cerdos, la infección por áscaris altera la eficacia de la vacuna contra Mycoplasma hyopneumoniae.95 En ratones, la infección por S. mansoni interfiere con los efectos protectores de la vacunación con BCG96 y la infección por Heligmosomoides polygyrus reduce la eficacia de la inmunización contra Plasmodium chabaudi.97 En hámster, la infección por Ancylostoma ceylanicum deprime la respuesta linfoproliferativa, la producción de IFN- γ y la síntesis de anticuerpos a la vacunación con un antígeno recombinante del propio parásito (Ay-ASP-2) y, en correspondencia con ello, estimula la producción de IL-10.98
Tomados de conjunto, estos resultados en relación con la interferencia de las infecciones por helmintos sobre las respuestas a inmunizaciones deben ser tenidos en cuenta en el diseño de ensayos clínicos de vacunas humanas y en el desarrollo de estrategias de vacunación.
5. Aumento en la frecuencia de algunos tumores
Una de las consecuencias menos exploradas de la interacción entre infección por helmintos y respuestas inmunitarias es el posible efecto de esas parasitosis sobre la aparición y desarrollo de tumores. Aunque no existen evidencias epidemiológicas de que las helmintosis comprometan la vigilancia inmunológica contra procesos neoplásicos, existen ejemplos de asociación de algunas especies de parásitos con determinados tipos de tumores. Las infecciones por Opisthorchis viverrini y Clonorchis sinensis tienen una fuerte asociación con el desarrollo de colangiocarcinoma, un cáncer de los conductos biliares.99-100 También se ha demostrado la asociación entre infección por S. haematobium y cáncer de vejiga, posiblemente relacionada con el egreso de huevos de este helminto por la pared vesical.101 Se ha especulado que estas asociaciones representan casos en que promotores tumorales derivados de los parásitos, actuando en un contexto de inmunomodulación, estimulan el desarrollo de neoplasias.102
REFERENCIAS BIBLIOGRÁFICAS
1. Hotez PJ, Brindley PJ, Bethony JM. Helminth infections: the great neglected tropical diseases. J Clin Invest. 2008;118:1311-21.
]]>2. Cox F. History of human parasitology. Clin Microbiol Rev. 2002;15:595-612.
3. Hotez P, Ottesen E, Fenwick A, Molyneux D. The neglected tropical diseases: the ancient afflictions of stigma and poverty and the prospects for their control and elimination. Adv Exp Med Biol. 2006;582:23-33.
4. Salgame P, Yap GS, Gause WC. Effect of helminth-induced immunity on infections with microbial pathogens. Nat immunol. 2013;14:1118-26.
5. Dickson, JH. The omnivorous Tyrolean Iceman: colon contents (meat, cereals, pollen, moss and whipworm) and stable isotope analyses. Phil Trans R Soc Lond. 2000;355:1843-9.
6. Maddison SE. Serodiagnosis of parasitic diseases. Clin Microbiol Rev. 1991;4:457-9.
]]>7. Bundy DAP. This wormy world then and now. Parasitology Today. 1997;13:407-8.
8. de Silva NR, Brooker S, Hotez PJ, Montresor A, Engels D, Savioli L. Soiltransmitted helminth infections: updating the global picture. Trends Parasitol. 2003;19:547-51.
9. Moreau E, Chauvin A. Immunity against helminths: interactions with the host and the intercurrent infections. J Biomed Biotech 2010, doi:10.1155/2010/428593.
10. Mc Sorley HJ, Maizels RM. Helminth Infections and Host Immune Regulation. Clin Microbiol Rev. 2012;25:585-608.
11. Mishra PK, Palma M, Bleich D, Loke P, Gause WC. Systemic impact of intestinal helminth infections. Mucosal Immunol. 2014;7:753-62.
]]>12. Flamme LA. The platinum age of parasitology: harnessing the power of the parasite. Parasite Immunol. 2015;37:275-6.
13. Fleming JO, Weinstock JV. Clinical trials of helminth therapy in autoimmune diseases: rationale and findings. Parasite Immunol. 2015;6:277-92.
14. Shepherd C, Navarro S, Wangchuk P, Wilson D, Daly NL, Loukas A. Identifying the immunomodulatory component of helminths. Parasite Immunol. 2015;6:293-303.
15. Nutman T. Looking beyond the induction of Th2 responses to explain immunomodulation by helminths. Parasite Immunol. 2015;6:303-13.
16. Loke P, Lim YAL. Helminths and the microbiota: parts of the hygiene hypothesis. Parasite Immunol. 2015;6:314-23.
]]>17. Ezenwa VO, Jolles AN. Opposite effects of anthelmintic treatment on microbial infection at individual versus population scales. Science. 2015;347:175-7.
18. Anderson RM, May RM. Helminth infection of humans: mathematical model, population dynamics and control. Adv Parasitol. 1985;24:1-101.
19. Bethony JM. Vaccines to combat the neglected tropical diseases. Immunol Rev. 2011;239:237-70.
20. Mangan NE, van Rooijen N, McKenzie AN, Fallon PG. Helminth-modified pulmonary immune response protects mice from allergen-induced airway hyperresponsiveness. J Immunol. 2006;176:138-47.
21. Palm NW, Rosenstein RK., Medzhitov R. Allergic host defences. Nature. 2012;484:465-72.
]]>22. Anthony RM, Rutitzky LI, Urban JF, Stadecker MJ, Gause WC. Protective immune mechanisms in helminth infection. Nat Rev Immunol. 2007;7:975-87.
23. Allen JE, Maizels RM. Diversity and dialogue in immunity to helminths. Nat Rev Immunol. 2011;11:375-88.
24. Chen F. An essential role for TH2-type responses in limiting acute tissue damage during experimental helminth infection. Nat Med. 2012;18:260-6.
25. García-Hernández MH. Regulatory T cells in children with intestinal parasite infection. Parasite Immunol. 2009;31:597-603.
26. Hagan P, Blumenthal UJ, Dunn D, Simpson AJG, Wilkins HA. Human IgE, IgG4 and resistance to reinfection with Schistosoma haematobium. Nature. 1991;349:243-5.
]]>27. Joseph S. Increases in human T helper 2 cytokine responses to Schistosoma mansoni worm and worm-tegument antigens are induced by treatment with praziquantel. J Infec Dis. 2004;190:835-42.
28. Manoury B, Gregory WF, Maizels RM, Watts C . Bm-CPI-2, a cystatin homolog secreted by the filarial parasite Brugia malayi, inhibits class II MHC-restricted antigen processing. Curr Biol. 2001;11:447-51.
29. Sartono E, Kruize YCM, Kurniawan-Atmadja A, Maizels RM, Yazdanbakhsh M. Depression of antigen-specific interleukin-5 and interferon-γ responses in human lymphatic filariasis as a function of clinical status and age. J Infect Dis. 1997;175:1276-80.
30. Matisz CE, McDougall JJ, Sharkey KA, McKay D. Helminth parasites and the modulation of joint inflammation. J Parasitol Res. 2011:942616. doi:10.1155/2011/942616.
31. Saenz SA. Innate immune cell populations function as initiators and effectors in Th2 cytokine responses. Trends Immunol. 2010;31: 407-13.
]]>32. Massacand JC. Helminth products bypass the need for TSLP in Th2 immune responses by directly modulating dendritic cell function. Proc Natl Acad Sci USA. 2009;106:13968-73.
33. Taylor BC. TSLP regulates intestinal immunity and inflammation in mouse models of helminth infection and colitis. J.Exp Med. 2009;206:655-67.
34. Harris N. Advances in helminth immunology: optimism for future vaccine design? Trends Parasitol. 2011;27:288-93.
35. Fallon PG. Identification of an interleukin (IL)-25-dependent cell population that provides IL-4, IL-5, and IL-13 at the onset of helminth expulsion. J Exp Med. 2006;203:1105-16.
36. Moro K. Innate production of T(H)2 cytokines by adipose tissue-associated c-Kit(+)Sca-1(+) lymphoid cells. Nature. 2010;463:540-4.
]]>37. Neill DR. Nuocytes represent a new innate effector leukocyte that mediates type-2 immunity. Nature. 2010;464:1367-70.
38. Price AE. Systemically dispersed innate IL-13-expressing cells in type 2 immunity. Proc Natl Acad Sci USA. 2010;107:11489-94.
39. Martinez F, Helming L, Gordon S. Alternative activation of macrophages: an immunologic functional perspective. Annu Rev Immunol. 2009;27:451-83.
40. Murray PJ, Wynn TA Protective and pathogenic functions of macrophage subsets. Nat Rev Immunol. 2011;11:723-37.
41. White RR, Artavanis-Tsakonas K. How helminths use excretory secretory fractions to modulate dendritic cells. Virulence. 2012;3:668-77.
]]>42. Everts B. Schistosome-derived omega-1 drives Th2 polarization by suppressing protein synthesis following internalization by the mannose receptor. J Exp Med. 2012;209:1753-67.
43. Al-Riyami L, Harnett,W. Immunomodulatory properties of ES-62, a phosphorylcholine-containing glycoprotein secreted by Acanthocheilonema viteae. Endocr. Metab. Immune Disord. Drug Targets. 2012;12:45-52.
44. Klaver EJ. Trichuris suis-induced modulation of human dendritic cell function is glycan-mediated. Int J Parasitol. 2013;43:191-200.
45. Carvalho L. Mechanisms underlying helminth modulation of dendritic cell function. Immunology. 2009;126:28-34.
46. Everts B, Smits HH, Hokke CH, Yazdankbakhsh M. Sensing of helminth infections by dendritic cells via pattern recognition receptors and beyond: consequences for T helper 2 and regulatory T cell polarization. Eur J Immunol. 2010;40:1525-37.
]]>47. Mahanty S. High levels of spontaneous and parasite antigen-driven interleukin-10 production are associated with antigen-specific hyporesponsiveness in human lymphatic filariasis. J Infect Dis. 1996;173:769-73.
48. Bancroft AJ, Else KJ, Humphreys NE, Grencis RK. The effect of challenge and trickle Trichuris muris infections on the polarisation of the immune response. Int J Parasitol. 2001;31:1627-37.
49. Steinfelder S. The major component in schistosome eggs responsible for conditioning dendritic cells for Th2 polarization is a T2 ribonuclease (omega-1). J Exp Med. 2009;206:1681-90.
50. El Kasmi KC. Toll-like receptor-induced arginase 1 in macrophages thwarts effective immunity against intracellular pathogens. Nat Immunol. 2008;9:1399-406.
51. Harris J. T helper 2 cytokines inhibit autophagic control of intracellular Mycobacterium tuberculosis. Immunity. 2007;27:505-17.
]]>52. Rausch S. Functional analysis of effector and regulatory T cells in a parasitic nematode infection. Infect Immun. 2008;76:1908-19.
53. Mosser DM, Edwards, JP. Exploring the full spectrum of macrophage activation. Nat Rev Immunol. 2008;8:958-69.
54. Segura M, Su Z, Piccirillo C, Stevenson, MM. Impairment of dendritic cell function by excretory-secretory products: a potential mechanism for nematode-induced immunosuppression. Eur J Immunol. 2007;37:1887-904.
55. Setiawan T. Heligmosomoides polygyrus promotes regulatory T-cell cytokine production in the murine normal distal intestine. Infect Immun. 2007;75:4655-63.
56. Walsh KP, Brady MT, Finlay CM, Boon L, Mills KH. Infection with a helminth parasite attenuates autoimmunity through TGF-β-mediated suppression of Th17 and Th1 responses. J Immunol. 2009;183:1577-86.
]]>57. Aranzamendi C. Trichinella spiralis-secreted products modulate DC functionality and expand regulatory T cells in vitro. Parasite Immunol. 2012;34:210-23.
58. Elliott AM. Associations between helminth infection and CD4+ T cell count, viral load and cytokine responses in HIV-1-infected Ugandan adults. Trans R Soc Trop Med Hyg. 2003;97:103-8.
59. Li Z. The phenotype and function of naturally existing regulatory dendritic cells in nematode-infected mice. Int J Parasitol. 2011;41:1129-37.
60. Teixeira A. Cytokines, chemokine receptors, CD4+CD25HIGH+ T-cells and clinical forms of human schistosomiasis. Acta Trop. 2008;108:139-49.
61. Knowles SC. The effect of helminth co-infection on malaria in mice: a meta-analysis. Int J Parasitol. 2011;41:1041-51.
]]>62. Schopf L. Differential modulation of allergic eye disease by chronic and acute Ascaris infection. Invest Ophthalmol Vis Sci. 2005;46:2772-80.
63. Sakaguchi S, Yamaguchi T, Nomura T, Ono M. Regulatory T cells and immune tolerance. Cell. 2008;133:775-87.
64. Fillatreau S, Sweenie CH, McGeachy MJ, Gray D, Anderton S. B cells regulate autoimmunity by provision of IL-10. Nat Immunol. 2002;3:944-50.
65. Yazdanbakhsh M. T cell responsiveness correlates differentially with antibody isotype levels in clinical and asymptomatic filariasis. J Infect Dis. 1993;167:925-31.
66. Su Z, Segura M, Stevenson MM. Reduced protective efficacy of a blood-stage malaria vaccine by concurrent nematode infection. Infect Immun. 2006;74:2138-44.
]]>67. Correale J, Farez M, Razzitte G. Helminth infections associated with multiple sclerosis induce regulatory B cells. Ann Neurol. 2008;64:187-99.
68. Josefowicz SZ, Lu LF, Rudensky AY. Regulatory T cells: mechanisms of differentiation and function. Annu Rev Immunol. 2012;30:531-64.
69. MacDonald AS, Araujo MI, Pearce EJ. Immunology of parasitic helminth infections. Infect Immun. 2002;70:427-33.
70. Van Riet E, Hartgers FC, Yazdanbakhsh M. Chronic helminth infections induce immunomodulation: consequences and mechanisms. Immunobiology. 2007;212:475-90.
71. Taylor B, Wadsworth J, Wadsworth M, Peckham M. Changes in the reported prevalence of childhood eczema since the 1939–45 war. The Lancet. 1984;2:1255-7.
]]>72. Ring J. Davos Declaration: allergy as a global problem. Allergy. 2012;67:141-3
73. Bruschi F, Araujo MI, Harnett W, Pinelli E. Allergy and Parasites. J Parasitol Research. 2013;2013:502562. doi:10.1155/2013/502562.
74. Cooper PJ, Barreto ML, Rodríguez LC. 2006. Human allergy and geohelminth infections: a review of the literature and a proposed conceptual model to guide the investigation of possible causal associations. Br Med Bull. 2006;80:203-18.
75. Flohr C, Quinnell RJ, Britton J. Do helminth parasites protect against atopy and allergic disease? Clin Exp Allergy. 2009;39:20-32.
76. van den Biggelaar A. Decreased atopy in children infected with Schistosoma haematobium: a role for parasite-induced interleukin-10. Lancet. 2000;356:1723-27.
77. Rujeni N. Atopy is inversely related to schistosome infection intensity: a comparative study in Zimbabwean villages with distinct levels of Schistosoma haematobium infection. Int Arch Allergy Immunol. 2012;158:288-98.
78. Araujo M. Inverse association between skin response to aeroallergen and Schistosoma mansoni infection. Int Arch Allergy Immunol. 2000;123:145-8.
79. Medeiros M. Schistosoma mansoni infection is associated with a reduced course of asthma. J Allergy Clin Immunol 2003; 111:947-51.
80. Araujo MI, de Carvalho EM. Human schistosomiasis decreases immune responses to allergens and clinical manifestations of asthma. Chem Immunol Allergy. 2006;90:29-44.
81. van den Biggelaar AH. Long-term treatment of intestinal helminths increases mite skin-test reactivity in Gabonese schoolchildren. J Infect Dis. 2004;189:892-900.
82. Flohr C. Reduced helminth burden increases allergen skin sensitization but not clinical allergy: a randomized, double-blind, placebo-controlled trial in Vietnam. Clin Exp Allergy. 2010;40:131-42.
83. Obihara CC, Beyers N, Gie RP. Respiratory atopic disease, Ascaris immunoglobulin E and tuberculin testing in urban South African children. Clin Exp Allergy. 2006;36:640-8.
84. Flohr C, Tuyen LN, Lewis S, et al. Poor sanitation and helminth infection protect against skin sensitization in Vietnamese children: a cross-sectional study. J Allergy Clin Immunol. 2006;118:1305-11.
85. Leonardi-Bee J, Pritchard D, Britton J. Asthma and current intestinal parasite infection. Am J Respirat Crit Care Med. 2006;174:514-23.
86. McKay DM. The therapeutic helminth? Trends Parasitol. 2008;24:1-6.
87. Weinstock JV. The possible link between de-worming and the emergence of immunological disease. J Lab Clin Med. 2002;139:334-8.
88. Weinstock JV. The worm returns. Nature. 2012;491:183-5.
89. Sabin EA, Araujo MI, Carvalho EM, Pearce EJ. Impairment of tetanus toxoid-specific Th1-like immune responses in humans infected with Schistosoma mansoni. J Infect Dis. 1996;173:269-72.
90. Cooper PJ, Espinel I, Paredes W, Guderian RH, Nutman TB. Impaired tetanus-specific cellular and humoral responses following tetanus vaccination in human onchocerciasis: a possible role for interleukin-10. J Infect Dis. 1998;178:1133-8.
91. He Y. The inhibitory effect against collagen-induced arthritis by Schistosoma japonicum infection is infection stage-dependent. BMC Immunol. 2010;11:28. doi:10.1186/1471-2172-11-28.
92. Cooper PJ, Chico M, Losonsky G, Espinel I, Sandoval C, Aguilar M. Albendazole treatment of children with ascariasis enhances the vibriocidal antibody response to the live attenuated oral cholera vaccine CVD 103-HgR. J Infect Dis. 2000;182:1199-206.
93. Cooper PJ, Chico M, Espinel I, Sandoval C, Guevara A, Levine M. Human infection with Ascaris lumbricoides is associated with suppression of the IL-2 response to recombinant cholera toxin B-subunit following vaccination with the live oral cholera vaccine CVD 103 HgR. Infect Immun. 2001;69:1574-80.
94. Elias D, Wolday D, Akuffo H, Petros B, Bronner U, Britton S. Effect of deworming on human T cell responses to mycobacterial antigens in helminth-exposed individuals before and after bacille Calmette-Guérin (BCG) vaccination. Clin Exp Immunol. 2001;123:219-25.
95. Macedo MS, Barbuto JAM. Murine delayed type hypersensitivity is suppressed by Ascaris suum extract. Braz J Med Biol Res. 1988;21:523-5.
96. Faqim-Mauro EL, Coffmann RL, Abrahamsohn IA, Macedo MS. Mouse IgG1 antibodies comprise two functionally distinct types that are differentially regulated by IL-4 and IL-12. J Immunol. 1999;163:3572-6.
97. Su Z, Segura M, Stevenson MM. Reduced protective efficacy of a blood-stage malaria vaccine by concurrent nematode infection. Infect Immun. 2006;74:2138-44.
98. Ghosh K, Wu W, Antoine A, Bottazzi ME, Valenzuela J. Hotez P, Mendez S. The impact of concurrent and treated Ancylostoma ceylanicum hookworm infections on the immunogenicity of a recombinant hookworm vaccine in hamsters. JID. 2006;193:155-62.
99. Haswell-Elkins MR. Cross-sectional study of Opisthorchis viverrini infection and cholangiocarcinoma in communities within a high-risk area in northeast Thailand. Int J Cancer. 1994;59:505-9.
100. Smout MJ. Infection with the carcinogenic human liver fluke, Opisthorchis viverrini. Mol Biosyst. 2011;7:1367-75.
101. Fried B, Reddy A, Mayer D. Helminths in human carcinogenesis. Cancer Lett. 2011;305:239-49.
102. Smout MJ. A granulin-like growth factor secreted by the carcinogenic liver fluke, Opisthorchis viverrini, promotes proliferation of host cells. PLoS Pathog. 2009;5:e1000611. doi:10.1371/journal.ppat.1000611.
Recibido: 20 de julio de 2015.
Aprobado: 11 de febrero de 2016.
Luis Fonte Galindo. Instituto de Medicina Tropical "Pedro Kourí", Autopista Novia del Mediodía Km. 61/2, La Lisa, Apartado postal 601, Marianao 13. La Habana, Cuba.
Correo electrónico: luisfonte@infomed.sld.cu