Producción y procesos productivos
Existe un grupo de premisas con diferente grado de exigencia como son:
- Dos grupos de productos al momento de su producción: no radiactivos y radiactivos.
- Instalaciones dedicadas.
- Producciones repetitivas de pequeños tamaños de lotes. Imposibilidad de aplicación del principio de producción en campañas.
- Necesidad de importar la materia prima isotópica y de realizar producciones competitivas.
Para los flujos de producción se partió de un enfoque que buscaba reducir al mínimo el riesgo de contaminación microbiana de los radiofármacos durante su fabricación. Para ello el proceso se diseña de modo que las etapas donde no se emplee material radiactivo tengan un peso específico muy alto dentro del flujo tecnológico y que, de esta forma, se minimicen las etapas que conlleven el uso de material radiactivo y, por tanto, el trabajo en instalaciones que no siempre cumplen con la clasificación establecida desde el punto de vista farmacéutico. Este enfoque ha demostrado ser pertinente, dado que el mercado no es grande y por tanto, tampoco los recursos financieros disponibles.
Equipamiento
]]> Existe en CENTIS un rango de equipos vinculados a los procesos productivos, algunos, específicos para la producción de radiofármacos. Son de tres tipos: de preparación de la producción, los directamente vinculados al proceso productivo y equipos de control de calidad. Se han aprobados procedimientos orientados a asegurar que cada equipo sea apropiado para su uso, fácil de operar y confiable. Un importante trabajo se ha desarrollado en las áreas de Aseguramiento Ingeniero para mantener en disposición operativa bajo condiciones de BPF equipos y dispositivos, devenidos obsoletos desde este punto de vista. Está establecido un programa de validación de acuerdo con las regulaciones nacionales, que se aplica fundamentalmente al equipamiento crítico. Una producción consistente y la calidad del producto van a depender de la confiabilidad y funcionamiento estable del equipamiento, lo que obliga a su validación durante la instalación y puesta en marcha, así como posteriormente a intervalos regulares. En las normativas internas se consigna cuándo, por quién y cómo se debe efectuar la validación y registrar los resultados. Asimismo, se tiene en cuenta el mantenimiento preventivo, la disposición de reservas de repuestos críticos, un protocolo de limpieza asociado al equipo y su uso. Los mantenimientos de todo tipo y la disposición de piezas de repuesto, constituyen un factor crítico que ha requerido de atención permanente en busca de alternativas viables, como la fabricación por medios propios.Componentes, envases y embalajes
La calidad del producto está directamente relacionada con los materiales que lo integran o que pueden entrar en contacto con él: ingredientes activos, vehículos, bulbos, tapones. De acuerdo con las BPF en CENTIS se dispone de procedimientos escritos con las especificaciones, compra, ensayos de aceptación, etiquetado, embalaje, almacenamiento y uso de estos insumos. Se consideran por separado a los efectos de un mayor rigor de atención. La baja concentración del componente activo en los radiofármacos obliga a seleccionar contenedores que no adsorban el producto radiactivo o interactúen con él, disminuyendo su pureza radioquímica.
Documentación
El registro del cumplimiento de las BPF, de la calidad del producto y de su control, de todo lo que tiene lugar en el proceso productivo es parte esencial del aseguramiento de la calidad. Lo que no se registra es como si no hubiera ocurrido, hay que hacer lo que está escrito y registrar todo lo que se hace. La documentación es vía principal para conocer si se siguen las BPF. Los elementos esenciales que conforman el sistema documental en CENTIS son: Manual y Política de Calidad, Procedimientos Normalizados de Operación (PNO) y Registro de lotes. La documentación sirve además, para que el colectivo comprenda cómo se organiza y lleva a cabo el proceso productivo, permite evaluar la trazabilidad y constituye la base para auditar este. Todo ello es ya práctica rutinaria en CENTIS.
Validación
Constituye una evaluación crítica del proceso de fabricación, entendido este como todas las operaciones que comprenden la adquisición de materias primas, materiales e insumos, producción, control de la calidad, liberación, almacenamiento y distribución de productos farmacéuticos y los controles relacionados con estas operaciones. De esa manera la validación es la acción documentada que demuestra que todo procedimiento, proceso, equipo, material, actividad o sistema realmente brinda los resultados esperados. Se trata pues, de un estudio sistemático para demostrar que el proceso dará lugar de manera consistente a los mismos resultados. Debe ser visto como un componente del diseño de la calidad del producto, diferente a los ensayos de calidad o la aprobación de las materias primas. Dentro de la organización productiva en CENTIS se dispone de un plan maestro de validación que comprende todos los aspectos señalados y el control de su ejecución.
Controles de laboratorio
Se refiere al establecimiento de especificaciones apropiadas, estándares de operación y metódicas, así como su control. En CENTIS cada lote de producción de radiofármacos es controlado desde el punto de vista de estándares establecidos de pureza radionuclídica, química y radioquímica, entre otros parámetros específicos de cada producto, como puede ser el tamaño de partículas. Los ensayos de esterilidad y pirógenos se llevan a cabo en el menor tiempo posible. Antes de liberar el lote se revisan los registros de producción y su correspondencia con las BPF, el análisis de las materias primas y otros factores que indiquen que los resultados están en conformidad con los requisitos establecidos.
]]> RESULTADOS
En relación con los procesos productivos CENTIS ha obtenido licencias de fabricación de:
- Generadores de
 -
-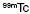
- Liofilizados para marcaje con
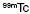
- Ioduro de Sodio marcado con
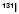 , solución oral
, solución oral - Fosfato de Sodio
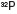 , inyección IV
, inyección IV - Iodobencilguanidina
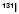 , inyección IV
, inyección IV - Fosfato Crómico marcado con
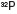 , suspensión para inyección IA
, suspensión para inyección IA - Cloruro de Itrio
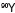 , precursor para marcaje
, precursor para marcaje
Muy relacionado con lo anterior, pero más específicamente asociado a la calidad y uso de radiofármacos, CENTIS ha obtenido el Registro Sanitario de los productos antes mencionados.
El Registro Sanitario es la autorización expedida por la autoridad reguladora para comercializar un medicamento de uso humano en determinado territorio, una vez evaluada como satisfactoria su calidad, seguridad y eficacia, así como las características de su fabricante. Proceso lento y costoso. La naturaleza de los radiofármacos y su mercado ha dado lugar a que en EE.UU. y Europa se discuta con frecuencia la necesidad de flexibilizar los requisitos para el registro de los radiofármacos. Se aluden dos razones principales: la vida en extremo corta de algunos de ellos, particularmente los usados en tomografía de emisión de positrones, y las bajas concentraciones del producto activo, cuya influencia en el orden toxicológico es en gran medida irrelevante [4,5]. Al mantenerse los mismos requisitos regulatorios para los radiofármacos que para los fármacos convencionales da lugar a que las firmas productoras evalúen con cuidado las inversiones y la recuperación de estas. El mercado de radiofármacos es especializado y no llega a competir con el de otros fármacos de uso necesariamente más extendido. Se insiste, por la experiencia adquirida, en que los tiempos de otorgamiento de registro se acorten y se revisen determinados requisitos que se consideran demasiado rígidos para el caso de los radiofármacos, en particular para los de uso diagnóstico. En relación con esto se aprecia una mayor flexibilidad en las regulaciones del órgano cubano, el Centro Estatal para el Control de la Calidad de Medicamentos (CECMED), sin detrimento del rigor que siempre lo ha caracterizado.
Proyección: productos e instalaciones
La etapa actual de CENTIS obliga a un salto de calidad en el cumplimiento de las BPF al poner énfasis de manera significativa en los radiofármacos terapéuticos, de particular cuidado en el proceso productivo e importancia actual [6]. En varios artículos de esta revista se hace referencia a esos radiofármacos. En el orden de las instalaciones se prevé a corto plazo la instalación de una celda clase A para la dosificación y la esterilización por filtración de los productos que no se pueden someter a esterilización por vapor. El enfoque esencial es sostener lo alcanzado y dar pasos para la certificación de un Sistema de Gestión de la Calidad.
CONCLUSIONES
CENTIS cuenta con un adecuado sistema de Buenas Prácticas de Fabricación de Radiofármacos resultado de 15 años de atención sistemática, creciente y calificada en correspondencia con las tendencias en el mundo, la jerarquía dada al tema en la institución y al papel de control, educación y ayuda continua del órgano regulador cubano, el CECMED. Ello está avalado, porque CENTIS tiene licenciados todos sus procesos productivos y registrados los productos que comercializa. Se dan las condiciones para pasar al establecimiento y certificación de un Sistema de Gestión de la Calidad.
]]> REFERENCIAS BIBLIOGRÁFICAS
1.- Centro para el Control Estatal de Medicamentos, Equipos y Dispositivos Médicos (CECMED). Directrices sobre Buenas Prácticas de Fabricación de Productos Farmacéuticos. Regulación 16-2012. La Habana: CECMED, .
2.- European Commission Enterprise and Industry Directorate-General. Consumer goods, Pharmaceuticals, Brussels, 25 October 2005. EudraLex, The Rules Governing Medicinal Products in the European Union Volume 4, EU Guidelines to Good Manufacturing Practice Medicinal Products for Human and Veterinary Use, Part I, Chapter 1 Quality Management.
3.- European Commission Enterprise and Industry Directorate-General. Consumer goods, Pharmaceuticals, Brussels, 10 October 2006 EudraLex, The Rules Governing Medicinal Products in the European Union Volume 4, EU Guidelines to Good Manufacturing Practice Medicinal Products for Human and Veterinary Use, Draft Annex 3, Manufacture of Radiopharmaceuticals.
4.- PASSCHIER J. Regulatory and Practical Considerations for Choosing the Right Synthesis Module. 15th European Symposium on Radiopharmacy and Radiopharmaceuticals. Scotland, UK, April 2010.
5.- SWANSON D, GRAM M, et al. Current Good Manufacturing Practice for PET Drug Products in the United States. J. Nucl. Med. 2009; 50(8): 26NH-28N.
6.- MURPHY PS, BERGSTROM M. Radiopharmaceuticals for oncology drug development: a pharmaceutical industry perspective. Curr. Pharm. Des. 2009; 15(9): 957-965.
]]> Recibido: 3 de septiembre de 2012
Aceptado: 4 de octubre de 2012 ]]>