Dra. Nereyda Martínez Suárez,1 Dra. Iraida Falcón Márquez,2 Dra. Marta Herrera Soto,2 Dra. Clara Gómez Cabrera,2 Dra. Ileana Agramonte Centelles,1 Dr. Adel Samara3 y Dr. Vladimir Villamil2
Exponemos nuestra experiencia en los primeros 100 casos, en los cuales utilizamos implantes orbitarios confeccionados en Cuba con hidroxiapatita porosa coralina (HAP-200), en el período comprendido entre 1995-2000. Nuestra casuística estuvo enmarcada entre los 5 y 65 años de edad, predominando los grupos de edades de 15 a 35 años con 63 casos, el 72 % correspondió al sexo masculino. Los traumatismos primaron como causa de pérdida del globo ocular (80 %). Efectuamos 5 tipos de técnicas quirúrgicas, 22 enucleaciones, 46 evisceraciones (26 con y 9 sin conservación corneal respectivamente, 11 con cuadrisección escleral) y 32 reconstrucciones de cavidades antiguas (implantes secundarios). En la mayoría de los pacientes operados los síntomas y signos posoperatorios fueron locales y catalogados de ligeros, que desaparecieron en la primera semana. Observamos dentro de las complicaciones 12 dehiscencias conjuntivales, 10 exposiciones de los implantes, 2 hipercorrecciones, 1 hipocorrección y 1 quiste conjuntival. La gammagrafía orbitaria demostró crecimiento fibrovascular en la totalidad de los pacientes sometidos a dicha investigación. Los resultados cosméticos evaluados fueron la conservación del surco orbitario y la motilidad del muñón que se consideraron satisfactorios, así como la tolerancia al material implantado que fue buena en el 93 % de los casos al cabo de los 2,5 años.
DeCS: IMPLANTES ORBITALES; IMPLANTACION DE LENTES INTRAOCULARES; PROCEDIMIENTOS QUIRURGICOS OFTALMOLOGICOS; HIDROXIAPATITAS/uso terapéutico; CIRUGIA PLASTICA; OJO ARTIFICIAL.
Hace más de 100 años que comenzaron a utilizarse los implantes orbitarios para tratar de lograr una mejoría cosmética en los pacientes que perdían el globo ocular, al restablecer en ellos el volumen de la cavidad y proporcionarles una mayor motilidad a las prótesis; los primeros consistían en esferas huecas de cristal y las utilizó Mülles en 1884.1,2
Desde entonces, la forma y su composición ha variado mucho, entre los materiales utilizados en su confección hemos tenido sustancias orgánicas (cartílagos, esclera, hueso de cabeza de fémur de recién nacido) e inorgánicas (cristal, tantalio, plástico, silicona y recientemente la hidroxiapatita y el pórex).3
Los implantes orbitarios se han clasificado en integrados y no integrados y en hundidos o expuestos. En 1941, Ruedmann introdujo un tipo de implante parcialmente expuesto que le proporcionaba gran motilidad a las prótesis, por lo cual tuvieron gran auge, pero muy pronto cayeron en desuso por el alto índice de infección y extrusión que presentaron.4,5
En 1985, el doctor Arthur C. Perry inició una investigación en Estados Unidos con implantes orbitarios confeccionados con hidroxiapatita, aprobándose en 1989 su utilización, con la que se obtuvo resultados satisfactorios.6,7
La hidroxiapatita es un complejo de fosfato de calcio que conforma la porción inorgánica del hueso humano (50 % del volumen normal del hueso),1 no es tratado por el organismo como una sustancia extraña y cuando se coloca en contacto con el hueso normal, este crece a través de sus poros.
En nuestro país, se logró obtener por el Centro Nacional de Investigaciones Científicas (CNIC) la hidroxiapatita porosa coralina (HAP-200) a partir de ciertos corales marinos, que se ha utilizado en varias especialidades como ortopedia, maxilofacial, periodoncia y neurocirugía desde 1990 con excelentes resultados.8
]]> Reportamos nuestra experiencia en los primeros 100 pacientes, en los cuales colocamos implantes orbitarios confeccionados con dicho material.Realizamos un estudio descriptivo observacional de reporte de casos en los primeros 100 pacientes a los cuales se les colocaron implantes orbitarios de HAP-200 en el período de 1995-2000 en el Servicio de Cirugía Oculoplástica del Hospital Oftalmológico Ramón Pando Ferrer. Se excluyeron de la utilización de este material a los portadores de sepsis ocular, de trastornos de la musculatura extrínseca, antecedentes de traumas orbitarios severos o de múltiples cirugías en cavidades anoftálmicas, las cuales presentaban cicatrices y/o fibrosis intensas.
En el examen oftalmológico preoperatorio se incluyó ultrasonido en aquellos ojos atróficos o con medios opacos para descartar la presencia de un tumor intraocular y biometría ultrasónica del ojo sano para calcular el tamaño del implante que se debía colocar de acuerdo con la tabla propuesta por el doctor Perry.2
Los implantes fueron suministrados por el Departamento de Biomateriales del CNIC, ya estériles en forma de esferas de 18, 19, 20 y 21 mm de diámetro, las que presentaban una estructura porosa tridimensional interconectada con poros y microporosidades de 200 y 5 micras respectivamente; estos se introdujeron en solución salina con antibiótico (gentamicina 80 mg o quemicetina 1 g) durante 30 min previo a su colocación.
Los procederes quirúrgicos se realizaron con anestesia peribulbar y sedación, reservando la general para las enucleaciones y los niños.
Las técnicas quirúrgicas empleadas fueron: enucleaciones, evisceraciones con y sin conservación corneal, implantes secundarios en cavidades anoftálmicas, siguiendo en todas ellas los procederes propuestos por el doctor Perry,9 además, se incorporó en el último año la técnica de evisceración y reconstrucción de cavidades antiguas con cuadrisección escleral.
En las enucleaciones y cavidades antiguas en las que se requirió forrar los implantes se utilizó fascia lata autóloga (35 casos) y esclera de banco (14 casos), a dichos forros se les realizaron 5 ventanas, una posterior de 10 mm y 4 anteriores de 3 x 2 mm en cuyos bordes anteriores fijamos los músculos rectos para favorecer el crecimiento fibrovascular dentro del implante. En el caso de las evisceraciones, la ventana posterior se situó temporal al nervio óptico y las anteriores entre los músculos rectos.
Al finalizar el acto quirúrgico se colocó pomada antibiótico-antiinflamatoria, conformador de acrílico y vendaje compresivo por 24 h, al cabo de las cuales se indicaron compresas frías y tratamiento antibiótico-antiinflamatorio local y sistémico por vía oral durante una semana, reservando la vía parenteral para los que presentaron síntomas moderados o intensos. El seguimiento fue diario en la primera semana y luego semanal durante los primeros 30 días, al cabo de los cuales los enviamos a los departamentos de somatoprótesis del CIMEQ o del Hospital Luis Díaz Soto para la confección de una prótesis individual; se continuaron evolucionando mensualmente hasta los 6 meses, a partir del 1er. semestre posoperatorio el seguimiento fue anual, si no existían eventos adversos.
Aquellos pacientes interesados en optimizar la motilidad protésica (para lo cual requerirían otro proceder quirúrgico) fueron sometidos a partir de los 6 meses del implante a un estudio gammagráfico en el Centro de Investigaciones Clínicas, utilizando Tecnecium-99 como isótopo radiactivo.
Se analizaron las variables siguientes: edad, sexo, causa de pérdida del globo ocular, técnicas quirúrgicas empleadas, tamaño de los implantes utilizados, signos y síntomas posoperatorios, complicaciones, resultados gammagráficos, evaluación cosmética y tolerancia al implante.
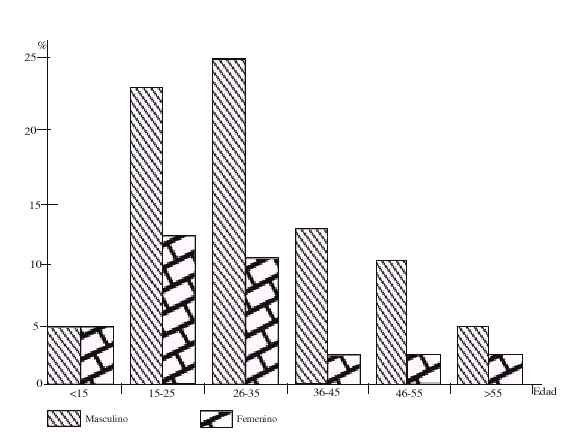
Nuestro universo estuvo conformado por 100 pacientes, 72 de los cuales correspondían al sexo masculino y 28 al femenino, cuyas edades estaban comprendidas entre los 5 y 65 años, predominando los grupos entre 15 y 35 con 63 casos (fig. 1).
Fig. 1. Distribución de los pacientes según edad y sexo.
La etiología traumática fue la que prevaleció con 80 casos (fig. 2).
Fig. 2. Distribución de pacientes por diagnóstico etiológico.
La técnica quirúrgica más realizada fue la evisceración (46 casos) (fig. 3) y el tamaño del implante más usado fue el de 18 mm (79 casos).
]]>
Fig. 3. Distribución de pacientes según las técnicas quirúrgicas.
En los 49 procederes en que hubo necesidad de forrar los implantes (22 enucleaciones y 27 cavidades antiguas) utilizamos esclera de banco en 14 y el resto se cubrió con fascia lata autóloga. Los síntomas y signos posoperatorios que se observaron fundamentalmente fueron locales como: dolor, edema palpebral, quemosis y secreción serohemática, catalogados de ligeros en la mayoría y que desaparecieron durante la primera semana (tabla).
Tabla. Distribución de los pacientes según signos y síntomas posoperatorios
| Síntomas y signos Dolor ocular | Días | ||
| < 4 | 4 - 7 | 8 - 15 | |
| Ausente | 9 | ]]> 56 | 72 |
| Ligero | 81 | 35 | 23 |
| Moderado-intenso | 10 | 9 | 5 |
| Edema palpebral Ausente | 15 | ]]> 27 | 65 |
| Ligero | 69 | 57 | 28 |
| Moderado-intenso | 16 | 16 | 7 |
| Quemosis Ausente | 31 | 44 | ]]> 71 |
| Ligero | 60 | 47 | 23 |
| Moderado-intenso | 9 | 9 | 6 |
| Secreciones Ausente | 48 | 55 | 69 |
| Serohemática | ]]> 52 | 45 | 24 |
| Mucopurulenta | 0 | 0 | 7 |
Las complicaciones que se presentaron fueron 12 dehiscencias conjuntivales con exposición del implante en 10 de ellas, 7 de las cuales evolucionaron a sepsis locales severas y en las que hubo que retirar las esferas de HAP-200, otras complicaciones fueron 2 hipercorrecciones, 1 hipocorrección y 1 quiste conjuntival (fig. 4).
Fig. 4. Distribución de los pacientes según las complicaciones.
En los 41 pacientes que se realizaron las gammagrafías orbitarias se comprobó en su totalidad un crecimiento fibrovascular adecuado dentro del implante.
]]> En la evaluación cosmética observamos conservación total del surco orbitario y motilidad del muñón mayor de 5 mm en 82 pacientes (fig. 5).Fig. 5. Paciente operada hace 3 meses. Se visualizaron movimientos amplios del muñón y aspecto final cosmético.
La tolerancia del implante fue satisfactoria en el 93 %. No observamos reacciones adversas a la hidroxiapatita.
En el estudio realizado utilizamos implantes orbitarios integrados de HAP-200 de producción nacional. Antiguamente al referirse a la propiedad de integración de un implante, quedaba implícito el hecho de fijar la musculatura extrínseca en el acto quirúrgico, actualmente se utiliza el término biointegrable valorando la propiedad del material empleado en su confección de permitir el crecimiento del tejido fibrovascular a través de él y así incorporarse como parte viviente del organismo.10
La mayoría de nuestros pacientes estaban enmarcados en los grupos de edades relacionados con una etapa laboral activa y la pérdida del globo ocular estuvo relacionada con traumatismo en el 80 % de ellos.
Las reconstrucciones de cavidades anoftálmicas colocando implantes secundarios fueron realizadas en 32 casos con una antigüedad entre 1 mes y 33 años; en los más recientes pudimos localizar fácilmente la musculatura extrínseca y el saco escleral, posibilitando el proceder, por el contrario en los más antiguos cuyas cavidades no estaban preparadas para dichos efectos se dificultó la maniobra, encontrándose algunos sacos esclerales atróficos o ausentes (enucleaciones previas), lo que motivó que la motilidad final obtenida en ellos fuera limitada (menor de 3 mm).
En el año 2002, fue introducida en nuestro servicio la técnica de cuadrisección escleral, con ella pudimos colocar implantes de tamaños adecuados en ojos atróficos y en sacos esclerales pequeños sin realizar tensión en las suturas, lo cual es de gran utilidad ya que una sutura que produzca tensión en los tejidos puede ser la causa de exposición de los implantes, además el área de contacto directo del implante con los tejidos orbitarios (polo posterior) con esta técnica es mayor, favoreciendo el crecimiento fibrovascular dentro de él; otra ventaja es que no necesitamos material ajeno para forrar la esfera.11
Los síntomas y signos posoperatorios fueron locales en la mayoría, y catalogados de ligeros y que desaparecieron después de la primera semana.
Las complicaciones fueron pocas y concordamos con lo referido en la literatura.12-15 Las dehiscencias conjuntivales observadas fueron 12, 3 de ellas superficiales y 9 profundas, apareciendo todas después de la segunda semana; una de las superficiales resolvió espontáneamente, las otras tuvimos que resuturarlas en el salón de operaciones; en cuanto a las profundas, en 2 hubo que colocar un parche de fascia lata autóloga y 7 evolucionaron a sepsis locales severas, no cediendo ante la antibioticoterapia impuesta por lo que tuvimos que extraer los implantes en estos casos; una vez realizada la extracción, los signos de inflamación y de secreción intensa desaparecieron rápidamente, lo cual atribuimos a un rechazo al material del forro del implante (esclera de banco) que habíamos utilizado en ellos y no a la hidroxiapatita en sí.
]]> Varios investigadores se han referido a la frecuencia relativa con que aparecen las exposiciones de estos implantes.15-21Por lo general, ocurre cuando el proceso de fibrovascularización no se ha concluido, al parecer la erosión de los tejidos puede ser asiento de colonizaciones bacterianas;9 se recomienda para evitar estas complicaciones seleccionar un implante adecuado, ya que los de gran tamaño impiden un cierre sin tensión; colocación profunda y envoltura con una capa de fascia o esclera para evitar que la HAP erosione la Tenon y la conjuntiva; además, realizar amplias ventanas para favorecer la vascularización y un cierre meticuloso por planos sin tensión.
En las 2 hipercorrecciones sustituimos los implantes por otros de menor tamaño y en el caso que apareció un quiste conjuntival, el cual era de 3 mm, lo resecamos sin otra complicación.
Se plantea que la hidroxiapatita completa su integración a los 6 meses,1 al respecto múltiples referencias internacionales se han reportado,22-24 en trabajos anteriores realizados por Pérez y otros,25 con la HAP-200 obtuvieron los mismos resultados. Nosotros confirmamos este crecimiento fibrovasculador en el interior de los implantes en 41 casos sometidos al examen gammagráfico orbitario. Esto nos permitirá la perforación de los implantes y la colocación de prótesis articuladas que no descansarían en los fórnices inferiores y le proporcionarán una mayor motilidad a la ectoprótesis, aunque nuestros pacientes, por lo general, se encuentran satisfechos con los resultados cosméticos obtenidos.
Por todo lo anterior concluimos que los implantes esféricos biointegrales confeccionados con HAP-200 han sido utilizados en diferentes técnicas quirúrgicas, con los que obtuvimos excelentes resultados con un bajo índice de complicaciones y una elevada tolerancia a dicho material y que con estos implantes no sólo restauramos el volumen perdido de la cavidad, sino que le imprimimos una mayor motilidad a las prótesis oculares y así aumentamos el grado de satisfacción desde el punto de vista cosmético de los pacientes anoftálmicos.
Por los resultados positivos obtenidos con este bioimplante de HAP-200 (Coralina), producido en Cuba, creemos que debe ser extendida su aplicación al resto de las unidades de asistencia oftalmológica de nuestro país como un método novedoso y de gran valor para mejorar la calidad de vida desde el punto de vista estético de los pacientes portadores de prótesis oculares.
We explain our experience with the first 100 cases in whom orbital implants made in Cuba with coralline porous hydroxyapatite (PHA-200) were placed between 1995 and 2000. Our casuistics comprised patients aged 5-65. It was observed a predominance of the age groups 15-35 with 63 cases. 72 % were males. Traumas prevailed as the main cause of eyeball loss (80 %). 5 types of surgical techniques were performed: 22 enucleations, 46 eviscerations (26 with and 9 without corneal conservation, respectively, 11 with scleral cuadrisection) and 32 reconstructions of old cavities (secondary implants).The postoperative symptoms and signs were local and mild in most of the patients that were operated on and they disappeared during the first week. 12 conjunctival deshicences, 10 implant exposures, 2 hypercorrections, 1 hypocorrection and 1 conjunctival cyst were observed among the complications. The orbital scintigraphy showed fibrovascular growth in all the patients under study. The evaluated cosmetic results were the conservation of the orbital sulcus and the motility of the strump that were considered as satisfactory, as well as the tolerance to the implanted material that was good in 93 % of the cases after 2.5 years.
Subject headings: ORBITAL IMPLANTS; LENS IMPLANTATION, INTRAOCULAR; OPHTHLAMOLOGIC SURGICAL PROCEDURES; HYDROXYAPATITES/therapeutic use; SURGERY, PLASTIC; EYE, ARTIFICIAL.
1. Dutton J. Hydroxyapatite as an ocular implant. Opthalmology 1991;98(3):370-7.
2. Perry C. Advances in enucleation. Ophthalmol Clin North Am 1991;4(1):173-82.
3. Jordon DR, Allen LH, Ells A, Gilberg S, Browasteins S, Munro S. The use of vycril mesh (poliglacten 910) for implantation of hydroxyapatite orbital implants. Ophthalmol Plast Reconstruc Surg 1991;11(2):95-9.
4. Shields C, Shields JA, De Potter P. Hydroxyapatite orbital implant after enucleation. Experience with initial 100 consecutive cases. Arch Ophthalmol 1992;100:333-8.
5. Shields JA, Shields C, De Potter P. Hydroxyapatitie orbital implant after enucleation. Experience with 200 cases. Mayo Clin Proc 1993;68:1191-5.
6. Shields C, Shields JA, Eagle RC, De Potter P. Histopathologic evidence of fibrovascular ingrowth four weeks after placement of the hydroxyapatite orbital implant. Am J Ophthalmol 1991;111:363-6.
7. Leitha T, Stoudnherz A, Schaly U. Three-phase bone scintigraphy of hydroxyapatite ocular implants. Eur J Nucl Med 1995;22(4):308-14.
8. González Santos R, Guerra-López García J. Materiales biorreactivos para implantes óseos. Características y aplicaciones. Laboratorio de Biomateriales. Centro Nacional de Investigaciones Científicas. 1992:10-38.
9. Boy BF. Atlas de Cirugía Ocular. Ciudad de Panamá: Highlights of Ophthalmology; 1996: 262-5. (World Atlas Series)
10. Murry WR, Heiny GW; Bonnin JM, Martin R. Cepela MA. Exposure rate of hydroxyapatite spheres in the anophthalmic socket: histopathologic correlation and comparison with silic sphere implants. Ophthalmic Plast Reconstruct Surg 1993;9(2):96-104.
11. Yang JG, Khmang S, WeeWon R, Kin DM, Di Jin H. Hydroxyapatite implantation with scleral cuadrisection after evisceration. Ophthalm Surg Lasers 1997;28(11):915-9.
12. Christmas NJ, Gordon CD, Murray TG, Tse D, Jhonson T, Garonzik S. Intraorbital implants after enucleation and their complications: a 10 years review. Arch Ophthalmol 1998;116(9):1199-203.
13. Kostick DAA, Lensberg JV. Evisceration with hydroxyapatite implant surgical technique and review of 31 cases reports. Ophthalmology 1985;102(10):1548-9.
14. Jordan DR, Browestein S, Jolly SS. Abscessed hydroxyapatite orbital implants. A report of two cases. Ophthalmology 1996;103(11):1784-7.
15. El Shohed Fansi S, Sherif. Magdi M, Ali Ahmed T. Management of tissue breakdown and exposure associated with orbital hydro-xyapatite implants. Ophthalmol Plast Reconstruct 1995;11(2);91-4.
16. Goldberg RA, Holds JB, Ebrahimpour J. Exposed hydroxyapatite orbital implants. Report of six cases. Ophthalmology 1992;99(5):831-6.
17. Kim YD, Goldberg RA, Shors M, Steinsaper KD. Management of exposed hydroxyapatitie orbital implants. Ophthalmology 1994;101(10):1709-15.
18. Destreicher JH. Treatment of exposed coral implant after failed scleral patch graft. Ophthalmol Plast Reconst Surg 1994;10(2):110-3.
19. Kaltreider SA, Newman SA. Prevention and management of complications associated with the hydroxyapatite implants. Ophthalmol Plast Reconst Surg 1996;12(1):18-31.
20. Destreicher JH, Liv E, Berkowitz M. Complications of hidroxiapatite orbital implants. A review of 100 consecutive cases and a comparison of Dexon mesh (poliglycolic acid) with scleral wrapping. Ophthalmology 1997;104(2):324-9.
21. Pondya AD, Rich C, Eifreg DE, Manfred J, Recffer RL. Experimental evolution of hydroxyapatite reservoir tube sheent of rabbits. Ophthalmic Surg Laser 1996;27(4):308-14.
22. Civelek AC, Pacheco EM, Natarajan JK, Wagner HM, Iliff NT. Quastitative measurement of vascularization and vascular ongrowth rate of coralline hydroxyapatite ocular implants by Tc-99 MDP bone meageng. Clin Nucl Med 1995;20(9):779-87.
23. Menzel C, Grunwald F, Busin M, Monks T, Schonberg AP. Vascularization of ocular coralline hydroxyapatite implants. Eur J Nucl Med 1994;21(12):1343-5.
24. Numerow LM, Kloiber R, Mitchell RJ, Malnar CR, Anderson MA. Hydroxyapatite orbital implants. Scanning with tech...? 99. Clin Nucl Med 1994;19(1):9-12.
25. Pérez Blázquez G, González Santos R, Acosta Díaz L, Solano Bravo ME, Oliva Acosta J. Hidroxiapatita porosa coralina HAP-200 como implante esférico integrado en el onaftalino quirúrgico. Rev Cubana Oftalmol 1998;11(1):5-13.
Recibido: 7 de junio de 2001. Aprobado: 31 de agosto de 2001.
Dra. Nereyda Martínez Suárez. Hospital Oftalmológico Docente Ramón Pando Ferrer, Ciudad de La Habana, Cuba.
1 Especialista de II Grado en Oftalmología. Instructora.
2 Especialista de I Grado en Oftalmología.
3 Residente de 2do. año de Oftalmología.