
Iván E. Cuevas
Instituto Finlay. Centro de Investigación-Producción de Vacunas. Ave. 27 No.19805. La Lisa. A.P. 1601 C.P. 11600,
Ciudad de
Se realizó un estudio sobre los problemas de la vigilancia poscomercialización desde la industria farmacéutica. Las reacciones adversas a medicamentos y vacunas causan un aumento significativo en los costos de la atención sanitaria; las vacunas en particular tienen un beneficio diferido y desconocido y un riesgo inmediato, por lo cual se requiere de mayores estándares de vigilancia. La farmacovigilancia por sí misma tiene obstáculos que pueden ser mayores cuando se enfocan desde la industria farmacéutica. El acompañamiento o apadrinamiento como estrategia permite vencer esos obstáculos y establecer el sistema de vigilancia poscomercialización, lo cual ha sido práctica sistemática del Instituto Finlay y es la concreción de cómo se debe asumir un mayor nivel de responsabilidad en los productos con el ciclo completo. La experiencia en nuestro Instituto con relación al enfoque poscomercialización, donde se observan todos los factores y condiciones que inciden en efectos deseados o no de los productos, es un adelanto para que con la aplicación de herramientas epidemiológicas y farmacoeconómicas, obtener una mejor evaluación del impacto sanitario y económico en la aplicación de nuestras vacunas. La implementación y puesta en marcha de la farmacovigilancia en la industria de medicamentos es un desafío y una necesidad para completar el desarrollo de la industria farmacéutica.
Palabras clave: Vacunas, farmacovigilancia, eventos adversos.
Introducción
Entender el riesgo asociado al uso de medicamentos, medirlo y sopesar sus consecuencias, puede ser un catalizador de la industria farmacéutica, parafraseando a Bernstein (1).
La farmacovigilancia surge luego de la epidemia de focomelia causada por la talidomida en 1961, y se ha convertido en una herramienta decisiva de la industria de medicamentos y la salud pública (2).
]]> Es una actividad destinada a la identificación, evaluación y prevención de los riesgos asociados a los medicamentos en la fase IV del desarrollo farmacéutico (3).Para poder cumplir con los objetivos de la vigilancia poscomercialización, las industrias de medicamentos, las autoridades sanitarias y las agencias reguladoras de medicamentos deben tener un intercambio fluido de informaciones (4), porque la gerencia de los sistemas de vigilancia está en manos de las autoridades sanitarias y no en la industria farmacéutica.
La atención está dirigida a observar el impacto de los medicamentos y de las vacunas en la población, con el objetivo de emprender las acciones que permitan mantener la relación riesgo-beneficio de estos; es una situación favorable, es decir, debemos ajustar la prescripción y anotar las contraindicaciones de uso en grupos especiales, o bien suspender su uso cuando esto no sea posible (3).
Luego de la introducción de un nuevo medicamento de uso general, la metodología principal para los estudios de seguridad es la observación y se utilizan datos del examen de los pacientes tratados en la práctica clínica más bien que de la experimental (donde están los datos de mucho más alta calidad, con un control mejor de los factores de confusión).
El uso del medicamento brinda a los profesionales de la industria farmacéutica la oportunidad de explorar el funcionamiento y la adherencia de la población especial a la droga nueva y la observación de acontecimientos adversos especiales (como las reacciones adversas tipo B) solo detectables con una experiencia durante la práctica clínica rutinaria y en estudios de muestras poblacionales mayores.
La maestría en farmacoepidemiología es ahora un deber para cualquier compañía farmacéutica, por lo que muchos han establecido proyectos de investigación colaborativos con instituciones académicas dedicadas al tema.
El objetivo de este artículo es mostrar el enfoque de la vigilancia poscomercialización desde la industria farmacéutica, y específicamente se describe cómo se manifiesta en el Instituto Finlay.
¿Por qué la farmacovigilancia es parte del desarrollo del producto?
La información recolectada en las fases previas al registro no basta para perfilar la seguridad de los medicamentos y las vacunas, pues es obtenida sobre muestras relativamente pequeñas y una selectiva recolección de datos en un tiempo limitado y fuera de la práctica clínica habitual (5, 6). La biografía del producto se inicia con el registro y se concreta en la fase IV del desarrollo del fármaco (6,7), durante el cual se detectan eventos adversos raros y el efecto de interacciones o condiciones clínicas coexistentes (8, 9).
Las diferencias existentes entre los diseños de estudio de la fase III y IV (Cuadro 1), fundamentan la desigual sensibilidad en la detección de eventos adversos.
Cuadro 1: Diferencias entre el uso de medicamentos en los ensayos clínicos Fase III y los estudios observacionales de práctica clínica habitual en fase IV.
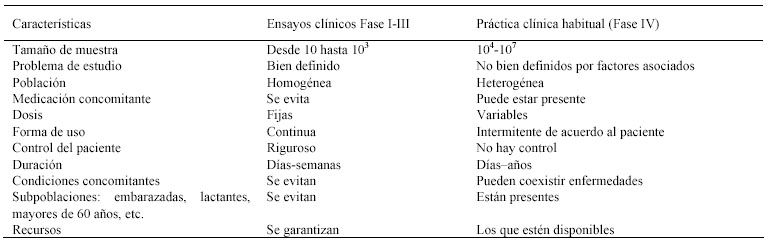
Fuente: Modificado de (7, 10).
Los datos obtenidos por una consistente farmacovigilancia permiten estimar la incidencia de las reacciones adversas, el balance entre el beneficio y el daño, las comparaciones con tratamientos alternativos y predecir las consecuencias en caso de que un medicamento sea utilizado en grupos especiales (11, 12).
Situación actual de la industria farmacéutica
Vista desde la industria farmacéutica esta actividad permite que se cumpla el principio de la bioética: primum non nocere. Solo así se podrá proteger a los usuarios de sus productos mediante la pronta identificación de riesgos propios del medicamento, detección de factores predisponentes, descubrir errores programáticos, descartar falsas señales, estimar la causalidad por medio de algoritmos y cuantificar la magnitud del riesgo con relación al beneficio (4, 6 y 13).
La utilización de vacunas es un caso especial, por tener un beneficio diferido y desconocido; mientras su riesgo es inmediato (14). Son administradas a niños sanos dentro de los programas nacionales (5, 15, 16), precisan de un excelente perfil de tolerancia y sistemas de monitoreo con el mayor estándar de desempeño.
Ejemplos de la utilidad de la farmacovigilancia en vacunas son los siguientes (Cuadro 2).

Procedimientos empleados
Se define como evento o experiencia adversa a cualquier acontecimiento médico inconveniente que se presente durante el tratamiento con un medicamento o vacuna, el cual no tiene necesariamente una relación causal con este tratamiento.
Las prácticas empleadas son varias: notificación de eventos adversos, para una posterior evaluación clínica y detección de señales. Pueden ser obtenidos de fuentes diversas como: reporte espontáneo, artículos publicados, búsqueda de casos entre ingresos hospitalarios, estudios analíticos observacionales (de caso-control y de cohorte), estudios correlacionales de cambios en la mortalidad y/o mortalidad ante cambios en consumo (o prescripción) de ciertos medicamentos y los ensayos clínicos de productos; cada uno de estos tipos de estudios con sus ventajas y sus desventajas (34).
El sistema de reporte espontáneo no permite por sí mismo medir el riesgo; sin embargo es sencillo, sensible, su bajo costo y fácil extensión a nivel nacional, admite que se confeccionen bases de datos para la búsqueda de un nuevo conocimiento (minería de datos), se detecten nuevas señales, que por su gran utilidad en la detección de sospechas de reacciones adversas se ha convertido en el sistema más universalmente aceptado en la farmacovigilancia (34).
Las pautas de armonización internacionales sugieren la necesidad de instaurar la transmisión electrónica de reportes de casos entre todas las partes (fabricantes, direcciones sanitarias y agencias reguladoras) y la conformación de bases de datos para lograr una mejor retroalimentación del sistema de farmacovigilancia. Ello constituye el real y actual desafío de la farmacoepidemiología, vista desde la industria farmacéutica (4,6).
Magnitud del problema
Si se tiene en cuenta que sólo entre el 2% y el 5% de todos los eventos adversos son notificados a través de los sistemas de reporte espontáneos, lo cual puede llegar hasta un 10% y un 20% en centros con un buen desempeño (35, 36), y se sabe que además de su impacto en la salud humana dejan una huella significativa en la calidad de la vida, los costos de la atención sanitaria, por el aumento en la estadía hospitalaria y los recursos humanos y materiales necesarios para su tratamiento (37), comprenderemos la complejidad de los estudios de farmacovigilancia.
Datos disponibles sitúan a las reacciones adversas entre el 3% y el 7% de todas las admisiones hospitalarias (38, 39), de las cuales más de la mitad no son reconocidas al momento del ingreso.
]]> En un estudio, donde el 6,5% de los pacientes hospitalizados había tenido un evento adverso, se estima que el 28% de ellos podían haberse evitado (40).Se calcula que más de un millón de norteamericanos fueron ingresados en 1994 debido a eventos adversos, acumulando más del 4,7% de todos los ingresos. Estimados anuales sitúan ese diagnóstico en entre el 5% y el 35% de consultas externas (41).
Entre la mitad y la tercera parte de los fallecimientos inducidos en Estados Unidos por el uso de un medicamento pueden evitarse (42, 43), y está entre la cuarta y la sexta causa de muerte en los hospitales (44).
En otros estudios se plantea que la mortalidad hospitalaria por reacciones adversas está en una frecuencia de 15/1000 ingresos hospitalarios (45).
En general, la carga económica de la morbilidad y la mortalidad por esta causa se ha estimado entre 30-
Obstáculos en la farmacovigilancia
Al instaurar la farmacovigilancia se han detectado obstáculos en diferentes escenarios que pueden ser mayores cuando se enfocan desde la industria de medicamentos, ejemplo de los cuales se muestran en el Cuadro 3.
Cuadro 3. Obstáculos básicos para la instauración de la farmacovigilancia (46)


Estrategia de la farmacovigilancia aplicada en el Instituto Finlay
En Cuba la biotecnología asume las Buenas Prácticas en el desarrollo, producción y distribución de medicamentos, y el enfoque de calidad total con una atención centrada en el usuario final.
La preferencia por la sistemática valoración del impacto de los productos por la industria farmacéutica y las autoridades sanitarias es la mejor estrategia para vencer la inercia que se presenta en el establecimiento de los sistemas de vigilancia poscomercialización.
Entre las acciones llevadas a cabo por el Instituto Finlay en esta línea de trabajo y que sirven de ejemplo, tenemos las siguientes:
· Creación del Grupo Operativo para el Control de
· Actualización del Programa de Prevención y Control de Síndromes Neurológicos Infecciosos (57).
· Patrocinio y participación en el capítulo de Infectología de
· Participación en comisiones y supervisiones integrales convocadas por el Centro Estatal para el Control de los Medicamentos referidas al tema de vacunas.
· Estudio de clúster de casos sospechosos de enfermedad meningocócica (58, 59), y de eventos adversos a la vacuna antitifoídica de polisacárido Vi.
]]> · Estudio descriptivo retrospectivo de eventos adversos a la vacuna antimeningocócica B y C en municipios de Ciudad de La Habana (60).· Evaluación de la cadena de frío para la conservación de las vacunas del programa de inmunizaciones y otros biológicos.
Estas acciones son una referencia de cómo se debe asumir un mayor nivel de responsabilidad por los productos en las industrias y centros con el ciclo completo de investigación-desarrollo-producción de medicamentos, y es un ejemplo de lo que significa el término acompañamiento de los productos (61).
La instauración de la farmacovigilancia desde el Instituto Finlay ha sido posible gracias a la colaboración con el Centro de Desarrollo de Farmacoepidemiología, pues las industrias de medicamentos no tienen acceso al sistema de recopilación de notificaciones. Con esto se logra que la institución se beneficie con los datos, mientras las autoridades sanitarias se benefician con recibir un enfoque analítico más detallado de problemas particulares de los medicamentos y biológicos utilizados en las diferentes instancias del sistema de salud.
La capacitación de los profesionales de la asistencia sanitaria para completar un mejor uso de los productos y el asumir una propia estrategia para la farmacoepidemiología en el Instituto Finlay es una contribución al desarrollo de la salud pública en tanto maquinaria social que asegurará a cada individuo en la comunidad un nivel de vida adecuado para el mantenimiento de la salud (62).
Conclusiones
Ante los desafíos de nuevas enfermedades y la reemergencia de las viejas, el fortalecimiento de la farmacovigilancia permitirá a las autoridades sanitarias acortar los plazos de aprobación del Registro Médico Sanitario para los nuevos medicamentos, por la seguridad que aportan los sistemas de vigilancia poscomercialización.
El incremento de nuevos productos farmacéuticos en Cuba y en otras regiones del mundo, es una motivación adicional para completar la información de seguridad de nuestros productos en
Referencias
1. Bernstein PL. Against the gods: the remarkable story of risk. John Wiley and Sons, New York, 1996.
2. The Uppsala Monitoring Centre Chapter 2. A short history of involvement in drug safety monitoring by WHO. En:The Uppsala Monitoring Centre. The Importance of Pharmacovigilance (Safety monitoring of medicinal products). World Health Organization, Geneva; 2002:5-8.
3. De Abajo FJ, Montero D, Madurga M, et al. Análisis y gestión de riesgos en Farmacovigilancia. Organización de la Farmacovigilancia en España. En: El ensayo clínico en España (García AG y Gandía L, eds). Farmaindustria, Madrid, 2000:191-216.
4. Talbot JCC, Nilsson BS. Pharmacovigilance in the pharmaceutical industry. British Journal of Clinical Pharmacology 1998; 45:427-431.
5. ISDB Declaration on therapeutic advance in the use of medicines. Paris 15-16 November 2001. Disponible en: http://66.71.191.169/isdbweb/pdf/Berlin_Declaration_on_Pharmacovigilance_January_2005.(pdf), accedido 18 de junio 2006.
6. The Uppsala Monitoring Centre. Chapter 4. Pharmacovigilance in drug regulation.En:The Uppsala Monitoring Centre. The Importance of Pharmacovigilance (Safety monitoring of medicinal products). World Health Organization, Geneva 2002:15-23.
7. Furones Mourelle JA. Bases científicas para el desarrollo y la utilización de los medicamentos. En: Morón FJ y Levy M. Farmacología General. Editorial Ciencias Médicas. La Habana, 2002: 9-21.
8. Trontell A. Expecting the unexpectedDrug safety, pharmacovigilance and the prepared mind. New England J Med. 2004;351(14):1385-87.
9. Dainesi SM. Pharmacovigilance: More Than Ever, An Overall Responsibility. Clinics 2005;60(4):267-70.
10. Sasich LD, Lurie P, Wolfe SM. The Drug Industrys performance in finishing post-marketing research (Phase IV) studies. Disponible en: http://www.citizen.org/hrg/Publications/1520.htm, accedido 20 junio 2006.
11. Waller PC, Evans SJW: A model for the future conduct of pharmacovigilance. Pharmacoepid. Drug Safety 2003; 12:17-29.
12. Reducing medication errors requires a multifactorial approach: Drugs Ther. Perspect. 2004; 20 (8): 22-5.
13. Benefit-risk balance for marketed drugs. Evaluating safety signals: Report of CIOMS working group IV. CIOMS, Geneva. 1998.
14. Autret-Leca É, Jonville-Béra AP, Beau-Salinas F. Pharmacovigilance des vaccins. La Revue du Practicien 2004; 54:526-531.
15. Immunization safety surveillance: Guidelines for managers of immunization programmes on reporting and investigating adverse events following immunization. Immunization Focus: WHO Regional Office for the Western Pacific. Manila. WHO 1999.
16. Global programme for vaccines and immunization: Expanded Programme on Immunization. Surveillance of adverse events following immunization: Field guide for managers of immunization programmes. Geneva: WHO, 1997.
17. National Institutes of Health "Task Force on Safer Childhood Vaccines: Final report and recommendations" Disponible en: www.niaid.nih.gov/publications/Vaccine/pdf/safevacc.pdf, accedido 14 de Julio 2006.
18. Nathanson, N.; Langmuir, A.D. The Cutter incident. American Journal of Hygiene 1963; 78:16-81.
19. Chen, R.; Knoebel, H.; Glasser, J.; et al. Investigation of sudden unexplained infant deaths following DTP-OPV-HBV vaccinations. Taiwan, 1990-92 (abstract). Postmarketing Surveillance 1993; 7:194.
20. Tuttle, J.; Chen, R.T.; et al. The risk of Guillain-Barre syndrome after tetanus-toxoid-containing vaccines in adults and children in the United States. Am J Public Health. 1997 Dec;87(12):2045-8
21. Terracciano, G.; Chen, R.T.; Schoenberger, L.; et al. Investigation of a rare vaccine-associated adverse event, GBS, using hospital discharge data in a retrospective cohort study (abstract). Pharmacoepidemiology and Drug Safety. 1997; 6:S62.
]]>22. Simon PA, Chen RT, Elliott JA, Schwartz B. Outbreak of pyogenic abscesses after diphtheria and tetanus toxoids and pertussis vaccination. Pediatric Infectious Disease Journal. 1993;12:368-371.
23. Gale JL, Thapa PB, Wassilak SGF, et al. Risk of serious acute neurological illness after immunization with DTP vaccine: a population based case-control study. Journal of the American Medical Association 1994; 271:37-41
24. Davis RL, Marcuse E, Black S, Shinefield H, et al. MMR2 at 4 to 5 years and 10 to 11 years of age: a comparison of adverse clinical events after immunization in the Vaccine Safety Datalink project. Pediatrics. 1997;100(5):767-771.
25. Black S, Shinefield H, Ray P, Lewis E, Chen R, Glasser J, et al. Risk of hospitalization because of aseptic meningitis after measles-mumps-rubella vaccination in one-to two-year-old children: an analysis of the Vaccine Safety Datalink (VSD) project. Pediatric Infectious Disease Journal. 1997; 16:500-503.
26. Griffin MR, Taylor JA, Daugherty JR, Ray WA. No increased risk of invasive bacterial infection found following DTP immunization. Pediatrics 1992; 89:640-642.
27. Ray P, Black S, Shinefield H, Dillon A, Schwalbe J, Holmes S, Hadler S, Chen R, et al. Risk of chronic arthropathy following rubella vaccination. Journal of the American Medical Association 1997; 278: 551-556.
28. Rosenthal S, Chen R, Hadler SC. The safety of acellular pertussis vaccine versus whole cell pertussis vaccine: a post-marketing assessment. Archives of Pediatrics and Adolescent Medicine. 1996; 150:457-460.
29. Comité de Vacunas SLIPE. Capítulo 8: Vacunaciones no sistemáticas:Anti-rotavirus. En: SLIPE. Manual de vacunas de Latinoamérica. Madrid Edicion 2005: 298-303
30. Parashar UD, Hummelman EG, Bresee JS, Millar MA, Glass RI. Global illness and deaths caused by rotavirus disease in children. Emerg Infect Dis. 2003; 9(5): 565-72
31. Gangarosa EJ, Galazka EJ, Wolfe CR, Phillips LM, Gangarosa RE, Mi Chen E. Impact of anti-vaccine movements on Pertussis control: the untold story. Lancet 1998; 351:356-61.
32. Wise RP, Kiminyo KP, Salive ME. Hair loss alter routine immunizations. JAMA. 1997; 278:1176-1178.
33. Strebel, P.M.; Sutter, R.W.; Cochi, S.L.; et al. Epidemiology of poliomyelitis in the United States one decade after the last reported case of indigenous wild virus-associated disease. Clinical Infectious Diseases 14(2):568-579; 1992.
34. Zapata A. Farmacovigilancia. En: Morón FJ y Levy M. Farmacología General. Editorial Ciencias Médicas. La Habana, 2002: 139-146.
35. Lazarou J, Pomeranz BH, Corey PN: Incidence of adverse drug reactions in hospitalized patients: a metaanalysis of prospective studies. JAMA 1998; 279:1200-5
36. Schneeweiß S, Hasford J, Göttler M, et al.: Admissions caused by adverse drug events to internal medicine and emergency departments. Europ. J. Clin. Pharmacol. 2002; 58:285
37. Gautier S, Bachelet H, Bordet R, Caron J.The cost of adverse drug reactions. Expert Opin Pharmacother. 2003 Mar;4(3):319-26.
Bouajordet I, Ebbesen J, Eriksen J, et al.: Fatal adverse drug events. J. Intern. Med. 2001; 250: 327
38. Pirmohamed M, James S, Meakin S, et al.: Adverse drug reactions as cause of admision to hospital: Prospective analysis of 18820 patients. BMJ 2004; 329: 15-9
39. International Society of Drug Bulletins EU: Berlin Declaration on Pharmacovigilance; January 2005:1-28. Disponible en: http://www.icf.uab.es/informacion/boletines/ISDB/Declaration.pdf accedido por última vez 15 de junio de 2006
40. Gandhi TK, Weingart SN, Borus J, et al.: Adverse drug events in ambulatory care. N. Engl. J. Med. 2003; 348: 1556-64
41. Gurwitz JH, Field TS, Harrold LR. et al.: Incidence and preventability of adverse drug events among older persons in the ambulatory setting. JAMA 2003; 289: 1107-16
42. Bates DW, Cullen DJ, Laird N, et al.: Incidence of adverse drug events and potential adverse drug events. JAMA 1995; 274: 29-34
43. White TJ, Arakelian A, Rho JP.Counting the costs of drug-related adverse events. Pharmacoeconomics. 1999 May;15(5):445-58.
44. Wayne AR: Population-based studies of adverse effects. N. Engl. J. Med. 2003; 349: 1592-4
45. Classen DC, Pestotnik SL, Evans RS, et al: Adverse drug events in hospitalized patients. JAMA 1997; 277: 301-6.
46. Obstacles To Pharmacovigilance. En: International Society of Drug Bulletins EU: Berlin Declaration on Pharmacovigilance January 2005:10-17.
47. Chan AW, Hróbjartsson A, Haahr MT, et al.: Empirical Evidence of Selective Reporting of Outcomes in Randomized Trials. JAMA 2004; 291: 2457-65.
48. Garland, E.J.: Facing the evidence: antidepressant treatment in children and adolescents. CMAJ 2004; 170: 489-91.
49. Medawar C, Hardon A, Herxheimer A. Depressing research. Lancet 2003; 363:2087.
50. Altman OF, Clancy C, Blendon RJ. Improving patient safety Five years after the IOM Report. New Engl J Med. 2004;351(20):2041-43.
51. Bates DW, Evans RS, Murff H, et al.: Detecting adverse events using information technology. J. Am. Med. Inform. Ass. 2003; 10:115-28.
52. Hauben M: Early Postmarketing Drug Safety Surveillance: Data Mining Points to Consider. Ann. Intern. Med. 2004; 38:1625-30.
53. Medicines Act 1968 Advisory Bodies: Annual Reports 2002. MHRA. London, 2003.
54. The Uppsala Monitoring Centre, WHO Collaborating Centre for International Drug Monitoring: The Importance of Pharmacovigilance, 2002.
55. The Uppsala Monitoring Centre, WHO Collaborating Centre for International Drug Monitoring: Safety monitoring of medicinal products, 2000.
56. Biriell C, Edwards JR. Reasons for reporting adverse drug reactions--some thoughts based on an international review.: Pharmacoepidemiol Drug Safety 1997; 6: 21-6.
57. Quintana I, Sotolongo F, Llop A, Cuevas I, Martínez N, Velásquez JC, Alvarez R, Martínez E, Tamargo I, Pérez A, Martínez I, Leiva T. Programa Nacional de Prevención y Control de Síndromes Neurológicos Infecciosos. Editores: Raúl Pérez, Manuel Santín, Ibrahin Quintana. Ministerio de Salud Pública, Dirección Nacional de Epidemiología, Ciudad de La Habana, Agosto de 1999.
58. Camaraza MA, Ochoa R, Arnet AG, Sotolongo F, Martínez I, Cuevas I. Assessment of immune response against C11 (ATCC) strain induced by Cuban meningoccocal vaccine (VA-MENGOC-BC®) in adolescents of Ciego de Avila, Cuba. En: Proceedings of 13th International Pathogenic Neisseria Conference, Norwegian Institute of Public Health, Oslo, Norway; Sept.1-6, 2002.
59. Camaraza MA, Ochoa R, Sotolongo F, Martínez I, Cuevas I. Inmunogenicidad inducida por la vacuna antimeningocócica VA-MENGOC-BC® contra la cepa de N. meningitidis ATCC C11 en adolescentes después de 12 años de vacunados. Rev Cubana Med Trop. 2004;56(1):26-30.
60. Cuevas I et al. Eventos adversos temporalmente asociados a la vacuna antimeningocócica contra serogrupo B, 1998-1999. En: Enfermedades infecciosas y microbiología. Suplemento 2001; 21: 123.
61. Gibson B, Product Stewardship in the Chemical Industry. ATSE Focus 1997 (98) Disponible en: http://www.atse.org.au/index.php?sectionid=372, accedido 12 de julio 2006.
62. Toledo G y otros. Fundamentos de Salud Pública. Ciudad de La Habana, Cuba: Editorial Ciencias Médicas; 2005.
Abstract
A study about problems of post-commercialization surveillance in the pharmaceutical industry was carried out. Adverse reactions to medicines and vaccines cause a significant increase in the costs of sanitary assistance; vaccines in particular have a deferred and unknown benefit and an immediate risk. This is the reason why higher surveillance standards are required. Pharmaco-surveillance by itself presents obstacles which can be greater when they are focused on from the pharmaceutical industry. Company or sponsorship as strategy allows overcoming these obstacles and establishing the post-commercialization surveillance system which has been systematic practice of Finlay Institute. The experience of our Institute where all factors and conditions influencing on products are observed is an advance to obtain a better evaluation of the sanitary and economic impact on the application of our vaccines. Implementation and starting of pharmaco-surveillance in the medicine industry is a challenge and a necessity to complete the development of the pharmaceutical industry.
Keywords: Vaccines, pharmaco-surveillance, adverse reactions.
Recibido: Diciembre de 2006 Aprobado: Marzo de 2007