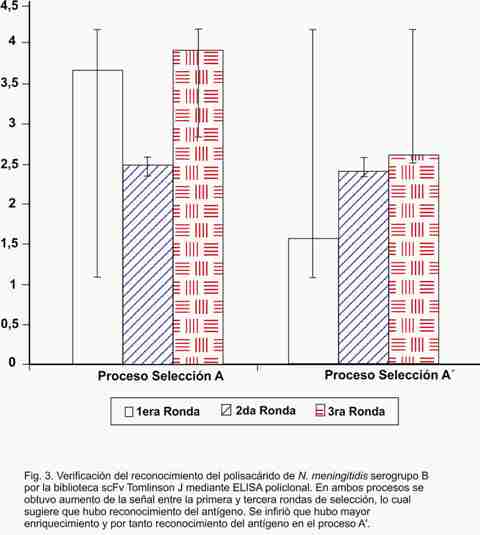
 ]]>
]]>
Aplicación de una biblioteca de anticuerpos lineales humanos frente al polisacárido capsular de Neisseria meningitidis serogrupo B
Application of a human linear antibody library against the capsular polysaccharide from Neisseria meningitidis serogroup B
Emigdio León-Toirac,1* Frank Camacho,2 María Elena Sarmiento,2 Alina Alerm,3 Domingo González,2 Humberto González,2 Armando Acosta2
1. Instituto de Neurología y Neurocirugía. Calle 29 esquina a D. Plaza de la Revolución, La Habana, Cuba.
2. Instituto Finlay, Centro de Investigación y Producción de Vacunas. Ave. 27, No. 19805, La Lisa, A.P. 16017 Cod. 11600. La Habana, Cuba. ]]>
3. Universidad Médica Victoria de Girón. La Habana, Cuba.
email: emigdio.leon@infomed.sld.cu
* Especialista de 1er grado en Inmunología y Medicina General Integral. Jefe Dpto Neurobiología, Laboratorio de Inmunología.
RESUMEN
Neisseria meningitidis serogrupo B produce aún morbimortalidad significativa. Su polisacárido capsular muestra similitud estructural con proteínas humanas y pobre inmunogenicidad, obstaculizando así el desarrollo de vacunas y anticuerpos monoclonales (AcM) y policlonales contra esta bacteria. Recientemente se han creado bibliotecas artificiales de anticuerpos humanos expresados en bacteriófagos que reconocen específicamente a moléculas diana existentes, con la ventaja sobre los AcM convencionales por su rápida obtención, sin utilización de animales de laboratorio, lo que emerge como alternativa atractiva para la producción de AcM contra antígenos peculiares o complejos. Se realizó un trabajo de investigación básica, utilizando una biblioteca de fagos filamentosos que expresan constitutivamente regiones variables de anticuerpos humanos, que se enfrentó al polisacárido capsular de N. meningitidis serogrupo B. Los resultados que se obtuvieron mediante ELISA policlonal sugieren la existencia de anticuerpos humanos expresados en fagos que lo reconocen.
Palabras claves: Neisseria meningitidis, polisacárido serogrupo B, bacteriófagos, anticuerpos monoclonales
ABSTRACT
Neisseria meningitidis serogroup B still produces a significant morbidity and mortality. Bacterial capsular polysaccharide in serogroup B shows structural homologies with human proteins and poor immunogenicity which make difficult the development of vaccines and polyclonal and monoclonal antibodies (MAb) against it. Artificial libraries of human antibodies via the expression and selection of them in bacteriophages have become known. Those antibodies are used as specific recognizing molecules capable to join to almost any existing target, with advantages over conventional MAb due to its faster obtainment without needing animal immunization, emerging as an attractive alternative for the production of MAb against complex or particular antigens. This was a basic experimental piece of work, using a phage library that expresses variable regions of human immunoglobulins to identify ligands with the capacity to recognize N. meningitidis serogroup B polysaccharide. Polyclonal ELISA screening suggests the existence of human antibodies expressed in phages which recognized the antigen of interest. ]]>
Key words: Neisseria meningitidis, serogroup B polysaccharide, bacteriophages, monoclonal antibodies.
INTRODUCCIÓN
La meningitis meningocócica constituye un problema de salud que afecta a múltiples países, independientemente de su desarrollo económico, de sus condiciones climatológicas o de los avances alcanzados por los mismos en el desarrollo de antimicrobianos y vacunas contra los microorganismos generadores de esta entidad nosológica (1).
La situación epidemiológica cubana relacionada con esta enfermedad tuvo un viraje considerable a finales de la década de 1980, cuando producto de la tenacidad de investigadores del Instituto Finlay se obtuvo VA-MENGOC-BC®, un producto vacunal reconocido internacionalmente como la primera vacuna efectiva contra el meningococo del grupo B, uno de los de mayor morbimortalidad.
La composición de esta vacuna está dada por un complejo de vesículas purificadas de la membrana externa del meningococo de serogrupo B y polisacárido capsular purificado del meningococo serogrupo C, adsorbido en gel de hidróxido de aluminio (1, 2).
Aunque posee un excelente perfil de reactogenicidad, inmunogenicidad y eficacia (83%), su aparición marcó el inicio de un largo periplo en la búsqueda priorizada de nuevos productos farmacológicos alternativos que tengan en cuenta las complejas características estructurales y funcionales de este microorganismo (1, 3).
Para el desarrollo de vacunas contra N. meningitidis el polisacárido capsular ha sido el inmunógeno de elección, ya sea en forma natural o conjugada, no siendo así en el caso del serogrupo B, debido a la elevada similitud estructural existente entre el polisacárido y las moléculas de ácido siálico, presentes en las superficies celulares humanas, así como con la molécula de adhesión NCAM (del inglés, neural cell adhesion molecule), altamente expresada en células del sistema nervioso durante el periodo embrionario y en la vida posnatal temprana (4, 5).
Esta peculiaridad, así como su naturaleza bioquímica polisacarídica y la repetitividad de monómeros homogéneos, convierten al polisacárido del serogrupo B en una molécula poco inmunogénica. La escasa inmunogenicidad de este componente le confiere a la bacteria un mecanismo de escape a la respuesta inmune del hospedero, generando gran dificultad para trabajar en la obtención de productos biológicos efectivos contra estas cepas (3, 4). ]]>
El constante interés por eludir estos escollos ha generado un creciente número de aproximaciones experimentales enfocadas a lograr un incremento de la inmunogenicidad del polisacárido, con el objetivo de revertir la tolerancia inmunológica inducida por la presencia de este mimetismo molecular, empleando la conjugación con proteínas (4) o la sustitución de grupos N-acetil, presentes en la molécula homopolímero, 200 unidades repetitivas de ácido a(2®8) N-acetilneuramínico, por grupos N-propionil (5). Los resultados han sido contradictorios debido al incremento del riesgo de autorreactividad en el hospedero vacunado o la transferencia materna de inmunoglobulinas (Ig) por vía transplacentaria que interfieran con el desarrollo neurológico del feto (4-6).Otras alternativas (7, 8) contemplan el posible empleo de AcM como herramientas terapéuticas y diagnósticas, aplicadas en la caracterización serológica de antígenos de N. meningitidis con fines epidemiológicos (4), debido a su altísimo grado de unión y especificidad antigénica, así como por la garantía de una excelente ubicación de la diana molecular.
La evolución de los AcM ha transitado desde su obtención en el modelo murino en un inicio, luego los AcM quiméricos humanizados hasta la obtención de anticuerpos (Ac) con mayor eficacia a partir de la implementación de numerosas variantes en el proceso de obtención de los mismos (8). Tal es el caso de los anticuerpos recombinantes expresados en bacteriófagos o fagos, que son proteínas pequeñas compuestas por los dominios variables (Fv, del inglés Fragment variable) de las cadenas pesada y ligera de una Ig, asociados generalmente por un conector peptídico flexible. Estas moléculas han recibido la denominación en el argot científico de AcM de una sola cadena, debido a su especificidad de reconocimiento y a su procedencia de regiones variables de Ig, pero en estructura primaria, o sea, no conformacional (9).
Las técnicas de biología molecular resultan imprescindibles para obtener y poner en uso estas bibliotecas artificiales de anticuerpos que pueden originar estructuras reconocedoras capaces de unirse a casi cualquier molécula diana existente. De esta manera, los fragmentos de Ac derivados de fagos ofrecen ventajas sobre los AcM tradicionales al tener menor talla, mayor capacidad de penetración a tejidos y mejor aclaramiento plasmático. El empleo de esta tecnología no requiere de animales de experimentación, elemento que contribuye con la rapidez del proceso de producción y constituye un notable aporte, desde el punto de vista tecnológico y ético. Otra de las ventajas de gran importancia es que permite la obtención de AcM frente a antígenos de baja inmunogenicidad, como es el caso de los polisacáridos (8, 9).
Un estudio precedente (6) ha empleado epítopos capsulares presentes de manera natural en la superficie de meningococos para desarrollar anticuerpos antiidiotípicos de una sola cadena que, al ser administrados en humanos, inducen anticuerpos de clase G dirigidos contra la cápsula bacteriana, sin ocasionar reactividad cruzada con la molécula NCAM humana. De igual manera, otros autores (4, 10) también reportan el empleo de bibliotecas de fagos en modelos de experimentación murinos para lograr mimotopos que evitan el riesgo de reactividad cruzada relacionado con la inmunización del antígeno capsular completo. En este caso el procedimiento empleado para la obtención de AcM es mediante la producción de hibridomas (10).
Este estudio pretendió verificar la posibilidad de aplicación de una biblioteca de Igs humanas, expresadas en fagos filamentosos, en el reconocimiento del polisacárido capsular de N. meningitidis de serogrupo B. Esta herramienta, mucho más sencilla y que no requiere de la utilización de animales de laboratorio, empleada por primera vez para este inmunógeno en el Instituto Finlay, contribuyó a la búsqueda de nuevas estrategias de intervención diagnósticas y terapéuticas en el ámbito de las infecciones por N. meningitidis.
MATERIALES Y MÉTODOS
Se desarrolló un trabajo de investigación básica utilizando una biblioteca de fagos filamentosos que expresan regiones variables de Ac lineales humanos que se enfrentó al polisacárido de N. meningitidis de serogrupo B.
Cepas o microorganismos ]]>
La cepa de N. meningitidis de la cual se obtuvo el polisacárido presentó el fenotipo B:4:P1.19,15:L3,7,9. Esta cepa es utilizada para la obtención de las vesículas de membrana externa de la vacuna VA-MENGOC-BC® (1).Las cepas bacterianas empleadas de E. coli TG1 supE D(hsdM - mcrB) 5 (rk- mk- McrB-) thi D(lac - proAB) fueron donadas por el Centro de Ingeniería Genética y Biotecnología (CIGB) de La Habana, Cuba.
Los fagos auxiliadores M13 K07 fueron suministrados por BioLabs, Reino Unido. Para la elución de fagos se empleó como reactivo la trietilamina suministrada por Sigma-Aldrich.
Polisacárido B de N. meningitidis
Se purificó el polisacárido por el método empleado para la obtención del polisacárido C en el proceso de producción de VA-MENGOC-BC® (protegido bajo patente en favor de sus autores) con algunas modificaciones que consisten en precipitaciones alcohólicas seriadas al 25% y 80%, con periodos de incubación entre 4 y -20 ºC, seguidos de centrifugación a 4 ºC, 3500 x g por 30 min. El debris celular resultante se sometió a tratamiento con alcohol y secado en campana con cloruro de calcio, donde se monitoreó el peso de la muestra tres veces por día. El proceso de secado se detuvo cuando no existieron variaciones en el peso de la muestra o las variaciones entre dos mediciones consecutivas fueron menores de 0,01 g. Se caracterizó la muestra purificada, estimando la concentración del polisacárido de N. meningitidis mediante la determinación de ácido siálico, según método de Svennerholm (11). Para determinar la concentración de proteína se empleó el método de Lowry (12) y para la de ácidos nucleicos, la lectura directa por espectrofotometría (13).
Para la determinación cualitativa de lipopolisacáridos (LPS) como contaminante de la muestra de polisacárido B purificado de N. meningitidis, 20 µg de la misma se incubaron a 100 ºC durante 5 min en presencia de 2-mercapto-etanol (Merck) y se aplicó en una electroforesis en gel de poliacrilamida al 15% (SDS-PAGE) (14), seguida de una tinción con plata para LPS (15), según Laemmli y Tsai. La concentración de LPS se estimó mediante la cuantificación de unidades de 2-Keto, 3-deoxietanoato de amonio al 99% (KDO) mediante el método de ácido tiobarbitúrico (TBA) modificado (16).
Anticuerpos y conjugados
Los Ac de trabajo fueron policlonales antipolisacárido B de N. meningitidis (obtenido de conejo), producido comercialmente para el diagnóstico por la Empresa Producción de Biológicos "Carlos J. Finlay", La Habana, Cuba y Ac policlonal anti-IgG total de conejo conjugado a enzima peroxidasa de rábano picante (origen bovino), suministrado por Sigma; así como el AcM anti-M13 conjugado a la enzima peroxidasa de rábano picante (HRP/Anti-M13), suministrado por General Electric Healthcare, Londres, Reino Unido.
Biblioteca de anticuerpos lineales
Esta biblioteca de anticuerpos lineales expresados en fagos filamentosos comprende más de 100 millones de scFv diferentes clonados en un vector fagémido que incluye un gen de resistencia a la ampicilina, que requiere transformación en células de E. coli TG1. Los scFv poseen un único polipéptido con los dominios de las regiones variables de las cadenas pesadas VH (V3-23/DP-47 y JH4b) y ligera Vk (O12/O2/DPK9 y Jk1) de Ig humanas, unidos entre sí por un conector flexible de glicina-serina, con diversidad en cadenas laterales incorporadas en las posiciones del sitio de unión a antígenos. El tamaño de la biblioteca es de 1,37 x 108 y el porcentaje de inserción es de 88% (9). ]]>
Evaluación de la funcionalidad de la biblioteca con la seroalbúmina bovina (BSA)La biblioteca se obtuvo comercialmente en forma de fagémido/scFv, por lo que antes de su empleo se transformó, indujo, purificó y tituló, utilizando como antígeno de enfrentamiento BSA suministrada por PROMEGA en inmunotubos Maxisorp de 3 mL. Estos procesos se realizaron en tres rondas consecutivas de selección que aportaron tres fracciones adsorbidas (A) con 100 fagos infectivos como mínimo y tres fracciones no adsorbidas (N) (9). Finalmente, se evaluó la funcionalidad de la biblioteca de anticuerpos lineales scFv usando la BSA como antígeno.
Selección de Anticuerpos scFv contra polisacárido B purificado
Para la selección de fagos que reconocieron al polisacárido B de N. meningitidis se utilizó la metodología descrita anteriormente, pero empleando el polisacárido B como antígeno de recubrimiento a razón de 10 µg/mL en cada pocillo. La concentración de recubrimiento correspondió al punto medio de la meseta obtenida entre las concentraciones de 5 y 20 µg/mL. El proceso se realizó por duplicado (ciclos de selección A y A').
Evaluación del reconocimiento del polisacárido B de N. meningitidis por las secuencias de Ig humanas expresadas en fagos filamentosos
Se emplearon variantes de ensayo inmunoabsorbente ligado a enzima (ELISA, del inglés Enzime Linked Immunosorbent Assay) indirecto, en tiras individuales Maxisorp de 8 pocillos.
Se empleó la variante de ELISA policlonal de fagos para verificar la unión de scFv al polisacárido B de N. meningitidis purificado, aplicando 100 µL de polisacárido de N. meningitidis serogrupo B purificado en tiras Maxisorp e incubando estas a 4 ºC durante 14 h. Se realizaron tres lavados con solución salina tampón fosfato (SSTF) - Tween 20 al 0,1%.
Para el bloqueo se empleó SSTF - leche descremada al 2%. Se adicionaron 100 µL de los fagos obtenidos de cada ronda de selección (dilución 1:5) y se incubó durante 1 h. Se adicionaron los Ac anti-M13 conjugados a enzima peroxidasa a la concentración recomendada por el fabricante (1:5000), incubando durante 1 h a una temperatura de laboratorio. Se empleó como solución sustrato la ortofenilendiamina (OPD) con peróxido de hidrógeno y tampón acetato sódico, pH 6,0. Se realizó la lectura en espectrofotómetro a una longitud de onda de 492 nm (9).
Para ratificar la especificidad del reconocimiento se estableció una comparación con ELISA policlonal de fagos, al cual se adicionaron 100 µL por pocillo de una solución de polisacárido C a una concentración de 2,5 µg/mL (17). El resto del proceso transcurrió como fue descrito anteriormente.
Paquetes de análisis de resultados y elaboración de gráficos ]]>
Para el procesamiento de los datos y análisis de los resultados se utilizó el programa GraphPad Prism version 4.00 para Windows, GraphPad Software, San Diego California USA, www.graphpad.com. Se calcularon coeficientes de correlación (lineal y de Pearson).
RESULTADOS Y DISCUSIÓN
Los polisacáridos de N. meningitidis son antígenos a tener en cuenta para el desarrollo de vacunas contra distintos serogrupos, tomando en consideración su presencia en todos los serotipos, su ubicación celular en la superficie externa de la bacteria y su capacidad de inducir Ac bactericidas (18).
La purificación de estas moléculas constituye un elemento de crucial importancia en el desarrollo de biopreparados, empleando el método clásico de purificación por precipitación con cetavlon y etanol combinado con extracciones con fenol, brindando un producto con características óptimas para la inducción de inmunidad y por tanto para la producción de vacunas (5)
La vacuna cubana antimeningocócica VA-MENGOC-BC® emplea como inmunógenos al polisacárido capsular purificado de N. meningitidis serogrupo C (50 µg) y vesículas purificadas de la membrana externa de N. meningitidis serogrupo B (50 µg). En la producción de este producto profiláctico el polisacárido B es considerado un contaminante que se elimina durante el proceso (1, 18). Teniendo en cuenta que este último era el antígeno de interés de esta investigación, nos propusimos purificar el polisacárido B, a partir de uno de los pasos del proceso de producción, empleando una de las fracciones desechadas con alto contenido glucídico, proveniente de la cepa de N. meningitidis con fenotipo B:4:P1.19,15:L3,7,9 (1).
Con la fracción que se obtuvo se siguió el método empleado para la purificación del polisacárido C con modificaciones (2), teniendo en cuenta las características particulares del polisacárido B. De la aplicación de estas técnicas se logró una cantidad de aproximadamente 2 g de polisacárido B purificado, en presentación de polvo seco, con una concentración de 2,142 mg/mL. Posteriormente se procedió a la caracterización del mismo para evaluar si la molécula obtenida estaba acorde con los parámetros de calidad establecidos para polisacáridos capsulares de uso vacunal, según la presencia de proteínas, ácidos nucleicos y lipopolisacáridos.
Los criterios de liberación de polisacáridos de N. meningitidis para vacunas del Departamento de Control de la Calidad del Instituto Finlay norman que la relación proteínas/polisacáridos debe ser £ 1 mg/g (menor del 1% de la muestra); la de ácidos nucleicos debe ser £ 1 mg/g (menor del 1% de la muestra) y la de LPS debe ser inferior a 20 unidades de endotoxina/mg de polisacárido, según LAL (13) y se estima que sea menor del 5%, según método de TBA (16).
En la presente investigación se obtuvo un producto con características que sugieren un elevado nivel de pureza, inferido al determinarse en la muestra las concentraciones de proteínas, ácidos nucleicos y lipopolisacáridos. La concentración de proteínas fue de 7,98 µg/mL (representando un 0,15% del total de la muestra). La concentración de ácidos nucleicos fue de 0,39 mg/mL (7,8%). La electroforesis en gel de poliacrilamida con tinción con plata demostró la ausencia de bandas de LPS en la muestra, lo cual se corroboró cuantitativamente con la detección de unidades de KDO, con una concentración de 0,163 mg/mL (Tabla).
Aunque no se cuenta con especificaciones de calidad del polisacárido serogrupo B, ya que no existe vacuna basada en el mismo, los valores obtenidos, luego de la caracterización molecular se aproximan a los referidos en los controles de calidad para vacunas que emplean como inmunógeno al polisacárido del serogrupo C de N. meningitidis. El grado de pureza del polisacárido B procesado para este trabajo minimizó la obtención de clonos de fagos que reaccionaron con contaminantes e incrementó la eficiencia de los procesos sucesivos. ]]>
En nuestro trabajo utilizamos la biblioteca scFv Tomlinson J que es empleada en diversas aplicaciones (8, 9). Este producto se sometió a procesos de transformación y amplificación a partir de la forma comercial, garantizando un elevado porcentaje de inserción de los genes scFv. Se obtuvo un lote de 15 alícuotas, cada una con 500 µL de la biblioteca scFv Tomlinson J expandida. Producto de su amplificación se obtuvo una cantidad de fagos, 1,6 x 1016 UFC/µL, la cual estuvo por encima del rango sugerido por los creadores de la biblioteca (9) como óptimo para iniciar el trabajo de selección (1012 - 1013 UFC/µL).Se comprobó la funcionalidad del producto resultante, determinando el nivel de enriquecimiento después de sucesivos ciclos de selección con BSA (Fig. 1). Se tomó como criterio el aumento proporcional del número de unidades formadoras de colonias entre la primera y ultima ronda de selección. El comportamiento de las fracciones eluidas de las distintas rondas de selección evidenció un aumento gradual del título de la fracción adsorbida entre la primera y tercera ronda de selección. Se garantizó la estabilidad del proceso mediante la conservación del error para 1 desviación estándar en cada etapa del mismo. Esto puso en evidencia la adecuada funcionalidad de la biblioteca.
Los resultados se expresaron como el cociente entre la media de las densidades ópticas obtenidas de la lectura de los duplicados de cada una de las fracciones (A) y la media de las densidades ópticas de los duplicados de la muestra de la biblioteca utilizada antes del inicio del proceso de selección (C-, control negativo) resultando en (X DO A) / X DO C-) (9).
El incremento del número de fagos en la fracción adsorbida en cada ronda de selección contrastó con la estabilidad de los conteos de fagos en las fracciones no adsorbidas obtenidas al final de cada ronda, lo cual tributó a una disminución gradual de la relación entre las fracciones no adsorbida/adsorbida. Este resultado concuerda con lo reportado por Menéndez y cols. (19) con metodología similar a la nuestra. Aunque otros autores (10, 18) obtienen resultados que muestran mayor enriquecimiento combinando el presente método con la citometría de flujo.
Al establecer las condiciones iniciales para el enfrentamiento de la biblioteca amplificada al polisacárido de N. meningitidis de serogrupo B se decidió que el recubrimiento de los inmunotubos debía hacerse con el polisacárido purificado disuelto exclusivamente en SSTF. Este proceder difiere de lo reportado en la literatura (17) que plantea un recubrimiento más eficiente empleando poli-L-Lisina y otros artificios para aumentar la capacidad de fijación del antígeno.
Se tomaron en cuenta algunos trabajos previos (5, 17), en los cuales se utiliza el polisacárido para el recubrimiento sin la adición de ninguna otra sustancia, ni pretratamiento de la fase sólida, para evitar la obtención de fagos que reaccionen inespecíficamente con otros componentes diferentes al antígeno seleccionado.
Con el enfrentamiento de la biblioteca scFv Tomlinson J, previamente expandida al polisacárido capsular purificado de N. meningitidis de serogrupo B, se eluyeron las fracciones adsorbidas con los supuestos fragmentos reconocedores del antígeno de interés. Se completaron dos procesos de selección frente al polisacárido objeto de estudio y se estableció la comparación de fracciones adsorbidas con la curva patrón de BSA. El proceso mostró un incremento proporcional del título de las fracciones adsorbidas en cada ronda de selección realizada, con tendencia lineal y coeficiente de correlación de 0,99; lo cual se correspondió con el enriquecimiento de Ac lineales en la fracción eluida, después de su interacción repetida con el antígeno glucídico capsular. Se interpretó que hubo funcionalidad adecuada de la biblioteca frente al antígeno. Estos resultados se reprodujeron en dos experimentos independientes realizados en condiciones similares (Fig. 2).
El reconocimiento del polisacárido de N. meningitidis serogrupo B por la biblioteca scFv Tomlinson J se verificó mediante ELISA policlonal. El ensayo inmunoenzimático mostró un aumento de la señal en relación con la obtenida por la biblioteca de fagos frente a la BSA, en todas las fracciones estudiadas. Este patrón se alteró solo con el resultado de la segunda ronda del primer ciclo de selección (A2), para lo cual no hay una explicación precisa. Es de señalar que a pesar de este resultado la tercera ronda de ese mismo ciclo de selección mostró los mayores niveles de señal con respecto a la ronda inicial.
Este resultado sugiere que hubo reconocimiento del polisacárido de N. meningitidis serogrupo B purificado por los Ac lineales humanos expresados en fagos de la biblioteca en estudio. Aunque los niveles de densidad óptica del proceso A fueron mayores que los del proceso A', los cocientes obtenidos de los valores de las terceras y primeras rondas de ambos procesos fueron de 1,05 y 1,65 respectivamente. Se infirió que hubo mayor reconocimiento del antígeno en el proceso A' (Fig. 3).
Las señales obtenidas al analizar el ELISA policlonal con las distintas fracciones de las tres rondas de los dos procesos de selección, fueron similares a las reportadas por otros autores (19) que han trabajado con antígenos polisacarídicos.
Teniendo en cuenta la similitud estructural parcial entre los polisacáridos de N. meningitidis de serogrupos B y C (4, 5) nos propusimos estudiar si se producía algún nivel de reactividad cruzada entre los fagos seleccionados después del enfrentamiento con el polisacárido B y el polisacárido C, seleccionando la fracción adsorbida que se obtuvo de la tercera ronda de selección del proceso A', la cual mostró mejor nivel de enriquecimiento cualitativo que las del proceso A.
Al aplicar el inmunoensayo policlonal con recubrimiento de ambos polisacáridos capsulares, esta fracción mostró señales en ambos casos, lo que reafirmó el reconocimiento específico de la estructura glucídica. Se comprobó que la presencia de señal tras el enfrentamiento de la misma fracción adsorbida con el polisacárido capsular de N. meningitidis serogrupo C era mayor. La respuesta contra el polisacárido B fue duplicada frente al antígeno C (cociente polisacárido C / polisacárido B = 2,51). Esta respuesta policlonal sugiere que se estableció reactividad cruzada entre ambos antígenos por los Ac lineales seleccionados en esta fracción (Fig. 4).
Este particular resultado pudiera ser expresión de la similitud estructural entre ambos polisacáridos. El mayor reconocimiento frente al polisacárido C pudiera estar relacionado con una mayor accesibilidad de los epítopos comunes después del recubrimiento de la placa de ELISA.
Estudios con AcM de tipo IgM contra el polisacárido B de N. meningitidis (5, 8) reportan el reconocimiento del polisacárido C por estos Ac. Por otro lado, una investigación anterior (5) refiere que la inmunización de ratones con conjugados de polisacárido B induce Ac que reconocen el polisacárido C y viceversa. A pesar de estos resultados, la existencia de reactividad cruzada contra el polisacárido B, partiendo de inmunizaciones con polisacárido C, ha sido refutada por algunos autores (20).
Nuestros resultados muestran la existencia de dicha reactividad cruzada, amparada probablemente por la similitud estructural entre las moléculas polisacarídicas que solo difieren en la posición de los enlaces de carbono en su estructura de homopolímero de Ácido N-acetil-neuramínico [a(2®8) en el caso del polisacárido B y a(2®9) para el polisacárido C] (7).
Además, la reactividad cruzada entre polisacáridos de N. meningitidis generalmente se ha observado en contextos de tolerancia (6), donde las influencias regulatorias tienen un rol crucial, como es el caso de las inmunizaciones con antígenos vacunales en animales de experimentación o en humanos. Fuera de este ambiente de regulación, se generan respuestas inmunes al romper la barrera de la tolerancia a nivel experimental, conjugando el polisacárido de interés con un péptido de 60 Kd derivado de la proteína de choque térmico (HSP, del inglés heat shock protein) (5) o como en nuestro estudio, al enfrentar in vitro el polisacárido con los efectores de la respuesta inmune. ]]>
La reactividad frente al polisacárido C podría, además, constituir una prueba indirecta de la obtención de clonos que reconocen al polisacárido B después del proceso de selección. Aunque en un estudio precedente (6) se sugiere la obtención de mimotopos del polisacárido serogrupo B de N. meningitidis mediante bibliotecas de péptidos expresadas en fagos filamentosos o la obtención de Ac antiidiotípicos, como alternativa tanto para el proceso de selección, como para el tamizaje de verificación posterior. Incluso, el empleo de estas moléculas miméticas permitiría trabajar con secuencias epitópicas que sean exclusivas del polisacárido B, limitando así la posibilidad de reactividad cruzada contra el polisacárido C.De manera confirmatoria debe emplearse la técnica de inmunoensayo enzimático monoclonal, como lo sugieren trabajos reportados en la literatura científica sobre métodos de ELISA monoclonal de este tipo (9, 10, 19) que testan un amplio número de clonos de alta especificidad, obtenidos de sobrenadantes sin diluir del cultivo de las fracciones más enriquecidas de los ciclos de selección iniciales. Este paso constituye un requisito obligatorio para identificar la presencia de clonos positivos o no, ya que el simple enriquecimiento entre una selección y otra no es conclusivo. Los resultados de esta investigación, eminentemente exploratoria, tributan necesariamente al ELISA monoclonal como paso de verificación que permitirá la caracterización del AcM obtenido.
Además, teniendo en cuenta que el sistema desarrollado por Tomlinson y cols. (9) consta de dos bibliotecas: I y J, con diferencias en el porcentaje de inserción de secuencias de Ig humanas y en sus respectivos repertorios, sería de utilidad en trabajos futuros realizar el enfrentamiento del polisacárido de serogrupo B de N. meningitidis con la biblioteca scFv Tomlinson I, con el objetivo de obtener clonos de fagos con mayor grado de reconocimiento por el antígeno en estudio, considerando la recomendación de los creadores de esta tecnología sobre la utilización simultánea de ambas bibliotecas para mayor rendimiento.
Otro aspecto a considerar, es el tipo de sistema de tamizaje a utilizar para verificar el reconocimiento frente al antígeno de interés. En el caso particular de los polisacáridos, por sus dificultades intrínsecas, algunos autores recomiendan el uso de varios sistemas paralelos a fin de ampliar las posibilidades de identificación de clonos con reactividad apropiada. En este sentido se ha reportado (6, 10) el empleo de ELISA de células completas con mayor sensibilidad al adicionar al recubrimiento la poli-L-lisina o avidina. Otra opción (17) propone emplear fases sólidas de materiales plásticos que garanticen una mayor adherencia de moléculas de antigenicidad compleja o aplicar tratamientos con derivatizaciones a los polisacáridos.
La estructura lineal de estos AcM también podría valorarse como una interferencia en el reconocimiento de antígenos. Por tal razón este trabajo se plantea como perspectiva mediata, que una vez que sean identificadas las secuencias lineales de Ig humanas que reconozcan específicamente al polisacárido de serogrupo B de N. meningitidis, estas se inserten en una molécula sintética de Ig humana. Este nuevo producto con estructura conformacional, obtenido por diferentes centros cubanos de investigación, garantizaría la recuperación de las funciones biológicas de este Ac, tanto por su porción de unión a antígenos, como por su fracción constante. De igual manera, se evaluará posteriormente la idoneidad, a nivel diagnóstico y terapéutico, de este AcM totalmente humano.
Finalmente, los resultados obtenidos mediante ELISA policlonal sugieren la existencia de AcM lineales capaces de reconocer al polisacárido B de N. meningitidis. Este trabajo constituye el primer reporte del empleo de la tecnología de bibliotecas de Ac lineales expresados en fagos para este inmunógeno, desarrollado de manera íntegra en el Instituto Finlay, centro rector de la investigación y producción de vacunas en el país. La implementación de nuevas investigaciones será necesaria para corroborar estos hallazgos, así como para caracterizar los Ac lineales específicos y evaluar sus posibilidades biológicas y clínicas.
Agradecimientos
A los colegas de los laboratorios de Virología, Biología Molecular, Inmunoquímica y AcM de la Vicepresidencia de Investigaciones del Instituto Finlay, por su valiosa colaboración técnica, y al profesor Rolando Ochoa, por sus oportunos comentarios sobre el tema.
]]>
REFERENCIAS1. Sotolongo F, Campa C, Casanueva V, Fajardo ME, Cuevas IE, González N. Cuban Meningococcal BC Vaccine: Experiences & Contributions from 20 Years of Application. MEDICC Review 2007;9(1):16-22.
2. Merchán Y, Cuevas M. Estudio de un método de desadsorción de los componentes de VA-MENGOC-BC para el control de calidad por HPLC. VacciMonitor 2003;12(3):1-4.
3. Domínguez F, Menéndez J, Ochoa R. An effective serogroup B meningococcal vaccine. Vaccine 2006;24(49-50):7025-6.
4. Nicolas P. Vaccinal strategies in response to new epidemiological challenges in 2010. Reasonable hope for a "B" meningococcal vaccine. Med Trop 2010;70(4):325-32.
5. Amir-Kroll H, Riveron L, Sarmiento ME, Sierra G, Acosta A, Cohen IR. A conjugate vaccine composed of a heat shock protein 60 T-cell epitope peptide (p458) and Neisseria meningitidis type B capsular polysaccharide. Vaccine 2006;24:6555-63.
6. Beninati C, Arseni S, Mancuso G, Magliani W, Conti S, Midiri A, et al. Protective Immunization against Group B Meningococci Using Anti-Idiotypic Mimics of the Capsular Polysaccharide. The Journal of Immunology 2004;172:2461-8.
7. Krug LM, Ragupathi G, Hood C, George C, Hong F, Shen R, et al. Immunization with N-propionyl polysialic acid-KLH conjugate in patients with small cell lung cancer is safe and induces IgM antibodies reactive with SCLC cells and bactericidal against group B meningococci. Cancer Immunol Immunother 2012;61(1):9-18.
8. Cabezas Sh, Rojas G, Pavón A, Álvarez M, Pupo M, Guillén G, et al. Selection of phage-displayed human antibody fragments on Dengue virus particles captured by a monoclonal antibody: Application to the four serotypes. Journal of Virological Methods 2008;147(2):235-43.
9. BIOTECH. Human single Fold scFv Libraries I + J (Tomlinson I+J) Grade Frac System Farmacia. California, SF., USA: Assay Biotechnology Company, Inc; 2006.
10. Shin JS, Lin JS, Anderson PW, Insel RA, Nahm MH. Monoclonal antibodies specific for Neisseria meningitidis group B polysaccharide and their peptide mimotopes. Infection and Immunity 2001;69(5):3335-42.
11. Svenerholm L. Quantitative estimation of Sialic II. A colorimetric resorcinol hidrochloric acid method. Biochem. Byophy Acta 1957;24:609-13.
12. Lowry O. A protein measurement with the folin - phenol reagent. Biol. Chem 1951;193:265-75.
13. WHO Expert Committee on Biological Standardization. Recommendations to assure the quality,safety and efficacy of group A meningococcal conjugate vaccines.Geneva:WHO;2006.Disponible en:http://www.who.int/biologicals/publications/trs/areas/vaccines/meningococcal/en/index.html
14. Laemmli UK. Cleaveage of strutural proteins during the assembly of the head of bacteriophage T4. Nature 1970;227:680-5.
15. Tsai CM, Frash SE. Silver stain a method to detection after polyacrylamide gel electrophoresis. Anal Biochem 1982;119:115-9. ]]>
16. Balboa JA, Estrada J, Nápoles LD, Aguilar S, González H, Hernández D, et al. Purificación de lipopolisacárido de Neisseria meningitidis a partir de una fracción colateral del proceso de producción de VA-MENGOC-BC®. VacciMonitor 2008; 17(1):17-26.
17. Ochoa R, Nerey M, Martínez JC. Use of Poly-L-lysine Precoating in an ELISA for the Detection of Antibodies against Serogroup C Neisseria meningitidis Capsular Polysaccharide. Biotecnología Aplicada 1999;16(3):173-5.
18. Lo Passo C, Romeo A, Pernice I, Donato P, Midiri A, Mancuso G, et al. Peptide Mimics of the Group B Meningococcal Capsule Induce Bactericidal and Protective Antibodies after Immunization. The Journal of Immunology 2007;178(7):4417-23.
19. Menéndez T, Santiago-Vispo NF, Cruz-Leal Y, Coizeau E, Garay H, Reyes O, et al. Identification and characterization of phage-displayed peptide mimetics of Neisseria meningitidis serogroup B capsular polysaccharide. International Journal of Medical Microbiology 2011;301(1):16-25.
20. Krambovitis E, McIllmurray MB, Lock PA, Holzel H, Lifely MR, Moreno C. Murine monoclonal antibodies for detection of antigens and culture identification of Neisseria meningitidis group B and Escherichia coli K-1. J Clin Microbiol 1987;25(9):1641-4. ]]>
Recibido: Marzo de 2013
Aceptado: Mayo de 2013 ]]>