ARTÍCULO ORIGINAL
Caracterización molecular de un aislamiento cubano de parvovirus canino
Molecular characterization of a Cuban isolation of canine parvovirus
Anniet Fresneda-Disotuar,1* Digna Contreras-González,1 Mayelin Paneque-Zayas,1 Lianet de la Cruz-Verdura,1 Carmen Veda Rueda2
1 Unidad de Producciones de Vacunas Virales y Bacterianas. Grupo Empresarial de Producciones Biofarmacéuticas y Químicas. LABIOFAM. Ave Independencia, km 16 ½ .Santiago de las Vegas. Municipio Boyeros. La Habana. Cuba, CP 10800.
]]> 2 Empresa Inmunología y Genética Aplicada. INGENASA, C.I.F. A28/685154 domiciliada en Madrid, Calle Hnos. García Noblejas Nº 41.email: labiofamcuba@labiofam.co.cu
*Licenciada en Bioquímica. Departamento de Investigaciones y Desarrollo Biofarmacéuticos, Labiofam, La Habana, Cuba.
RESUMEN
El parvovirus canino tipo 2 (VPC-2) es el agente causal de una enfermedad infecto-contagiosa que produce gastroenteritis aguda hemorrágica que afecta a caninos jóvenes. El VPC-2 es un virus con genoma ADN, pequeño, desnudo y muy resistente a las condiciones ambientales que emergió y se expandió rápidamente a fines de la década de los años 70. En los años 80 surgieron consecutivamente dos variantes antigénicas, denominadas VPC-2a y VPC-2b. En el 2000 se detectó una nueva variante antigénica llamada VPC-2c, reportándose con frecuencia en comunidades caninas de varios países del mundo. El objetivo de este trabajo consistió en caracterizar un aislamiento cubano de parvovirus canino, atenuado y adaptado a cultivo celular. El material genético fue amplificado por reacción en cadena de la polimerasa y secuenciado posteriormente. Las secuencias obtenidas fueron analizadas y comparadas con secuencias de aislados y cepas conocidas depositadas en las bases de datos, donde se evidenció que el aislamiento cubano era del tipo VPC-2.
Palabras clave: parvovirus canino, caracterización molecular, PCR.
ABSTRACT
The type 2 canine parvovirus (CPV-2) is the causal agent of an infected-contagious disease that produces a hemorrhagic and acute gastroenteritis that affects young canines. The CPV-2 is a virus with a small, naked DNA genome, very resistant to the environmental conditions that emerged and expanded fast at the end of the 70´s decade. In the 1980, two antigenic variants of CPV-2 emerged almost simultaneously. They were called CPV-2a and CPV-2b. In the 2000, a new antigenic variant was detected. It was called CPV-2c, and was frequently reported in canine communities in some countries worldwide. The objective of this work is to characterize a Cuban isolation of canine parvovirus attenuated and adapted to cellular cultivation. The genetic material was amplified by polymerase chain reaction and sequencing later. The obtained sequences were analyzed and compared with sequences of well-known strains placed in the data base where it was evidenced that the Cuban isolation was of CPV-2 type.
]]> Keywords: canine parvovirus, molecular characterization, PCR.
INTRODUCCIÓN
La parvovirosis canina es una enfermedad altamente contagiosa y de alta mortalidad. El agente etiológico que la produce es el parvovirus canino tipo 2 que se ubica taxonómicamente dentro de la familia Parviviridae, sub-familia Parvovirinae, género Parvovirus (1).
El virus tiene un genoma de cadena simple lineal, de polaridad negativa y una talla de 5,2 kb, que codifica las proteínas no estructurales NS1 y NS2, involucradas en la replicación viral, y las proteínas estructurales VP1, VP2 y VP3 que conforman la cápside. El VPC-2 carece de envoltura lipídica y posee una cápside de 26 nm de diámetro formada por 60 subunidades compuestas por VP1, VP2 y VP3 (2).
Los virus con genoma ADN usualmente poseen una tasa de evolución relativamente baja; sin embargo, el VPC-2 presenta una tasa de cambio muy elevada, más parecida a la de los virus con genoma ARN (3). Esto puede explicar la rápida y constante evolución de VPC-2 observada durante su corta historia desde su primera descripción en el año 1978.
En la década de los años 80, dos variantes antigénicas de VPC-2 emergieron casi simultáneamente y fueron llamados VPC tipo 2a y tipo 2b (4). En el 2000 fue detectado en Italia un nuevo tipo antigénico del VPC, el tipo 2c. Posteriormente fue reportado en Vietnam, España, Estados Unidos, Portugal, Alemania, el Reino Unido y Uruguay y más recientemente, se ha informado su detección también en Argentina (5).
La parvovirosis canina es una de las enfermedades infecciosas más prevalentes en canes entre 6 y 12 semanas de vida (6), pero también puede afectar perros de mayor edad. Los signos clínicos más comunes son: anorexia, depresión, disnea, seguidos de vómito y diarrea con frecuencia sanguinolenta y fiebre (7).
En Cuba la enfermedad fue descrita por primera vez en 1981 y su introducción en el país está relacionada con las importaciones de caninos (8); actualmente la incidencia de casos de parvovirosis en perros es creciente y la mortalidad es elevada, aunque hay que destacar que en los primeros cinco años de reportada la enfermedad en el país, los valores de mortalidad y letalidad eran superiores al 80% y en algunas zonas del 100%, motivado por la plena susceptibilidad de los caninos jóvenes unido a la gran virulencia de las cepas (9).
]]> Hoy en día, después de más de 20 años de haberse detectado la enfermedad, se observa que los valores de mortalidad y letalidad no son tan absolutos y la tasa de animales recuperados es mayor. En una encuesta realizada en la Clínica de animales afectivos de La Habana se constató que la parvovirosis canina está en la lista de las tres enfermedades más frecuentes de los cachorros, con mayor frecuencia en los de razas puras (10).En la actualidad se ha incrementado el empleo de vacunas en la prevención de esta enfermedad por su impacto en la salud animal. El Centro Nacional de Animales de Laboratorio (CENPALAB) de La Habana, produce una vacuna por subunidades contra el parvovirus canino tipo 2 (ALYb® PVCan); sin embargo, ante la necesidad de producir una vacuna viva atenuada contra la parvovirosis canina, nos propusimos la caracterización molecular de un aislado cubano de parvovirus canino, previamente atenuado y adaptado a cultivo celular, que pueda ser empleado en el futuro como candidato vacunal.
MATERIALES Y MÉTODOS
Procedencia y características de la cepa: La cepa de trabajo (CPL-0015) proviene de un aislamiento cubano obtenido en 1991 en el Laboratorio Central de Diagnóstico Veterinario del Instituto de Medicina Veterinaria, procedente de un perro joven con síntomas clínicos de parvovirosis canina (12). El virus fue sometido a 53 pases en la línea celular de riñón de perro (MDCK) para asegurar su modificación y 27 pases sobre cultivo de línea de riñón de gato (CRFK) para asegurar su estabilización.
Propagación del virus: Para la multiplicación viral se empleó la línea celular CRFK, (ATCC-CCL-94), obtenida y certificada por la ATCC (American Type Culture Collection) en el pase 180. Las células fueron cultivadas en medio mínimo esencial (Gibco) con glutamina y aminoácidos no esenciales, suplementado con caldo triptosa fosfato (Difco) al 10%, L -glutamina al 1% (Gibco), bicarbonato de sodio 1% (ICN) y s uero fetal bovino al 10% (SIGMA). Para la amplificación del aislamiento de parvovirus canino se tomó un bulbo liofilizado (Lote 1203002) conservado a -70ºC y se reconstituyó en 1 mL de medio mínimo esencial, luego se inoculó una dilución de 10-3 en frascos roux plásticos para cultivo celular de 25 cm2, sembrados previamente con la línea celular de CRFK en volumen de 1 mL. Los frascos se colocaron en la incubadora a 37 ºC durante 4 días. Se realizó la observación diaria hasta la aparición del efecto citopático caracterizado por redondeamiento celular a partir del tercer día; cuando alcanzó el 80% o más se procedió a realizar la colecta y se almacenó. Se tomó una alícuota para ser evaluada conservando el resto a -70ºC.
Extracción del ADN: Las células infectadas con la cepa de VPC-2 se centrifugaron a 1500 g durante un minuto a 4ºC. El precipitado celular fue incubado con proteinasa K a una concentración final de 250 µg/ml en tampón de lisis (Promega, EE.UU ) a 56ºC con agitación para garantizar la lisis completa de las células. A la muestra lisada se le añadieron esferas magnéticas y un tampón para la unión de las mismas con el ADN (Promega , EE.UU). Al tubo que contenía la mezcla de lisado y esferas se le aplicó un separador magnético durante cuatro minutos, según recomendaciones del fabricante. Este procedimiento garantiza que las esferas magnéticas unidas al ADN queden aglutinadas en la parte del tubo en contacto con el separador magnético y el resto de la solución sea eliminada. El tubo se retiró del separador magnético y se le añadió un tampón de lavado (500 µL de etanol al 70%). Se agitó por inversión y se eliminó la solución. Luego se añadió 200 µL de agua destilada estéril. Se retiró el separador para mezclar bien las esferas con el tampón de resuspensión de ADN. La solución se incubó durante 10 minutos con agitación a temperatura ambiente para eluir el ADN unido a las esferas. El ADN extraído se transfirió a un tubo limpio y fue conservado a -20 ºC hasta su uso.
Análisis del ADN viral: El ADN fue amplificado mediante la técnica de reacción en cadena de la polimerasa (RCP), para lo cual fueron diseñados 12 oligonucleótidos específicos que abarcaron todo el genoma viral. Para esto se tuvo en cuenta las zonas más conservadas del mismo en análisis realizado al alineamiento de secuencias reportadas de este virus y publicadas en las bases de datos existentes (13). Se realizó el diseño de los cebadores de forma tal que se amplificó el ADN genómico viral en 6 fragmentos de aproximadamente 1000 nucleótidos (nt) de longitud cada uno y que se solaparon en 100 nt entre si. Los cebadores fueron diseñados en los laboratorios INGENASA (España) y su síntesis se realizó por la casa comercial INVITROGEN. Las secuencias de los cebadores se muestran en la Tabla 1.
La posición de las secuencias en la tabla refiere su ubicación en el genoma viral. Los cebadores fueron diseñados en sentido 5' a 3'.
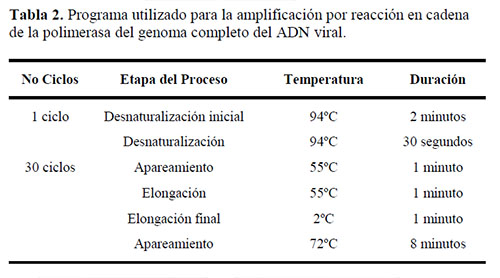
Los fragmentos fueron amplificados por RCP. Cada reacción se llevó a cabo en un volumen final de 25 µL, incluyendo aproximadamente 500 ng de ADN en 1 µL de muestra y 12,5 µL de la mezcla de reactivos (PCR Master Mix 2X, Promega, EE.UU). Se emplearon 25 pmol de oligos por reacción. La amplificación se llevó a cabo en un termociclador Perkin Elmer (GeneAmp PCR System 2400). Los productos amplificados se visualizaron mediante electroforesis en gel de agarosa al 0,8% teñido con bromuro de Etidio (0,5 µg/mL). En la preparación de las muestras se adicionó como colorante bromofenol azul. Se incluyeron controles negativos de la reacción de RCP y el marcador de peso molecular DNA ladder (Promega. EE.UU). Las muestras se corrieron a 120V durante 30 min. En cada una de las reacciones se incluyeron controles positivos y de reactivos. Las condiciones de amplificación se describen en la Tabla 2.
]]>
Todos los fragmentos amplificados se diluyeron hasta una concentración final de 50 ng/µL y su purificación y secuenciación se realizó utilizando el servicio de Macrogen, Inc (Corea). Se emplearon al menos uno o dos de los mismos oligonucleótidos descritos anteriormente a una concentración de 5 pmol/µL. En los casos necesarios se diseñó un oligonucleótido interno para completar la secuencia los cuales se obtuvieron también por la casa comercial INVITROGEN.
Las secuencias de nucleótidos se tradujeron a aminoácidos en el programa MEGA 3.1 (14). Se realizó una búsqueda de homología inicialmente con la secuencia disponible de una cepa de referencia de VPC-2 en la base datos Gen Bank cuyo número de acceso es: NC_001539 y posteriormente se amplió la comparación con secuencias de cepas y aislados de VPC-2 conocidos en la base de datos del NCBI (Centro Nacional para Información de Biotecnología) utilizando el programa BLAST (Basic Local Alignment Search Tool, NCBI) (15).
RESULTADOS Y DISCUSIÓN
En el presente estudio se utilizó la técnica de RCP para la detección del VPC- 2 a partir de células infectadas; se logró exitosamente aislar, amplificar y secuenciar el material genético completo del aislamiento cubano.
Fueron detectados cambios en la secuencia aminoacídica del aislamiento cubano localizados en el extremo N-terminal de la proteína NS1 y en la proteína VP2 como resultado del análisis de comparación de este aislamiento con la cepa de referencia VPC-2 depositada en la base de datos del Gen Bank y otras secuencias de cepas y aislamientos localizados en las base de datos NCBI.
Las secuencias de aminoácidos de las proteínas NS1 y VP2 del aislamiento cubano se muestran a continuación:
1-Secuencia de aminoácidos de la proteína NS1 CPV-Cuba
MSGNQYGEVMEGVNWLKKHAENEAFSFVFKCDNVQLNGKDVRWNNYTKPIQEELTSLIRGAQTAMDQTEEEEMDWESEVDSLAKKQVQTFDALIKKCLFEVFVSKNIEPNECVWFIQHEWG
]]> KDQGHCHVLLHSNLQQATGKWLRRQMNMYWSRWLVTLCSVNLTPTEKIKLREIAEDSEWVTILTYRHKQTKKDYVKMVHFGNMIAYYFLTKKKIVHMTKESGYFLSTDSGWKFNFMKYQDRQIVSTLYTEMKPETVETTTTAQETKRGRIQTKKEVSIKCTLRDLVSKRVTSPEDWMMLQPDSYIEMMAQPGGENLLKNTLEICTLTLARTKTAFELILEKADNTKLTNFDLANSRTCQIFRMHGWNWIKV
CHAIAVLNRQGGKRNVLFHGPASTGKSIIAQAIAQAVGNVGCYNAANVNFPFNDCTNKNLIWIEEAGNFGQQVNQFKAICSGQTIRIDQKGKGSKQIEPTPVIMTTNENITIVRIGCEERPEHTQPIRD
RMNIKLVCKLPGDGLVDKEEWPLICAWLVKHGYESTMANYTHHWGKVPEWDENWAEPKIQEGINSPGCKDLETQAASNPQSQDQVLTPLTPDVVDLALEPWSTPDTPIAETANQQSNQLGVTHK
DVQAPTWSEIEADLRAFTSEQLEEDFRDDLD*
Se señala en rojo el aminoácido cambiado en la secuencia aminoacídica de la cepa de VPC-2 cubana con respecto a las secuencias de otros aislamientos y cepas analizadas depositadas en las bases de datos.
2- Secuencia de aminoácidos de la proteína VP2 CPV-Cuba
MSDGAVQPDGGQPAVRNERATGSGNGSGGGGGGGSGGVGISTGTFNNQTEFKFLENGWVEITANSSRLVHLNMPESENYRRVVVNNMDKTAVNGNMALDDIHAQIVTPWSLVDANAWGVWFNP
GDWQVNTMSELHLVSFEQEIFNVVLKTVSESATQPPTKVYNNDLTASLMVALDSNNTMPFTPAAMRSETLGFYPWKPTIPTPWRYYFQWDRTLIPSHTGTSGTPTNIYHGTDPDDVQFYTIENSV
PVHLLTDEFATGTFFFDCKPCRLTHTWQTNRALGLPPFLNSLPQSEGATNFGDIGVQQDKRRGVTQMGNTNYITEATIMRPAEVGYSAPYYSFEASTQGPFKTPIAAGRGGAQTDENQAADGN
]]> PRYAFGRQGQKTTTTGETPERFTYIAHQDTGRYPEGDWIQNINFNLPVTNDNVLLPTDPIGGKTGINYTNIFNTYGPLTALNNVPPVYPNGQIWDKEFDTDLKPRLHVNAPFVCQNNCPGQLFVKVANLTNEYDDASANMSRIVTYSDFWWKGKLVFKAKLRASHTWNPIQQMSINVDNQFNYVPSNIGGMKIVYEKSQLAPRKLY
Se señala en rojo los aminoácidos cambiados en el aislamiento de VPC-2 cubano.
Producto de la alineación del aislamiento de VPC-2 cubano con la cepa de referencia de VPC-2 depositada en la base de datos del Gen Bank fueron observados cambios de nucleótidos y de los aminoácidos correspondientes; sólo tres de los seis cambios de nucleótidos detectados dan lugar a cambios en la estructura primaria de la proteína (Tabla 3).
El grado de homología de la secuencia de nucleótidos del aislamiento cubano de VPC-2, con respecto a secuencias de cepas y aislamientos conocidos de VPC-2 depositados en la base de datos de NCBI, se muestra en la Tabla 4. Los dos primeros aislamientos y la primera cepa listados solo presentan un cambio de nucleótido (nt 23) con respecto al aislamiento de VPC-2 cubano y pertenecen al grupo VPC-2.
La alta variabilidad de la proteína viral VP2 de VPC-2 es la causa principal del amplio rango de hospedadores y de las reacciones cruzadas entre las diferentes variantes que existen. En la actualidad, la secuenciación de esta proteína ha permitido identificar las tres variantes de VPC-2 (2a, 2by 2c) (16). Por esta razón para determinar el tipo de parvovirus a la que pertenecía el aislamiento cubano, se compararon las variaciones de aminoácidos en la proteína VP2 en las distintas variantes virales: VPC-2 original, VPC-2a, VPC-2b, VPC-2c, con respecto a la secuencia aminoacídica de la proteína VP2 del aislamiento cubano (Tabla 5).
Se puede apreciar que los aminoácidos de la proteína VP2 correspondientes a la variante VPC-2 original, tienen 100% de identidad con los aminoácidos de la proteína VP2 del aislamiento cubano, por lo que se puede concluir que el aislamiento cubano es de tipo VPC-2. Este resultado tiene una gran importancia en la selección de un candidato vacunal para la obtención de una vacuna viva atenuada contra la parvovirosis canina, ya que la prevención y el control de esta enfermedad se basa fundamentalmente en la vacunación.
Existen varios tipos de vacunas para proteger a los perros contra esta enfermedad. En este sentido son las vacunas vivas atenuadas las que proporcionan una mayor protección y duración de la inmunidad. Este tipo de vacunas en su mayoría son producidas con las cepas VPC-2 y algunas son fabricadas con la variante 2b.
Las cepas atenuadas de VPC-2 provienen de pasajes repetidos de los virus en cultivo celular. No se conoce el mecanismo que produce la mutación y la atenuación del virus, pero los virus vacunales se eliminan en títulos bajos por las heces, lo que sugiere que la ausencia de enteritis se debe a la disminución de la replicación viral en el intestino.
Desde que el virus tipo 2 fue enteramente reemplazado por los virus 2a, 2b y ahora 2c, producto a una mayor resistencia, amplio rango de hospederos y mayor patogenicidad, existe una preocupación mundial sobre el nivel de protección que ofrecen las vacunas atenuadas del tipo 2 original (17).
]]> Sin embargo, varios autores señalan que existe suficiente protección cruzada entre las cepas 2 y las nuevas variantes virales frente a la infección con VPC-2, lo que supone pensar que las vacunas siguen siendo vigentes y protegen contra las nuevas variantes que han aparecido de VPC-2. Greenwood y col. (1995) (18) demostraron que vacunas atenuadas con VPC-2, son capaces de proteger a perros contra desafíos de campo de cepas 2a y 2b. Spibey y col. (2008) también demostraron que perros vacunados con una sola dosis de una vacuna comercial con VPC-2 (Nobivac – Intervet), estuvieron protegidos contra los desafíos con el tipo 2c salvaje (19).A pesar de las diferencias entre la cepa original tipo 2 y las variantes 2a, 2b y 2c, los perros vacunados con una vacuna del tipo 2, llegan a generar una fuerte respuesta inmune contra VPC-2 y están plenamente protegidos (20).
En el presente estudio se realizó la caracterización molecular de un aislado cubano de parvovirus canino tipo 2 donde se evidenció que la misma es del tipo VPC-2, y aunque exista una gran controversia sobre el nivel de protección que ofrecen las vacunas atenuadas del tipo 2 original, varias vacunas comerciales son elaboradas actualmente a partir de este tipo de cepas, proporcionando una excelente protección y una larga duración de la inmunidad.
El uso de vacunas eficaces ha sido responsable del control y de la erradicación de numerosas enfermedades infecciosas, entre ellas la parvovirosis canina, y se han convertido en la mejor herramienta al alcance del veterinario clínico para la reducción de la morbilidad y mortalidad en los animales domésticos.
REFERENCIAS
1. Hoelzer K, Parrish, C. The emergence of parvoviruses of carnivores. Vet Res 2010;41(6):39. doi: 10.1051/vetres/2010011.
2. Castro TX, Costa EM, Leite JP, Labarthe NV, Garcia RC. Detection of the new variant CPV-2c. Braz J Microbiol 2010;41(4):1093-8.
]]>3. Cavalli A, Martella V, Desario C, Camero M, Bellacicco A, De Palo P, et al Evaluation of the antigenic relationships among canine parvovirus type 2 variants. Clin Vacc Immunol 2008;15(3):534-9.
4. Hoelzer K, Shackelton LA, Parrish CR, Holmes EC. Phylogenetic analysis reveals the emergence, evolution and dispersal of carnivore parvoviruses. J Gen Virol 2008;89(9):2280-9.
5. Maya L, Calleros L, Francia L, Hernández M, Iraola G, Panzera Y, et al. Phylodynamics analysis of canine parvovirus in Uruguay: evidence of two successive invasions by different variants. Arch Virol 2013;158(6):1133-41.
6. Calderón MG, Romanutti C, D'Antuono A, Keller L, Mattion N, La Torre J. Evolution of Canine Parvovirus in Argentina between years 2003 and 2010: CPV2c has become the predominant variant affecting the domestic dog population. Virus Res 2011;157(1):106-10.
7. De Cramer KG, Stylianides E, Van Vuuren M. Efficacy of vaccination at 4 and 6 weeks in the control of canine parvovirus. Vet Microbiol 2011;149(1-2):126-32.
]]>8. Merino N, Rodríguez J, Joa R, Achon I, Cabo JL. Reporte de un brote de gastroenteritis hemorrágica canina. Rev Cub Cienc Ve. 1982;13(2):223-4.
9. López R. Parvovirosis canina. La Habana: Universidad Agraria de la Habana; 1998.
10. Boffil P, Ramírez W, Montañez J, Reinaldo G, Perez M, Percedo M, Aveledo MA. Enfermedades Infecciosas de los animales. Enfermedades producidas por virus. Tomo II. La Habana: Editorial Félix Varela; 2007. p.341-62.
11. Puentes R. Parvovirosis Canina: situación actual y protección de vacunas contra las nuevas variantes virales circulantes en la región. Veterinaria 2012;48(185):5-10.
12. Barrios M, Luya M, Reyna A, Lorenzo M, Achon I. Aislamiento de parvovirus de un perro con gastroenteritis hemorrágica. Rev Cub Cienc Vet 1989;20(4):297-304.
]]>13. Reed PA, Jones EV, Miller TJ. Nucleotide Sequence and Genome Organization of Canine Parvovirus. J Virol. 1988;62:266-76.
14. Kumar S, Tamura K, Nei M. MEGA3: Integrated software for Molecular Evolutionary Genetics Analysis and sequence alignment. Briefings in Bioinformatics. 2004;5:150-63.
15. Zhang Z, Schwartz S, Wagner L, Webb Miller W. A greedy algorithm for aligning DNA sequences. J Comput Biol. 2000;7(1-2):203-14.
16. Truyen U. Evolution of canine parvovirus – A need for new vaccines? Microbiol 2006;117:9-13.
17. Pratelli A, Cavalli A, Normanno G, De Palma MG, Pastorelli G, Martella V, Buonavoglia C. Immunization of pups with maternally derived antibodies to canine parvovirus (CPV) using a modified live variant (CPV-2b). J Vet Med B Infect Dis Vet Public Health. 2000;47:273-6.
]]>18. Greenwood NM, Chalmers WSK, Baxendale W, Thompson H. Comparison of isolates of canine parvovirus by restriction enzyme analysis and vaccine efficacy against field strains. Vet Rec 1995;136:63-7.
19. Spibey N, Greenwood NM, Sutton D, Chalmers WS, Tarpey I. Canine parvovirus type 2 vaccine protects against virulent challenge with type 2c virus. Vet. Microbiol. 2008;128(1-2):48-55.
20. Truyen U, Everman J, Vieler E, Parrish C. Evolution of canine parvovirus involved loss and gain of feline host range. Virology 1996;215:186-9.
Recibido: Febrero de 2015 Aceptado: Mayo de 2015
]]>