
Influencia del medio de cultivo sobre la cinética de crecimiento y expresión de la proteína recombinante Rv2626c de Mycobacterium tuberculosis H37Rv expresada en Streptomyces lividans TK24
Influence of the culture medium on the kinetics of growth and expression of the recombinant protein Rv2626c of Mycobacterium tuberculosis H37Rv expressed in Streptomyces lividans TK24
Emmanuel N. King-Batsios,1,3* Anairis Pujol-García1**, Beatriz Tamargo-Santos,2 Gretel Marrero-Trujillo,1 Marcos J. Fontanies-Hernández,1 Kirenia Blain-Torres,3 Luis Riverón-Martínez,3 Caridad Zayas-Vignier,3 Reinaldo Acevedo-Grogues,3 V. Gustavo Sierra-González4
1 Departamento de Biotecnología e Inmunología, Instituto de Farmacia y Alimentos, (IFAL). Universidad de la Habana, La Habana, Cuba.
2 Escuela Latinoamericana de Ciencias Médicas, La Habana, Cuba
]]> 3 Instituto Finlay de Vacunas. La Habana, Cuba.4 BioCubaFarma, Grupo de las Industrias Biotecnológicas y Farmacéuticas de Cuba. La Habana, Cuba.
email: enkb2005@gmail.com; anapujol@ifal.uh.cu
* Alumno de Doctorado. MSc. Licenciado en Farmacia.
** Profesora de Microbiología. Licenciada en Biología.
RESUMEN
Streptomyces lividans, ha ganado gran atención en los últimos tiempos, como vector de expresión y producción de proteínas de Mycobacterium tuberculosis de interés biomédico, como alternativa a su obtención tradicional en E. coli. La proteína Rv2626c, Proteína de Respuesta Hipóxica 1, es codificada por el gen Rv2626c (hrp1) de M. tuberculosis, perteneciente al regulón de la fase de latencia DosR. Esta proteína se sobre-expresa en la fase de latencia de la tuberculosis bajo condiciones de estrés como hipoxia y bajos niveles, de óxido nítrico. Se ha demostrado la inmunogenicidad y capacidad de esta proteína, de inducir citocinas características del patrón Th-1, tales como el interferón gamma. Por ello, nuestro grupo logró la obtención de Rv2626c por la tecnología del ADN recombinante usando como cepa hospedera Streptomyces lividans TK24. Con el objetivo de aumentar el nivel de expresión de la proteína recombinante, rRv2626c en este trabajo se ensayaron diferentes medios de cultivo, evaluando el crecimiento de la cepa transformada en condiciones de zaranda. Se determinó la cinética de crecimiento en el medio definido, formulado industrialmente en el Centro Nacional de Biopreparados: caldo Triptona Soya (TSB-BioCen) y en medio de cultivo equivalente preparado en el laboratorio. Para establecer la cinética de crecimiento, se utilizó el cálculo del peso seco y la determinación de la concentración de proteínas totales por la técnica de ácido bicinconinico (BCA) a diferentes tiempos del cultivo. Posteriormente, se identificó la proteína clonada mediante SDS-PAGE y Western Blotting, así como los niveles de expresión mediante análisis densitométrico. Los resultados indican que se alcanzaron los máximos niveles de densidad celular a las 36 h de cultivo y los más altos niveles de expresión proteica total y específica entre las 42 y 54 h. Con el medio químicamente definido TSB-Biocen preformulado en lugar del preparado en el laboratorio partiendo de los componentes, se logró reducir el tiempo óptimo para la expresión-secreción de la proteína rv2626c de 96 a 54 h. Los mejores resultados en la promoción de la expresión de la proteína recombinante se lograron con el medio definido TSB-BioCen, a las 48 h con 8,5% de rendimiento específico, superando en más de 10 veces los niveles de crecimiento celular obtenidos con el medio elaborado en el laboratorio y más de dos veces los niveles de secreción de la proteína recombinante.
Palabras clave: Streptomyces lividans, medio de cultivo, Mycobacterium tuberculosis, proteína de respuesta hipóxica, Rv2626c.
The use of Streptomyces as a bacterial cell factory for the secretory production of bio-active Mycobacterium tuberculosis proteins have gained a lot of attention in recent years, as a convenient alternative to the traditionally used Escherichia coli. The protein Rv2626c protein, also known as Hypoxic Response Protein 1 (HRP1), is encoded by the gene rv2626c (hrp1) of M. tuberculosis which belongs to the Dormancy Safety Regulator (DosR) regulon. This protein is over-expressed during the latency phase of tuberculosis under stress related conditions such as hypoxia and low, non-toxic, levels of nitric oxide and, the immunogenicity and ability to induce cytokines characteristic of the Th-1 pattern of this protein, such as gamma interferon, have been demonstrated. On this basis, our working group, succeeded in obtaining rRv2626c via recombinant DNA technology using Streptomyces lividans TK24 as the host cell. To improve the expression level of the protein, different culture media were used to evaluate the growth of the transformed strain in shaken flask conditions. Growth kinetic for the recombinant strain was evaluated in defined media of preformulated tryptic soya broth (TSB-Biocen), through the determination of dry weight as well as total protein concentration by Bicinconinic acid assay (BCA). Protein identification was done by SDS-PAGE, Western Blot and its expression level by densitometric analysis. Our results indicated a maximal cell density at 36 h of culture, with higher concentration of total and specific protein at 42-54 h in comparison with previous media used. With the chemically defined media a preformulated TSB-Biocen rather than individual components, culture time for expression/secretion of rRv2626c was reduced from 96 h to 54 h. The best results in expression-secretion levels of rv2626c protein were obtained with the TSB-Biocen defined media at 48 h of culture with 8.5% of specific yield. More than 10 fold increase in cellular growth and more than 2 fold increase in specific yield.
Keywords: Streptomyces lividans, culture media, Mycobacterium tuberculosis, Hypoxic Response Protein 1, Rv2626c.
INTRODUCCIÓN
Streptomyces lividans, ha ganado gran atención en los últimos tiempos, como vector de expresión y producción de proteínas de Mycobacterium tuberculosis (Mtb) de interés biomédico, como una alternativa eficaz y eficiente al sistema tradicional de Escherichia coli.
Aunque la E. coli ha sido el hospedero, por excelencia, más empleado para la obtención de antígenos proteicos de otros microorganismos incluyendo Mtb (1-3), debido a que existen una amplia gama de conocimientos, informaciones y herramientas para su manejo genético, este sistema presenta limitaciones como problemas graves de contaminación con endotoxina o contaminantes residuales de E. coli, los cuales pudieran inducir la producción de citocinas no-específicas. Además, muchas proteínas recombinantes obtenidas en E. coli se acumulan inactivas en cuerpos de inclusión, lo cual dificulta los procesos de replegamiento de estas proteínas en su conformación nativa y puede afectar su actividad biológica y hace que los procesos de purificación sean complejos y extensos, con un costo elevado.
Streptomyces son bacterias aeróbicas Gram-positivas provenientes de la tierra que, al igual que las micobacterias (4), pertenecen al orden Actinomycetales. La mayoría de las especies de Streptomyces son microorganismos no patógenos, tienen un genoma con alto contenido de G + C en su ADN y son bien conocidos por su alta capacidad de secretar grandes cantidades de metabolitos secundarios tales como: antibióticos, fungicidas, herbicidas o enzimas extracelulares (5). Su probada excelencia en la capacidad de expresión, unido al hecho de que las proteínas clonadas son secretadas al medio de cultivo, convierten a Streptomyces en un hospedero atractivo para la expresión de proteínas recombinantes de Mtb.
Nuestro grupo de trabajo ha clonado el gen hrp1 de Mtb en S. lividans cepa TK24 provisto con la secuencia codificadora 3'-Strep-tag®II y bajo el control de las secuencias reguladoras del inhibidor subtilisin S. venezuelae CBS762.70 (vsi) (6), lográndose de esta manera la expresión y secreción de la proteína rRv2626c de Mtb, en las condiciones de cultivo descritas por Pimienta y col. en 2007 (7).
]]> Dentro de los Streptomyces, se seleccionó S. lividans TK24 (derivado de S. lividans 66) para el clonaje y expresión de la proteína rRv2626c, pues la misma carece de un sistema de restricción inminente, presente en otras especies y tiene actividad proteolítica endógena más baja que otras especies de Streptomyces. Además, S. lividans ha demostrado ser, repetidamente, un valioso hospedero en la secreción de proteínas heterólogas tanto procariotas como eucariotas y numerosos reportes han mostrado que ciertas proteínas, que no han podido ser obtenidas en E. coli, son producidas eficientemente por S. lividans.Por otra parte, el empleo de Streptomyces evita la eliminación de endotoxinas bacterianas, presentes en la membrana externa de las bacterias Gram-negativas como E. coli (8, 9). La cantidad total de rRV2626c (Strep-tagged Rv2626c) secretada por S. lividans, obtenida por Ayala y col. en 2013 (6), empleando el medio de cultivo caldo triptona soya (TSB, siglas en inglés), compuesto por (triptona 1,7%; harina de soya cubana 0,3%; glucosa 1%; NaCL 0,5%; K2HPO4 0,25%) (6), preparado en el laboratorio a partir de sus componentes individuales, fue aproximadamente 4 mg de proteína/L de sobrenadante de cultivo fermentado (6). Aunque este resultado fue alentador, era necesario aumentar la cantidad de proteína secretada, por ello se decidió evaluar el medio de cultivo TSB formulado industrialmente en el Centro Nacional de Biopreparados de Cuba (BioCen), que contiene entre sus ingredientes el hidrolizado enzimático de caseína.
Por tal razón, el objetivo de este trabajo fue el estudio comparativo de la influencia de medio de cultivo sobre la cinética de crecimiento y la expresión de la proteína recombinante rRv2626c de Mtb H37Rv expresada en S. lividans TK24. Específicamente, comparamos los medios TSB preparado en laboratorio y TSB formulado por BioCen.
MATERIALES Y MÉTODOS
Cepas bacterianas
Se utilizó la cepa de S. lividans TK24, procedente de John Innes Foundation, Norwich, UK y la cepa S. lividans TK24 transformada con el plásmido [pIJ-pvsi-rv2626c-Strep-tag II], ambas conservadas como suspensiones de esporas o de micelio por congelación a 70ºC en glicerol al 20%.
Medios y condiciones de cultivo
Para obtener las suspensiones de esporas de las cepas de S. lividans TK24 salvaje y transformada, se utilizó el medio de cultivo solido manitol-soya al 2%, compuesto por: agar, harina de soya, manitol, todos al 2% y agua csp., para el crecimiento de la cepa transformada se adiciona al medio tiostreptona a una concentración de 50 µg/mL.
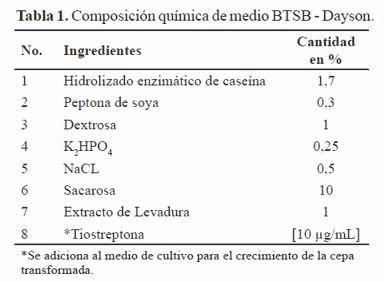
Para propagar las cepas de S. lividans TK24 [pIJ-pvsi-rv2626c-Strep-tag II] y S. lividans TK24, se utilizó el medio Caldo Triptona-Soya, suplementado con sacarosa y extracto de levadura, de la casa comercial Merck (Alemania) (BTSB- Dayson) pH 7,2 (Tabla 1) (10).
]]>
Los medios de cultivo ensayados para la producción y expresión de la proteína recombinante fueron:1) medio líquido TSB (10) pH 7,2 (preparado con los ingredientes individuales en el laboratorio según se describe en la Tabla 2, (TSB-Lab); 2) medio líquido TSB-BioCen pH 7,2, preparado a 30 g/L según recomendaciones del fabricante (Tabla 3). Ambos medios fueron esterilizados en autoclave durante 20 minutos, a 121ºC y una atmósfera de presión. Condiciones de cultivo de S. lividans TK24 [pIJ-pvsi-rv2626c-Strep-tag II] y expresión de la proteína rRv2626c en zaranda Una alícuota de 104 esporas se inoculó en 25 mL del medio BTSB en enlermeyers de 125 mL y se incubó por 72 h a 30ºC en una zaranda orbital termostatada (Info HT) con agitación de 240 rpm. Posteriormente, el 2% del cultivo fue inoculado en 100 mL de los dos medios de cultivos evaluados para la producción y expresión de la proteína recombinante (TSB preparado en el laboratorio y TSB-BioCen), en enlermeyers de 500 mL y se incubó con agitación de 240 rpm, en zaranda orbital termostatada a 28ºC durante 96 h (11).
Muestreo: Se tomó muestras del cultivo cada 6 h, a partir de las 24 h hasta las 60 h y después cada 12 h hasta las 96 h.
Determinación de la cinética de crecimiento de rRv2626c en los medios de cultivo evaluados
Para determinar la cinética de crecimiento de rRv2626c se utilizó el cálculo del peso seco. Para ello se extrajo 1 mL del cultivo en cada tiempo de muestreo en viales eppendorff de 1,5 mL de volumen (los viales vacíos fueron pesados previamente, hasta peso constante, en balanza analítica). El micelio (biomasa) fue separado del sobrenadante por centrifugación a 4700 g durante 5 min. Posteriormente, las biomasas se secaron a 60°C por 12 h en una estufa. Después se pesaron los viales con la biomasa seca, en balanza analítica hasta alcanzar peso constante, para lo cual los viales se colocaron en una desecadora durante diez min después de cada pesada.
El cálculo del peso seco de la biomasa se realizó por sustracción del peso de cada vial al peso del vial correspondiente que contenía la biomasa y se expresó en mg/mL. Se realizaron cinco réplicas de cada determinación, considerando no extraer más del 10% del contenido del cultivo para no afectar la relación entre el crecimiento de esta bacteria filamentosa y la producción del metabolito de interés (11).
Determinación de proteínas totales
La concentración de proteínas totales fue determinada por el método del ácido bicinconínico utilizando el estuche comercial PierceTM BCA Protein Assay Kit (Thermo Scientific, EUA) según las recomendaciones descritas por el fabricante. Se aplicaron 20 µL/pocillo de la muestra (sobrenadante de cultivo colectado en los diferentes tiempos) y de las diluciones doble seriadas de una solución patrón de albúmina de suero bovina (BSA por sus siglas en inglés) desde 2 hasta 0,025 mg/mL para hacer la curva de calibración. Luego se añadieron 200 µL/pocillo de la mezcla de reactivos, que contenía: solución alcalina de ácido bicinconínico (Reactivo A) y sulfato cúprico (Reactivo B) en una proporción 50+1 (v/v). Se incubó a 37°C en estufa durante 30 min y se determinó la absorbancia a una longitud de onda de 540 nm, en un lector de microplacas Multiskan (Thermo Scientific, EUA). Usando el programa Microsoft Excel se realizó una regresión lineal y se obtuvo la curva de calibración a partir de los valores de absorbancia. Las muestras se calcularon usando la curva de BSA y el resultado se expresó en mg/mL de proteínas.
]]> Detección e identificación de la proteína rRv2626cElectroforesis en gel de poliacrilamida. Se realizó la electroforesis en gel de poliacrilamida en presencia de duodecil sulfato de sodio (SDS/PAGE), en condiciones reductoras, según la metodología descrita por Laemmli (12), empleando un gel al 12,5% de acrilamida/bisacrilamida. El gel contenía en su composición cada uno de los reactivos y soluciones necesarios, en las cantidades estipuladas de acuerdo a las normativas de trabajo del laboratorio. Preparación de las muestras. Las muestras (sobrenadante de cultivo colectado en los diferentes tiempos) fueron preparadas a una concentración de 1 µg/µL. Las diluciones de las muestras se realizaron en tampón muestra Laemmli utilizando como agente reductor: DTT (ditiotreitol). Como patrón se utilizó Strep-Tag Protein Ladder de 100-16 kDa. (IBA GmbH, Alemania).
Corrida electroforética. La corrida electroforética se realizó en un equipo para electroforesis vertical (Bio-Rad, EUA), conectado a una fuente de la misma compañía. Se empleó un voltaje de 120 V y corriente libre. Este ensayo se realizó siguiendo lo establecido en los Procedimientos Normalizados de Operaciones, del laboratorio.
Tinción con nitrato de plata. Una vez finalizada la corrida electroforética, se extrajo el gel y se mantuvo en solución fijadora (metanol, ácido acético 5% y agua) durante 1 h a 20-25°C con agitación constante. Transcurrido este tiempo se lavó el gel tres veces durante 20 min con solución de etanol al 50%. Concluido este paso se mantuvo un minuto en solución de sensibilización (solución de tiosulfato de sodio pentahidratado 0,2g/L). Seguidamente, se lavó con abundante agua tres veces durante 20 seg exactamente. Posteriormente se inició la tinción adicionando al gel una solución que contenía nitrato de plata y formaldehído 37% durante 20 min. Le siguieron dos lavados con agua durante 20 seg cada uno, para seguidamente incubar el gel en la solución reveladora de carbonato de sodio, formaldehído 37% y Na2S2O3 hasta la completa visualización de las bandas. A continuación, se hicieron dos lavados con agua durante dos min cada vez y después se mantuvo el gel en solución fijadora durante 10 min. Por último, se realizó un lavado con metanol al 50% durante 20 min.
Identificación de la proteína rRv2626c. Para la identificación de la proteína rRv2626c se utilizó el análisis por Western Blot. Para ello, se siguió el protocolo descrito por el fabricante en Strep-tag® detection in Western blots (IBA GmbH, Alemania). Después de la corrida electroforética, se procedió a la transferencia semi-seca de las proteínas a una membrana de nitrocelulosa Hybond-C extra (Bio-Rad, EUA) con porosidad de 0,45 µm durante 2 h a 25ºC, con un voltaje de 300 V y corriente libre, empleando una cámara Western Blot (Pharmacia, Suecia). Cada perfil electroforético transferido se visualizó mediante el empleo de la solución de rojo ponceau. Posteriormente, se bloquearon los sitios libres de la membrana con 20 mL de tampón bloqueo-PBS (4 mM KH2PO4 pH 7,4, 16 mM Na2HPO4,115 mM NaCl con 3% BSA y 0,5% v/v Tween 20) y se incubó 1 h, concluida la incubación se lavó la membrana tres veces con tampón PBS-T20 (4 mM KH2PO4 pH 7,4, 16 mM Na2HPO4, 115 mM NaCl con 0,1 % v/v Tween 20), cada paso de lavado, durante 5 min. Después del último lavado se incubó la membrana 1 h en 10 mL de tampón PBS-Tween que contenía 2,5 µL del conjugado Strep-Tactin:HRP (1:4000). Posteriormente, la membrana se lavó dos veces con tampón PBS-Tween y a continuación se procedió a otros dos lavados con tampón PBS (4 mM KH2PO4 pH 7.4, 16 mM Na2HPO4,115 mM NaCl), realizando cada paso de lavado durante 1 min. Finalmente, se colocó la membrana en 50 mL de tampón PBS, que contenía 0,025 g de Diaminobencidina y 50 µL de H2O2 30%, hasta visualizar las bandas. Todas las incubaciones y los lavados se realizaron a una temperatura de 20-25°C y con ligera agitación.
Determinación de los niveles de expresión/secreción de rRv2626c
Análisis densitométrico. El gel obtenido de la electroforesis después de teñido con nitrato de plata se analizó en el densitómetro GS-800 (Bio-Rad, EUA) utilizando el programa Quantity One. Con este programa se determinó la masa molecular (MM) de cada una de las bandas de la proteína en estudio, observadas en el SDS-PAGE, a través de una regresión lineal con el patrón de masa molecular empleado.
Análisis estadístico
Para los análisis estadísticos y el procesamiento de los datos se utilizó el Programa para IBM SPSS Statistic V.22. Para demostrar la normalidad de los datos se utilizó el test de Kolmogorov-Smirnov (α=0,05). La estadística descriptiva incluyó, la media, la desviación estándar y el error estándar de la media. Se utilizó un ANOVA de dos vías complementado con el Test de Bonferroni para determinar diferencias entre los medios de cultivo y entre los diferentes tiempos del muestreo. Se construyó una curva de regresión líneal entre las concentraciones y las densidades ópticas y se estimó el coeficiente de determinación (R2). Fue usado para todos los cálculos un intervalo de confianza del 95%. En la elaboración de los gráficos se utilizaron las herramientas del Paquete Microsoft Excel de Microsoft Office V.2010.
]]> RESULTADOS Y DISCUSIÓN
Debido a que las bacterias son pequeñas, la única forma en que se pueden medir los eventos fisiológicos y bioquímicos es trabajar con las poblaciones. Para que los eventos que se miden en la población reflejen fielmente lo que está sucediendo en la célula individual, todas o la mayoría de las células deben estar en las mismas condiciones fisiológicas. Para estudios del metabolismo primario, esto generalmente se logra cuando el crecimiento del cultivo es exponencial.
Una característica de Streptomyces que hace que este tipo de estudio sea muy difícil es que los mismos crecen por elongación en la punta del micelio y por ramificación. Esto permite el logro de un crecimiento exponencial por micelio joven. Sin embargo, la homogeneidad fisiológica no se mantiene fácilmente a lo largo de muchas generaciones porque, las partes más antiguas y centrales del micelio pueden llegar a tener un límite de nutrientes.
Este problema se ve exacerbado por la tendencia de las microcolonias, inicialmente separadas, a agregarse en grupos más grandes en cultivos líquidos. Especies como S. lividans forman grupos de micelios densos y grandes a menos que se usen medios o condiciones de crecimiento especiales (11).
Se recomienda que mientras más complejo sea el medio, más rápida será la tasa de crecimiento y menos probabilidad de aglomeración de las células Para obtener un crecimiento balanceado en medio líquido donde cada componente celular es aumentado por el mismo factor de incremento para así lograr una gran cantidad de biomasa. (11).
La adición de dispersantes, como la alta concentración de sacarosa para acomplejar medios como el YEME, garantiza la generación de cultivos que son relativamente dispersos. Además, la adición de aminoácidos y pequeños péptidos del hidrolizado de caseína, que contiene todos los aminoácidos esenciales en buena proporción excepto el triptófano por su degradación hidrolítica, o medios que contienen polietileno glicol, o Junlon, mejoran la tasa de crecimiento y, por consiguiente, ayuda a la dispersión del microorganismo (11).
Por tales motivos y con el objetivo de incrementar los niveles de expresión/secreción de la proteína recombinante rRv2626c de Mycobacterium tuberculosis H37Rv, expresada en S. lividans TK24 en este trabajo, se evaluaron dos medios de cultivo para la producción de dicha proteína en cultivos en zaranda. Con los dos medios de cultivo evaluados TSB formulado en el laboratorio (Tabla 2) y TSB-BioCen (Tabla 3), se obtuvo la cinética de crecimiento que describen los gráficos de la Figura 1.
Con ambos medios de cultivo se obtiene un crecimiento exponencial de la cepa con un máximo de crecimiento a las 36 h; sin embargo, los valores máximos de biomasa fueron de 1,6 mg/mL y 20,38 mg/mL para el medio TSB-Lab y para el TSB-BioCen, respectivamente. El medio de cultivo TSB-Biocen fue muy superior en cuanto a su capacidad de promover el crecimiento celular y la densidad de la biomasa generada con valores estadísticamente significativos (p<0,001) e intervalos de confianza del 95%, en los tiempos de muestreo de 30, 36, 42, 48, 54, 60 y 72 h de cultivo.
Como ambos medios ensayados fueron sometidos a las mismas condiciones de estudio, el medio líquido TSB-BioCen, fue muy superior con respecto a densidad o crecimiento celular lo que probablemente se debió a la presencia del ingrediente hidrolizado enzimático de caseína, ya que el TSB-Lab no contiene este componente sino triptona. Según Kieser y col. mejora la tasa de crecimiento y por consiguiente, contribuye al crecimiento disperso y beneficia al rendimiento del proceso (11).
Otro aspecto a destacar es el tipo de medio resultante después de preparación. Aunque ambos medios de ensayo son líquidos, el TSB-Lab, resultó ser una suspensión, mientras el TSB-BioCen es una solución homogénea, dándole a las células mejor provecho del uso de los nutrientes disueltos y de esta manera contribuye a la obtención de más biomasa. Por otra parte, con el objetivo de disponer de las concentraciones de proteínas y poder seguir su cinética según evolución del tiempo de cultivo de manera precisa se usó el método del BCA por sus conocidas ventajas. Con los datos de concentraciones del patrón de BSA y conociendo los valores de absorbancia determinados por la lectura de la densidad óptica (DO), se construyó una curva de regresión lineal, que permitió determinar con un alto coeficiente de determinación (R2=0,9961), las concentraciones de las muestras.
]]> En cuanto a la concentración de proteínas totales secretadas al medio de cultivo, los resultados indicaron que para ambos medios los valores máximos de proteínas secretadas se encontraron alrededor de las 30 h de cultivo, disminuyendo progresivamente a partir de las 36 h (Fig. 2). El medio TSB-Biocen sostiene la expresión-secreción de proteínas con muy poca disminución de la misma durante decenas de horas, como se aprecia en la meseta de la Figura 2B.Al igual que en el experimento anterior, los mejores resultados en este parámetro, se obtuvieron con alta significación estadística (p<0,001) e intervalos de confianza del 95%, en todos los tiempos ensayados, con el medio TSB-BioCen. Esta mejoría en la concentración de proteínas secretadas al medio, probablemente se debió a que con el medio TSB-BioCen se obtuvo un mayor crecimiento celular.
En la Figura 3 se muestra la imagen del gel con los resultados de la separación electroforética de las muestras tomadas en los diferentes tiempos de cultivo, mediante SDS-PAGE en condiciones reductoras. Nuestros resultados con los dos medios de cultivo estudiados, coinciden con lo informado por Ayala y col. en 2013 (6), que plantea que no se observó expresión de la rRv2626c antes de las 24 h. A partir de este momento comienzan a visualizarse en ambos medios de cultivo bandas alrededor de los 37 KDa y los 17 KDa correspondientes, probablemente, a las formas dimérica y monomérica de esta proteína, hasta las 54 h, tiempo a partir del cual comienza a disminuir la intensidad de ambas bandas (Fig. 3).
En condiciones no reductoras el análisis electroforético muestra una sola banda, que en las condiciones de este trabajo migra con un valor de 37 KDa y corresponde al dímero de la proteína expresada. Por su cercano valor al total de la proteína recombinante expresada es que se toma su proporción en el densitograma como dato para calcular el % de expresión-secreción específico. Como puede apreciarse los mayores porcientos de expresión de la proteína, según esta técnica, se alcanzan entre las 42 y las 54 h de cultivo para ambos medios, siendo superiores los valores para el medio TSB-BioCen, con el cual se alcanzó un máximo de expresión-secreción de la proteína recombinante de 8,5% con respecto al total a las 48 h del cultivo (Tabla 4).
En la Figura 4 se presentan los resultados de la identificación por Western Blot de la proteína rRv2626c. Se muestra la presencia de las dos bandas de la proteína, de aproximadamente 17 y 37 KDa, correspondientes al monómero y dímero de la misma, respectivamente. Las cuales son reconocidas de forma específica por el conjugado Strep-Tactin HRP a través de la cola de Strep-Tag, que se encuentra unida al C-terminal de la proteína. Se seleccionó para este análisis el medio y los tiempos de mayor crecimiento y expresión/secreción de la proteína de interés. Podemos concluir que con el uso del medio de cultivo TSB-BioCen químicamente definido y formulado industrialmente en BioCen, Cuba, se garantiza la completa disolución de cada componente, este factor contribuyó a obtener una densidad celular máxima a las 36 h de cultivo, con una mayor concentración de proteínas totales y proteína específica de las 42 a las 54 h, en comparación con el medio anteriormente utilizado. Además, se redujo de manera significativa el tiempo de fermentación del microorganismo de 96 h para el medio TSB-Lab a 54 h con el TSB-BioCen.
De igual forma se incrementaron los niveles de expresión/secreción de la proteína rRv2626c, mejorando el rendimiento del proceso para la obtención de esta proteína, que resulta de gran interés como parte de la formulación de una nueva vacuna experimental contra la tuberculosis y en el desarrollo de nuevos métodos de diagnóstico del estado latente de esta enfermedad.
AGRADECIMIENTOS
]]> Los autores deseamos agradecer a Simón Chang, Arlenis Moreno, Caridad Rodríguez, Elsa Pimienta, Julio Cesar Ayala y Carlos Vallin, por sus contribuciones a la creación y desarrollo del Grupo de Biotecnología del IFAL y sus aportes a los resultados en la obtención de proteínas recombinantes de M. Tuberculosis en vector Streptomyces lividans. También a los colegas de Bélgica Kris Huygen, Lieve Mellaert y Josef Anné por sus valiosos aportes. Del Instituto Finlay de Vacunas, deseamos reconocer los aportes en la realización de múltiples tareas tecnológicas y soluciones prácticas, a Dayli Serrano, Osmir Cabrera, Rocmira Pérez, Maria Padrón, Elsa Rey y José L. Perez Quiñoy.
REFERENCIAS
1. Weldingh K, Rosenkrands I, Meng Okkels L, Doherty TM, Andersen P. Assessing the Serodiagnostic Potential of 35 Mycobacterium tuberculosis Proteins and Identification of Four Novel Serological Antigens. J Clin Microbiol 2005;43:57-65.
2. Bao-Lin W, Ying X, Chao-Qun W, Yun-Min X, Hong-Hai W. Cloning, expression, and refolding of a secretory protein ESAT-6 of Mycobacterium tuberculosis. Prot Expres Purific 2005;39:184-8.
3. Zhang SL, Zhao JW, Sun ZQ, Yang EZ, Yan JH, Zhao Q, et al. Development and evaluation of a novel multiple-antigen ELISA for serodiagnosis of tuberculosis. Tuberculosis 2009;9:278-84.
4. Bentley SD, Chater KF, Cerdeno-Tarraga AM, Challis GL, Thomson NR, James KD, et al. Complete genome sequence of the model actinomycete Streptomyces coelicolor A3(2). Nature 2002;417:141-7.
5. Gilbert M, Morosoli R, Shareck F, Kluepfel D. Production and secretion of proteins by streptomycetes. Crit. Rev. Biotechnol. 1995;15:(1)13-39.
6. Ayala JC, Pimienta E, Rodríguez C, Anné J, Vallín J, Milanés MT, et al. Use of Strep-tag II for rapid detection and purification of Mycobacterium tuberculosis recombinant antigens secreted by Streptomyces lividans. J Microbiol Methods 2013;94:192-8.
7. Pimienta E, Ayala JC, Rodríguez C, Ramos A, Van Mellaert L, Vallin C, et al. Recombinant production of Streptococcus equisimilis streptokinase by Streptomyces lividans. Microb. Cell Fact. 2007;6(1):20.doi.org/10.1186/1475-2859-6-20.
8. Vrancken K, Anné J. Secretory production of recombinant proteins by Streptomyces. Future Microbiol. 2009;4(2):181-2.
9. García J, Santana Z, Zumalacárregui L, Quintana M, González D, Furrazola G, et al. Estrategias de obtención de proteínas recombinantes en Escherichia coli. VacciMonitor 2013;22(2):30-9.
]]>10. Pozidis C, Lammertyn E, Politou AS, Anne J, Tsiftsoglou AS, Sianidis G, et al. Protein secretion biotechnology using Streptomyces lividans: large-scale production of functional trimeric tumor necrosis factor alpha. Biotechnol Bioeng 2001;72:611-9.
11. Kieser T, Bibb MI, Buttner MJ, Chater KF, Hopwood DA. Practical Streptomyces Genetics. Norwich, UK: John Innes Foundation; 2000.
12. Laemmli UK. Cleavage of structural proteins during the assembly of the head of bacteriophage T4. Nature 1970;227:680-5.
Recibido: Julio de 2018 Aceptado: Septiembre de 2018
]]>