ARTÍCULO ORIGINAL
Actividad hepatoprotectora del extracto acuoso seco de Boerhavia erecta L. (tostón) en ratas
Hepatoprotective action of dry aqueous extract from Boerhavia erecta L. (toston) in rats
]]>
Juana I. Tillán CapóI; Viviana Bueno PavónII; Carmen Carrillo DomínguezIII; Sara Agüero FernándezIV; Odalys Valdés MartínezV
I Doctora en Ciencias Veterinarias. Licenciada en Bioquímica Farmacéutica. Investigadora Auxiliar. Centro de Investigación y Desarrollo de Medicamentos (CIDEM). Ciudad de La Habana, Cuba.
II Doctora en Medicina Veterinaria. CIDEM. Ciudad de La Habana, Cuba.
III Técnica en Farmacia. CIDEM. Ciudad de La Habana, Cuba.
IV Técnica en Procesos Biológicos. CIDEM. Ciudad de La Habana, Cuba.
V Licenciada en Tecnología de la Salud. CIDEM. Ciudad de La Habana, Cuba.
Palabras clave: ratas, Boerhavia erecta, hepatoprotector.
INTRODUCTION: several in vitro studies of the aqueous extract from Boerhavia erecta L. and the human hepatome cell line PLC/PRF/5 showed suppression in the formation of hepatitis B surface antigen (HbsAg) and the inhibitory action of the antigen present in human serum contaminated with hepatitis B surface antigen. ]]>
OBJECTIVES: to determine the in vivo hepatoprotective effect of the aqueous extract from B. erecta.
METHODS: male Wistar rats were treated with 250 and 500mg of dry extract per kg intragastrically for 5 days, with induced hepatic damage on the last day, using 1 ml/kg of a 1:1 mixture of carbon tetrachloride and olive oil; after 24 hours, blood samples were taken to determine enzymatic activity of alanine-aminotransferase and for the euthanasia of the rats in order to perform the histological study of their livers.
RESULTS: the extract caused significant reduction in the enzymatic activity of alanine-aminotransferase from treated rat sera and provided complete protection to the parenchyma of those animals which were administered 500 mg/kg dose.
CONCLUSIONS: the in vivo hepatoprotective effect of B. erecta aqueous extract was shown against carbon tetrachloride-induced damage.
Key words: rats, Boerhavia erecta, hepatoprotective.
]]>
INTRODUCCIÓN
Boerhavia erecta L. es una especie vegetal de la familia Nictaginaceae,1 utilizada con éxito por la población africana en el tratamiento de las enfermedades hepáticas, de la cual existen alrededor de 100 publicaciones científicas posteriores a 1979.2 El país con mayor reporte ha sido la India con 54 y la actividad farmacológica más estudiada ha sido la hepatoprotectora,3 donde se han propuesto algunos productos elaborados a partir de la planta. Otra especie de este género, prácticamente no estudiada, es la B. erecta L. que es endémica de Cuba, no domesticada y constituye maleza.
En Cuba, en 1999, se iniciaron los estudios del extracto acuoso de B. erecta y la fracción con alto contenido de lactona, en la línea celular de hepatoma humano PLC/PRF/5 y en suero humano contaminado con antígeno de superficie de hepatitis B (HbsAg), que dio como resultado una supresión en la formación de HbsAg en las células de hepatocitos y una actividad inhibitoria del antígeno en suero; teniendo en cuenta estos resultados se decidió realizar el estudio del efecto hepatoprotector in vivo del extracto acuoso de la B. erecta utilizando un modelo experimental in vivo de daño hepático en ratas, inducido con tetracloruro de carbono.
MÉTODOS
Sustancias de prueba ]]>
Material vegetal: las partes aéreas de la planta silvestre fueron recolectadas de las áreas cercanas a la Estación Experimental de Plantas Medicinales "Juan Tomás Roig" de San Antonio de los Baños y una muestra fue depositada en el herbario de la propia estación con el número ROIG 4642. El material vegetal fue secado a 40 ºC durante 2 d en estufa con recirculación de aire. El extracto acuoso fue elaborado a partir del material vegetal seco en la proporción de 10/100 (P/V), sometida a ebullición durante 30 min, posteriormente fue filtrada y concentrada en un rotoevaporador al vacío, después fue sometida a un proceso de secado por aspersión y calor. Se obtuvo un polvo fino de color carmelita claro que fue identificado con el número L 402.
Tetracloruro de carbono: Riedel-de-EAU, Alemania.
Aceite de oliva: Ybarra S.A., España.
Animales
Para el estudio se utilizaron ratas machos Wistar procedentes de la colonia de la UCTB de Control Biológico del Centro de Investigación y Desarrollo de Medicamentos (CIDEM) con peso corporal entre 150 a 200 g. Los animales permanecieron en salas de pruebas con temperatura de 22 ± 2 °C y humedad relativa entre 50 y 60 %. La alimentación consistió en pienso estandarizado peletizado para roedores EMO 1001® proveniente del Centro Nacional para la Producción de Animales de Laboratorio (CENPALAB) y agua potable a libre acceso.
]]>
Procedimiento experimental
Los animales fueron distribuidos aleatoriamente a razón de 6 por grupo e identificados de manera individual con tinta indeleble. Los tratamientos fueron: grupo I control sin tratamiento, grupos II y grupo III tratados con extracto acuoso seco de B. erecta, a las dosis de 250 y 500 mg/kg de peso corporal (pc), respectivamente.
El extracto acuoso (polvo seco) de B. erecta fue preparado en agua a las concentraciones de 2,5 y 5 %, que fueron administradas por vía intragástrica a las respectivas dosis de 250 y 500 mg/kg de pc (sobre la base de sólidos totales del extracto) con un factor volumen/peso de 10 mL/kg, durante 5 d.
La inducción del daño hepático fue provocada al quinto día de tratamiento a todos los animales, con una mezcla de tetracloruro de carbono y aceite de oliva en la proporción 1:1 administrada por vía intraperitoneal con un factor de volumen/peso de 1 mL/kg de pc. Transcurridas 24 h de la inducción del daño, se procedió al pesaje de los animales y a la extracción de sangre para la determinación de alanino amino transferasa, mediante un kit diagnóstico del Laboratorio Farmacéutico Carlos J. Finlay, cuyo método ha sido descrito por Reitman y Frankel.4 Por último, se procedió a la eutanasia de los animales y la extracción del hígado para ser pesado y procesado histológicamente, mediante la técnica de tinción con hematoxilina-eosina y la observación al microscopio.
El presente trabajo se realizó de acuerdo con las regulaciones internacionales establecidas para el cuidado y manejo de animales de laboratorio.5
Estadística ]]>
Los valores de actividad enzimática de alanino amino transferasa y el peso relativo del hígado de los diferentes grupos fueron procesados estadísticamente para la obtención de la media y la desviación estándar de cada grupo, así como un análisis de varianza de una vía (ANOVA), seguido de la prueba de Duncan para la comparación de las medias.6
RESULTADOS
Los valores de actividad enzimática de alanino amino transferasa se muestran en la figura 1, donde se observan diferencias significativas (p< 0,01) entre el grupo tratado solo con tetracloruro de carbono y los tratados con los extractos a las dosis de 250 y 500 mg/kg de pc durante 5 d, junto con tetracloruro de carbono al quinto día de tratamiento. No se encontraron diferencias significativas en los valores de actividad de alanino amino transferasa entre los 2 niveles de dosis (250 y 500 mg/kg de pc) ensayados de extracto acuoso seco de B. erecta.
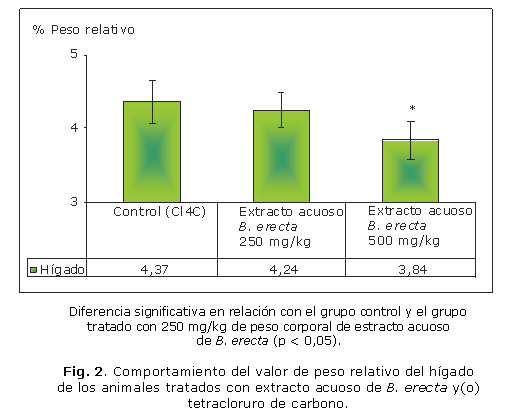
El peso relativo medio de los hígados de animales tratados con la dosis de 500 mg/kg de pc de extracto acuoso seco de B. erecta fue significativamente menor (p < 0,05), que el peso relativo medio de los hígados de animales tratados con la dosis de 250 mg/kg de pc de extracto y los animales pertenecientes al grupo control (Fig. 2).
]]>
En el estudio realizado a las muestras histológicas de hígado de los animales del grupo tratado solo con tetracloruro de carbono se pudo observar daño severo, con presencia de áreas intensas de necrosis, centros lobulares que forman puentes de confluencia y abarcan hasta la zona 3 del espacio de Rappaport. También hubo necrosis de coagulación en la periferia del tejido del hígado de todos los animales del grupo.El grupo II tratado con extracto acuoso de B. erecta a dosis de 250 mg/kg pc presentó una protección del parénquima, que bordeaba la vena centro lobular del tejido observado en la mayoría de los animales. Algunos puentes de confluencia fueron observados en el tejido del hígado de 2 animales, pero estos no abarcaron la zona 3 del espacio de Rappaport. Hubo presencia de áreas de necrosis centro lobular de aspecto vacuolar en casi todos los animales y solo 2 mostraron áreas extensas de coagulación en la periferia y necrosis.
El grupo III (dosis de 500 mg/kg de pc) presentó poco daño del parénquima; todos los animales mostraron protección del tejido alrededor de la vena centro lobular, no se observaron puentes de confluencia. Solo un animal mostró área de coagulación en la periferia del tejido observado y en pocos casos hubo focos de aspecto vacuolar.
DISCUSIÓN
El daño hepático inducido por tetracloruro de carbono en ratas albinas ha sido reportado por varios autores,7,8 el cual ocasiona lesiones hepáticas características posterior a los 30 min de su administración, que provocan alteraciones al nivel de los ribosomas y la función microsomal. Los lisosomas también se encuentran afectados tempranamente, lo cual ocasiona un daño hepático celular.
El tetracloruro de carbono ejerce su efecto tóxico al generar el radical libre CCl3, por acción de oxidasas ligadas al sistema P450 en el retículo endoplásmico. Por otro lado, la peroxidación de lípidos que afecta a la membrana plasmática se manifiesta en trastornos en el transporte de iones, como son ingreso masivo de agua, sodio y calcio con todas las consecuencias deletéreas para las células, que pueden llegar hasta su ruptura y muerte. Hay varios mecanismos que pueden inducir estos cambios, algunos ejemplos son el trauma físico, la fluidización de la membrana, la peroxidación de lípidos (tetracloruro de carbono), el daño al citoesqueleto, el bloqueo de canales y el ataque viral, entre otros.
Desde el punto de vista bioquímico, el daño hepático se refleja a través de un incremento de la actividad en suero de las enzimas alanino amino transferasa y fosfatasa alcalina, además del nivel de bilirrubina en un período de 24, 48, 96 y hasta 124 h. En el presente trabajo se observó la alteración de la actividad de la enzima alanino amino transferasa con un incremento significativo de esta, dado por la administración intraperitoneal de tetracloruro de carbono al grupo control, en relación con los valores obtenidos en los grupos de animales tratados con el extracto acuoso seco de B. erecta, lo que evidencia un efecto hepatoprotector del extracto evaluado. ]]>
Se conoce que la administración de tetracloruro de carbono a ratas provoca necrosis centro lobulares severas a las 24 y 48 h, con marcada degeneración grasa y variada infiltración celular.8 Las observaciones histológicas realizadas al tejido de los hígados de animales tratados con extracto seco de B. erecta y tetracloruro de carbono mostraron poco daño del parénquima. La dosis de 500 mg/kg mostró mejores resultados, al presentar protección del tejido hepático en todos los animales y la presencia de coagulación en el área de la periferia de solo un animal.En un trabajo realizado con extracto acuoso de B. diffusa e inducción de daño hepático con tetracloruro de carbono a ratas, se observó un efecto hepatoprotector con aumento del flujo biliar normal, que indica una fuerte actividad colerética.9
Por otra parte, los estudios fitoquímicos realizados con extractos de B. erecta revelan su contenido en isobetanina junto con neobetanina, catequinas, procianidinas y quercetinas, kaempferol y glicósidos como isorhamnetina,10 así como la acción antioxidante frente a sustancias químicas como alloxano11 y tetracloruro de carbono,7 al ejercer protección a las células de los daños causados por estos agentes.
Estudios clínicos realizados con plantas medicinales como Eclipta alba (Bhringaraj), Boerhavia diffusa (Punarnava) y Picrorhiza kurroa (Katuki) han mostrado resultados marcados en la protección y mejoría de los efectos provocados por la hepatitis viral A2.9,12
La presencia de compuestos fenólicos, flavonoides y los efectos antioxidantes reportados en la planta,10,11 capaces de evitar el daño a la membrana celular provocado por los radicales libres, sustancias químicas u otros agentes virales,7,8pudieran estar relacionados con los resultados hepatoprotectores del extracto acuoso de B. erecta encontrados en el presente trabajo, donde la dosis de 500 mg/kg de pc mostró la mejor protección del tejido hepático y valores menores de la enzima alanito amino transferasa.
REFERENCIAS BIBLIOGRÁFICAS
1. Roig JT. Plantas medicinales, aromáticas y venenosas de Cuba. 2 ed. La Habana: Editorial Científico-Técnica, 1988:883-4.
2. Castro Méndez Irma Esperanza, Rivero Martínez Reinaldo, Díaz González Ailema. Boerhavia spp. Rev Cubana Plant Med [serie en Internet]. 2001 Ago [citado Abr 2009];6(2):67-72. Disponible en: http://scielo.sld.cu/scielo.php?script=sci_arttext&pid=S1028 -47962001000200007&lng=es&nrm=iso
3. Boerhavia erecta. The Rainforest Plant Database [citado Abr 2009]. Disponible en: http://www.rain-tree.com/ervatostao.htm
4. Reitman S, Frankel S. A colorimetric method for the determination of serum glutamic-oxalic and glutamic-pyruvic transaminases. Amn J Clin Pathol.1957;28:56-63.
5. Universities Federation for Animal Welfare. Terrestrial vertebrates. Part 3, Species kept in the laboratory. The Ufaw Handbook on the care and management of laboratory animals. 7ª ed. V.1. London: Blackwell Science Ltd; 1999. p. 162-74.
6. Duncan DB. A significance test for differences between ranked treatments in an analysis of variance. Virginia J Sci. 1951;2:171-89.
7. Clarke SI, Lui EM. Interaction of methionin and tetrachloride on the protective effect of hepatotoxicity. C J Physiol Pharma. 1985;26(64):104-10.
8. Zimmerman HJ. The adverse effects of drugs and other chemicals on the liver. New York: Appleton Century Croft; 1978. p.164-7.
9. Chandan BK, Sharma AK, Anand KK. Boerhavia diffusa: a study of its hepatoprotective activity. J Ethnopharmacol. 1991;31(3):299-307.
10. Stintzing FC, Kammerer D, Schieber A, Adama H, Nacoulma OG, Carle R. Betacyanins and phenolic compounds from Amaranthus spinosus L. and Boerhavia erecta L. Z Naturforsch. 2004;59(1-2):1-8.
11. Satheesh MA, Pari L. Antioxidant effect of Boerhavia diffusa L. in tissues of alloxan induced diabetic rats. Indian J Exp Biol. 2004;42(10):989-92
12. Rawat AKS, Mehrotra S, Tripathi SC, Shome U. Hepatoprotective activity of Boerhavia diffusa L. roots. A popular Indian ethnomedicine. J Ethnopharmacol. 1997;56(1):61-6.
Recibido: 8 de abril de 2009.
Aprobado: 30 de julio de 2009.
Lic. Juana I. Tillán Capó. Centro de Investigación y Desarrollo de Medicamentos (CIDEM). Ave 26 No. 1605 entre Puentes Grandes y Ave. Boyeros. Ciudad de La Habana, Cuba. Correos electrónicos: juanatc@infomed.sld.cu; juana@cidem.sld.cu ]]>