
ARTÍCULO ORIGINAL
Actividad antiinflamatoria y antioxidante de Bauhinia kalbreyeri Harms en un modelo de inflamación intestinal agudo en ratas
Anti-inflammatory and antioxidant action of Bauhinia kalbreyeri Harms in an acute intestinal inflammation model used in rats
]]>
Paola Andrea Montealegre Moreno, Liliana Francis Turner
Universidad del Tolima. Colombia.
Objetivo: evaluar la actividad antiinflamatoria y antioxidante de extractos acuosos de hojas y corteza de Bauhinia kalbreyeri Harms mediante un modelo de inflamación intestinal en ratas.
Métodos: se utilizaron ratas Wistar, a las cuales se les indujo inflamación intestinal aguda mediante el uso de indometacina (15 mg/kg). Los extractos se administraron por gavage (40 mg/kg) durante 7 d. Se midieron los niveles enzimáticos de glutatión peroxidasa (GPX/L de sangre), se determinó el índice de actividad de la enfermedad y se realizó una caracterización macroscópica y microscópica de las lesiones.
Resultados: se determinó que la administración oral de los extractos tiene un efecto moderado sobre el modelo agudo de enteritis inducida por indometacina, con la disminución concomitante de los parámetros clínicos, patológicos e inflamatorios. Tanto el análisis histológico como el macroscópico de las muestras de animales tratados con extractos, confirmaron el efecto beneficioso ejercido por estos en el modelo de enteritis aguda inducida por indometacina, el cual se atribuye a los metabolitos secundarios presentes en la planta ya que se evidenció recuperación de la citoarquitectura, disminución en el grado de lesión y del índice de actividad de la enfermedad; así como la estabilización de los niveles de glutatión peroxidasa, que aumenta la viabilidad de las fibras de colágeno, evita el daño celular y promueve la síntesis de ADN, para iniciar la recuperación de la lesión.
Conclusión: este estudio se muestra como uno de los pioneros en dilucidar la actividad antiinflamatoria y antioxidante de Bauhinia kalbreyeri en un modelo in vivo.
]]>
Palabras clave: Bauhinia kalbreyeri, actividad antioxidante, actividad antiinflamatoria, glutatión peroxidasa, enfermedad inflamatoria intestinal, ratas.Objective: to evaluate the anti-inflammatory and antioxidant activity of aqueous extracts of leaves and bark from Bauhinia kalbreyeri Harms in an intestinal inflammation model applied to Wistar rats.
Methods: the Wistar rats were induced acute intestinal inflammation by using indomethacin (15 mg/kg). The extracts were administered by gavage (40 mg/kg) for 7 days. The enzyme levels of glutathione peroxidase (GPX/L of blood) were measured, the rate of disease activity was estimated, and finally the lesions were macroscopically and microscopically characterized.
Results: it was found that oral administration of the extracts has a modest effect on acute enteritis model induced by indomethacin, with concomitant decrease in the clinical parameters and inflammatory disease. Both the macroscopic and histological analysis of samples from the animals treated with extracts confirmed their beneficial effect on the indomethacin-induced acute enteritis model. This effect is attributed to the secondary metabolites in the plant since the experiment evidenced recovery of cytoarchitecture, lower degree of injury, reduced rate of disease activity, as well as stabilization of glutathione peroxidase levels that cause more viability of the collagen fibers, prevent cell damage and encourage DNA synthesis to start recovery from injury.
Conclusions: this study seems to be one of the pioneers in elucidating the anti-inflammatory and antioxidant properties of Bauhinia kalbreyeri in an in vivo model.
Key words: Bauhinia kalbreyeri, antioxidant activity, anti-inflammatory activity, glutathione peroxidase, inflammatory intestinal disease, rats.
]]>
INTRODUCCIÓN
La alta diversidad de especies vegetales con importantes propiedades terapéuticas ha promovido en los últimos años un incremento en las investigaciones científicas, que buscan comprobar los conocimientos de la medicina popular. Esto deriva en la búsqueda y obtención de drogas alternativas que presenten efectos colaterales en menor medida respecto a las convencionales y, de ser posible, se conviertan en herramientas útiles para mejorar las condiciones socioeconómicas de las comunidades que usan y comercializan sus propias plantas. Lo anterior se puede sustentar en el hecho de que las plantas medicinales y sus derivados hacen parte de cerca del 25 % de los fármacos actuales, otro 50 % son de origen sintético pero relacionado con los principios aislados de plantas medicinales.1
Se requiere la validación por medio de la investigación científica mediante la experimentación con modelos apropiados para probar los efectos farmacológicos; así como el aislamiento, la purificación y caracterización de principios activos, que garanticen la formulación de los medicamentos herbarios para uso humano o animal, porque resulta esencial el estudio de la dosis, la concentración y vía de administración. Entre la gran variedad de especies vegetales de interés terapeútico se encuentran las plantas del género Bauhinia (Fabaceae), de las que su uso medicinal ha sido respaldado por estudios científicos realizados en varios modelos experimentales, mediante los cuales se han comprobado algunos efectos biológicos y farmacológicos ya descritos en la literatura.1 Diferentes reportes han dado a conocer las distintas propiedades que exponen los individuos de este género, como sus acciones hipoglicemiantes y antimicrobianas, antiulcerosas, antihiperlipidémicas, antioxidantes y antiinflamatorias.2-8
Así mismo, en investigaciones previas se ha podido determinar la composición química de algunas de las especies del género Bauhinia; se han encontrado entre otros compuestos, lactonas, flavonoides, terpenoides, esteroides, triterpenos, taninos y quinonas lo cual ha permitido tener más claridad acerca de las bondades que brindan estas plantas para el mejoramiento de la calidad de vida de una parte importante de la población. Esos metabolitos poseen diversos efectos farmacológicos como antioxidantes, antiinflamatorios, antineoplásicos, cardiotónicos, entre otros, y a mediano plazo brindarán una herramienta alternativa al sistema de salud público, mediante la investigación de su uso potencial en diversos padecimientos.1,9-12
Dentro de las diferentes propiedades evidenciadas en las plantas del género Bauhinia, especialmente en la especie Bauhinia kalbreyeri Harms, las que más interesaron para el desarrollo de esta investigación fueron la antiinflamatoria y antioxidante, porque aunque las enfermedades inflamatorias crónicas han sido objeto de un intenso estudio por parte de la comunidad científica en los últimos años, su terapia sigue siendo insatisfactoria. Esto se debe a su asociación con una elevada incidencia de reacciones adversas, que en estos procesos, especialmente en la llamada enfermedad inflamatoria intestinal (EII), se manifiesta el estrés oxidativo causado por los radicales libres y oxidantes derivados del oxígeno y del nitrógeno, los cuales tienen un papel importante en la patogenia de las lesiones tisulares como las úlceras y la inflamación; también que estos padecimientos afectan a gran parte de la población en Colombia, con una prevalencia extrapolada de más 77 000 casos de EII, que se muestran como enfermedad de Crohn (EC) y colitis ulcerativa (CU).13
Sobre la base de lo expuesto antes y como continuidad a trabajos previos realizados en la región y en la Universidad del Tolima, el objetivo fudamental de esta investigación consistió en evaluar en un modelo experimental de inflamación aguda en ratas Wistar, si los extractos de hoja y corteza de Bauhinia kalbreyeri Harms son capaces de reducir y controlar los procesos inflamatorios intestinales, con la reducción concomitante de los síntomas característicos, y si parte de esta acción antinflamatoria está estimulada por la acción antioxidante de esos extractos.
]]>
MÉTODOS
Las hojas y corteza de B. kalbreyeri se colectaron en zona suburbana de Ibagué (1 350 m sobre el nivel del mar, 27 °C), en excelente estado fitosanitario y vegetativo (Fig. 1). En el intento de dar validez científica a la metodología aplicada por las etnias tolimenses, se prepararon extractos acuosos por el método de decocción. El material se secó en horno a 35 ºC hasta peso constante, se redujo el tamaño de partícula en un molino Thomas Wiley con malla de 2,0 mm y se obtuvo un polvo para la preparación del extracto acuoso por decocción (1:10 vegetal/solvente, 30 min); después de filtrar al vacío, el extracto se concentró (65 ºC) en un rotavapor BUCHI R114 hasta obtener un material viscoso, el cual se dejó enfriar y se congeló hasta su uso. Se determinó el peso seco de la planta (hoja y corteza) para el cálculo de las dosis a administrar.
Se tuvo como principal premisa el cumplimiento de las buenas prácticas de laboratorio (BPL) para el mantenimiento y la experimentación con animales de laboratorio, las 3Rs (refinamiento, reducción y reemplazo) y la guía Utilization and Care of Vertebrate Animals Used in Testing, Research and Training de 1985.14
Se utilizaron 44 ratas Wistar machos entre 200 y 250 g de peso corporal proporcionadas por el bioterio de Experimentación la Facultad de Ciencias de la Universidad del Tolima, grupo Modelos Experimentales para las Ciencias Zoohumanas (ME-CZH). Los animales se mantuvieron en cajas de polipropileno y en una densidad de 5 animales por cajas, a una temperatura de 22 ± 2 °C y humedad relativa de 60 %, atendiendo a los parámetros zootécnicos para la especie. La alimentación se controló a razón de 15 g de concentrado por animal al día y el agua se le suministró ad libitum. ]]>
Los animales se distribuyeron aleatoriamente en 6 grupos, con 6 individuos: Grupo V (control negativo), recibió una dosis del vehículo (NaHCO3 5 %) s.c. (subcutánea), el día 0 y se suplementó con agua destilada (4 ml/kg) por sonda orogástrica a las 8 a.m. a partir del día 1 durante 7 d; Grupo I (control positivo), recibió indometacina (15 mg/kg) vía s.c. el día 0 y se suplementó con agua destilada (4 mL/kg) por sonda orogástrica a las 8 a.m. a partir del día 1 durante 7 d; Grupo I/EH (experimetal), recibió indometacina vía s.c. el día 0 y se suplementó con el extracto de las hojas de Bauhinia kalbreyeri Harms (40 mg de hojas pulverizadas/kg de peso) a las 8 a.m. a partir del día 1 durante 7 d; Grupo I/EC (experimetal), recibió indometacina vía s.c. el día 0 y se suplementó con el extracto de la corteza de Bauhinia kalbreyeri Harms (40 mg de corteza pulverizada/kg de peso) a las 8 a.m. a partir del día 1 durante 7 d; Grupo V/EH (control tratamiento), recibió una dosis del vehículo (NaHCO3, 5 %) vías s.c. el día 0 y se suplementó con el extracto de las hojas de B. kalbreyeri a las 8 a.m. a partir del día 1 durante 7 d; Grupo V/EC (control tratamiento), recibió una dosis del vehículo (NaHCO3, 5 %) vía s.c. el día 0 y se suplementó con el extracto de la corteza de B. kalbreyeri a las 8 a.m. a partir del día 1 durante 7 d.Para evaluar la actividad antiinflamatoria de los extractos de hoja y corteza de Bauhinia kalbreyeri Harms se utilizó el modelo propuesto por Ramos y otros.15 La inflamación intestinal aguda se indujo mediante una inyección de indometacina disuelta en NaHCO3, 5 %, vía s.c. (15 mg/kg peso) el día 0 de experimentación a las 8:00 a.m.
Un día después de la administración de la indometacina se procedió a la aplicación de los tratamientos mediante sonda orogástrica (gavage), los extractos acuosos se administraron en dosis equivalentes a 40 mg de hojas o corteza por kilogramo de peso, una vez al día por 7 d (entre 0,3 y 1 ml de extracto, en dependencia del peso).
Durante el proceso de experimentación se realizó el control del peso y la talla de los individuos a las 8:00 a.m. todos los días (desde el día 1 y hasta el día 7) y de los cambios morfo-fisiológicos que presentaron a diario (cambio en el pelaje, color y contextura de las heces fecales, incluidos cuadros diarreicos y la presencia o no de sangre); estos parámetros permitieron asignar diariamente a cada animal un índice de actividad de la enfermedad (IAE), el valor del IAE para cada animal es el promedio del valor de la pérdida de peso, la consistencia de las heces y la presencia o no de sangre en estas.
Se midieron los niveles enzimáticos de glutatión peroxidasa en sangre de ratas utilizando un kit comercial de Laboratorios Randox Ltd. RANSEL, basado en una técnica cinética compuesta NADPH-dependiente. Los análisis se realizaron en un espectofotómetro automático (Barnstead Turner spectophotometer Sp-830 plus). Todas las lecturas se efectuaron por triplicado. Los resultados se expresaron en U/L de sangre entera.
El día octavo los individuos recibieron una dosis de 1 mL/5 kg de peso (intraperitoneal) de Eutanex® y se procedió a la necropsia. A lo largo de todo el abdomen del animal se realizó una incisión en la línea alba del plano muscular para evidenciar las vísceras abdominales. Se extrajo el yeyuno medio y se abrió por el lado opuesto al mesenterio, se lavó con suero fisiológico y se fijó en formol tamponado 10 % para el estudio histopatológico. Se realizaron cortes de 3 a 5 µm de grosor del yeyuno-íleon y se hizo tinción hematoxilina-eosina. A nivel macroscópico se utilizó una escala que considera el daño macroscópico de 0 a 13 puntos, asimismo se consideró la escala propuesta por los mismos autores para cuantificar el daño histológico en una escala del 0 al 10.
RESULTADOS
]]>
La inyección subcutánea de indometacina (15 mg/kg) en las ratas, como modelo de inflamación intestinal aguda, indujo un proceso inflamatorio intestinal. Todos los animales presentaron ablandamiento de las heces al día siguiente de la administración de la indometacina (día 1). Los tratados solo con indometacina (grupo I) desarrollaron signos evidentes de diarrea el primer día del estudio, al igual que los tratados con extracto de hoja de B. kalbreyeri (grupos I/EH) y el 80 % de los tratados con corteza (I/EC). Al segundo día disminuyó el porcentaje de diarrea en todos los grupos, pero se mantuvo durante los 7 d en el grupo tratado solo con indometacina (I), que además se caracterizó el 66 % de esta población por ser una diarrea sanguinolenta; esta característica se redujo en la medida en que pasaron los días. asimismo se evidenció la disminución de cuadros diarreicos en los grupos tratados con los extractos, que mostraron una recuperación más rápida para el grupo tratado con I/EC, porque al día 3 de tratamiento dejó de presentar diarreas, a diferencia del grupo I/EH que se estabilizó hasta el día 5 (Fig. 2). En cuanto al peso corporal, aunque no hubo una disminución significativa, se evidenció que los animales perdieron entre 1 y 10 % de peso (grupo I) o se mantuvieron sin variación (grupo I/EH). De acuerdo con estas características del proceso inflamatorio se asignó un valor de IAE, el cual resultó mayor en los animales con enteritis experimental. Los grupos controles (V, V/EH y V/EC) no presentaron diarrea, esto indica que la aplicación de los extractos por sí solos no tiene efectos adversos en la motilidad intestinal.
Adicionalmente se observaron cambios en el pelaje de los individuos tratados con indometacina (Grupos I, I/EH, I/EC), el 90 % presentó depilaciones del día 1 a 3, con posterior recuperación en 70 % de las lesiones al día 7. Algunos individuos de los grupos I, I/EH, I/EC, presentaron vocalizaciones y chillidos agudos, también permanecieron con la cabeza en el abdomen para dormir (contracción abdominal), el pelaje descuidado, aumento de la piloerección, así como un poco la agresividad y resistencia en el momento de la manipulación; además, se evidenció reducción de la conducta exploratoria, todo esto catalogado previamente como síntomas de malestar y enfermedad por parte de los individuos experimentales.16
En toda la experiencia, los grupos control (V, V/EH y V/EC) se comportaron como individuos sanos, lo cual indica que la vía de administración de los tratamientos y los extractos por sí solos no tiene efecto adverso en el organismo de los animales tratados. Al evaluar el IAE, se observó en el grupo I, el cual representa el modelo, que los animales presentaron diarreas, sangre en las heces y pérdida de peso; por consiguiente, generaron un IAE mucho más alto y constante que el de los grupos I/EH e I/EC, que mostraron menores valores a través de los días y no tuvieron diferencias significativas entre ellos. Esto indica que los dos extractos controlan de manera eficaz los signos de enfermedad y parece más rápida la acción del extracto de corteza, que al tercer día tuvo un IAE casi de 0, comparado con el del extracto de hoja que hasta el día 5 alcanzó esa cifra, lo cual se relaciona con la disminución de la frecuencia y duración de las diarreas y la pérdida de peso (Fig. 3).
]]>
A nivel macroscópico e histológico se observó una intensa respuesta inflamatoria en el intestino delgado, que se caracterizó por la presencia de edema en mucosa y serosa, úlceras y adherencias a nivel macroscópico (Fig. 4). Histológicamente se observó infiltrado inflamatorio, acortamiento de las vellosidades, necrosis de la mucosa, presencia de edema y hemorragia con infiltración de neutrófilos, eosinófilos y células plasmáticas, abscesos en las criptas que son consistentes en un cúmulo de neutrófilos y presencia de granulomas. La presencia de exudado linfocitario y neutrofílico en grado moderado para algunos individuos de los grupos I/EH e I/EC indica una resolución de las lesiones, quizá debido a la posible disminución de bacterias por el efecto antimicrobiano de los compuestos presentes en B. kalbreyeri (Fig. 5).
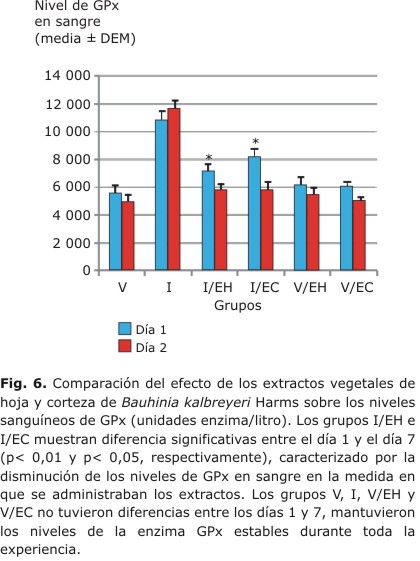
En el presente estudio, los animales del grupo tratado con indometacina (grupo I) mostraron incremento en los niveles de GPx en las dos mediciones realizadas, los cuales se mantuvieron constantes durante la experiencia. En cuanto a los grupos controles (V, V/EH y V/EC) se mantuvieron niveles bajos y constantes durante toda la experiencia, esto indica que no hubo alteración en la E-GPx y por ende en la lectura de GPx sanguínea (U/L). Los grupos tratados (I/EH e I/EC) no presentaron diferencias significativas entre ellos durante los días 1 y 7, aunque respecto a los controles el grupo I/EC se comportó igual a estos desde el primer día (Fig. 6). Se registró un aumento de la enzima en el grupo I del 8 % y una disminución en los grupos I/EH e I/EC de 18,8 y 30 %, respectivamente.
]]>
DISCUSIÓN
Para este proyecto en particular se evaluó la actividad antiinflamatoria y antioxidante de Bauhinia kalbreyeri Harms para dar sustento, en parte, al uso de esta especie en la medicina popular para diversos padecimientos, en especial en el tratamiento de la enfermedad inflamatoria intestinal EII y como continuidad a trabajos previos realizados en la región en torno a esta planta, por ello se utilizaron extractos acuosos obtenidos por método de decocción emulando la forma de preparación tradicional.
Se empleó un modelo de inducción de enteritis aguda por un medicamento antiinflamatorio no esteroide (AINE), indometacina, propuesto por Ramos y otros,15 el cual se considera un buen modelo de enfermedad de Crohn que es parte de las enfermedades inflamatorias intestinales (EII), porque presenta cierta similitud con algunas de las características histopatológicas de esa enfermedad; este medicamento inhibe las ciclooxigenasas y promueve la disminución de la producción de prostanglandinas, que son las responsables del mantenimiento de la integridad de la mucosa intestinal.17-20 En los animales de los grupos I, I/EH e I/EC, en que reprodujo artificialmente la enteritis, los estudios anatomopatológicos de las muestras obtenidas permitieron comprobar el establecimiento de esta y el mantenimiento de la lesión durante las sesiones de tratamiento.
Se tuvieron en cuenta diferentes aspectos para determinar la acción antiinflamatoria de los extractos de hoja y corteza de Bauhinia kalbreyeri Harms: los aspectos fisiológicos y las valoraciones macroscópicas e histológicas. En primera instancia se llevaron reportes de cambios fisiológicos (como peso, consistencia de las heces y cuadros diarreicos) para determinar el índice de actividad de la enfermedad, que evalúa la severidad clínica de la enteritis experimental. se observó que en el grupo I (modelo), al igual que en el modelo de colitis por D55, los animales presentaron diarreas, sangre en las heces y pérdida de peso; que fue máxima 7 a 8 d después de la administración del agente inductor, presenta un IAE más alto y constante que el de los grupos I/EH e I/EC, que fueron asignados con menores valores a través de los días y no tuvieron diferencias significativas entre ellos. Eso indica que los dos extractos controlan de manera eficaz los signos de enfermedad, que parece más rápida la acción del extracto de corteza, lo cual se relaciona con la disminución de la frecuencia y duración de las diarreas y la pérdida de peso.21
Cuando se presenta un proceso inflamatorio a nivel intestinal existe un patrón motor defensivo que aparece tras la activación del sistema inmune y cuyo objetivo es la rápida expulsión del tracto digestivo de agentes potencialmente nocivos. este patrón consiste en el incremento de la actividad motora propulsiva del intestino delgado y se da posterior a la colonización por parte de enterobacterias y anaerobias estrictas, lo que genera cuadros diarreicos. En el presente estudio se evidenció la disminución de los episodios diarreicos en los grupos tratados con los extractos después de la enteritis experimental, lo cual puede deberse en parte al efecto antibiótico y bactericida de Bauhinia kalbreyeri que se atribuye a los fitoconstituyentes encontrados en trabajos previos, como algunos compuestos fenólicos de tipo flavonoides y taninos.22,7
Se sabe que los flavonoides exhiben actividad antimicrobiana debido a la formación de un complejo con la pared celular bacteriana y que los taninos producen inhibición enzimática por los compuestos oxidados, quizá a través de la reacción con grupos sulfidrilos o de interacciones inespecíficas con proteínas; todo ello debido a que las bacterias y productos luminales claramente contribuyen a la respuesta inflamatoria, porque estudios previos determinaron que ratas libres de microorganismos y tratadas con antibióticos desarrollan mínimas lesiones después de la administración de indometacina. Esto se debe, como se ha dicho antes, a que la indometacina al alterar la permeabilidad de la mucosa facilita la entrada de bacterias y otros compuestos dañinos dentro de la lámina propia y produce inflamación. En la fase aguda de la EII las enterobacterias luminales aumentan en el duodeno, yeyuno, ileon y colon (E. coli, aerobias facultativas grampositivas como enterococos, faecalis, estafilococos y lactobacilos), y este aumento demuestra que las bacterias luminales están implicadas en la patogénesis de la enteritis aguda; además existen diversos estudios que documentan el potencial antimicrobiano de algunas especies de Bauhinia y específicamente su acción contra enterobacterias. Por ello, se recomienda realizar estudios posteriores que determinen los mecanismos de acción de los fitoconstituyentes de Bauhinia kalbreyeri sobre colonias bacterianas específicas, que ayude a soportar el supuesto que aquí se plantea.4,17,22,23 ]]>
Dentro de los factores fisiológicos encontrados se notó además que en los individuos tratados con indometacina se vieron grandes depilaciones, sobre todo en el lomo y cerca a la cabeza; estos eventos se pueden explicar por la alteración del estado general debido a la actividad de la enfermedad y a las complicaciones de tipo autoinmune que se evidencian en la enfermedad inflamatoria intestinal (EII), tanto en la colitis ulcerosa como en la enfermedad de Crohn, y que afectan las articulaciones, los ojos o la piel, y que se ven emuladas en el desarrollo de este modelo animal.16,24La enteritis experimental se ubicó en el yeyuno e íleon, así como en el colon. Es importante resaltar que la ventana de observación del efecto de los extractos fue de 7 d, por lo que sería muy interesante ampliar el tiempo de evaluación de los efectos de los extractos de 15 d a 1 mes postratamiento, teniendo en cuenta que los procesos de regeneración transcurren por diferentes fases (inflamatoria, proliferativa, epitelialización; y maduración y remodelado, respectivamente) y todo el proceso puede durar de 3 a 4 semanas.15,25-27
Se determinó que los grupos controles V, V/EH y V/EC no tenían diferencias entre ellos y sus características eran típicas de organismos sanos, lo cual indica que los extractos no generaron ningún efecto adverso en su administración. El grupo I presentó todas las características macroscópicas y microscópicas de la inflamación intestinal que el establecimiento del modelo, mientras que los grupos I/EH e I/EC mostraron una mejoría según trascurrieron los días en sus características macroscópicas y microscópicas, con una reducción en la intensidad de las lesiones sin evidencia de necrosis y supresión de la reacción inflamatoria, que confirmó el efecto beneficioso ejercido por estos en el modelo de enteritis aguda inducida por indometacina. Se evidenció recuperación de la citoarquitectura en la mayoría de los animales de estos grupos (por ejemplo, criptas con estructuras casi normales, regeneración de vellosidades, producción de fibrina, disminución de úlceras y de la necrosis, etc.), atenuando la infiltración de granulocitos, así como disminución en el grado de lesión y del IAE. Los procesos de recuperación de una lesión incluyen la inflamación, granulación, fibrosis, producción de colágeno y epitelización, los cuales se identificaron de forma leve en los animales tratados con los extractos; esto se puede atribuir a que al tener propiedades antioxidantes (debido a la presencia de compuestos fenólicos) inhiben la peroxidación lipídica, lo que aumenta la viabilidad de las fibras de colágeno por un aumento en la circulación, que evita el daño celular y promueve la síntesis de ADN. Se ha demostrado que las sustancias antioxidantes pueden promover la recuperación de una lesión y su epitelización, como se ha reportado en otras plantas del género Bauhinia, en las cuales altas cantidades de taninos pueden ser las responsables de la acción curativa en modelos animales de lesiones.28,29
Según reportes de Ramos,15 la dosis única subletal de indometacina a 15 mg/kg de peso vivo induce una inflamación aguda que tiene su mayor expresión al segundo día y se mantiene hasta el día 3. en la presente experiencia se pudo evidenciar que este modelo puede abarcar hasta los 7 d posaplicación manteniendo las mismas condiciones del cuadro inflamatorio inicial, así mismo, se reportan para el modelo lesiones limitadas al intestino delgado medio, lo que aunque se reprodujo en el presente estudio, también afectó el estómago, ciego y colon, tal como sucede en la enfermedad de Crohn.
En cuanto a la actividad antioxidante de los extractos acuosos de hoja y corteza de Bauhinia kalbreyeri se determinó mediante un kit comercial (Ransel) basado en el método de Paglia y Valentine,30 que es una técnica cinética compuesta NADPH-dependiente, la cual se fundamenta en la diferencia en el consumo de NADPH entre el blanco y la muestra para determinar la actividad enzimática de GSH-Px; esta es directamente proporcional a la disminución en la absorbancia.
Los resultados indicaron una variación inicial de los datos, que se puede deber a efectos de la manipulación. se determinó que el grupo I (modelo) presentó niveles altos de la enzima GPx en las dos mediciones realizadas y que se mantuvo estable durante la experiencia, similar al comportamiento de los grupos controles (V, V/EH y V/EC) con niveles de GPx relativamente bajos y constantes. Los grupos tratados (I/EH e I/EC) no presentaron diferencias significativas entre ellos durante los días 1 y 7, aunque respecto a los controles, el grupo I/EC se comportó igual a estos desde el primer día. Se registró un aumento de la enzima en el grupo I de 8 % y una disminución en los grupos I/EH e I/EC de 18,8 y 30 %, respectivamente. todo lo anterior indicaría que la acción antioxidante de la corteza es más eficaz que la de la hoja, lo cual parece ser consistente con los hallazgos in vitro en cuanto a la capacidad secuestradora de radicales libres (CSRL) y del contenido fenólico total por parte del extracto de corteza, que es superior al de hoja; pero aún permite pensar en B. kalbreyeri como una planta con potencial en la prevención de los daños producidos por las especies reactivas de oxígeno (ERO).3
Al haberse inducido una reacción aguda, la curva de comportamiento de la concentración de la glutatión peroxidasa aumenta (día 1), lo cual se puede dar por motivos de manipulación, que provoca estrés oxidativo y el posterior incremento en los niveles de GPx, sumado a la inducción de la enteritis experimental (día 0), en la cual la respuesta inmunitaria innata se activa, provocando una respuesta exagerada e incontrolada que conduce a un daño del tejido con inflamación. Esto da lugar a su vez al desencadenamiento del estrés oxidativo; seguido a ello, tras la administración de sustancias antioxidantes exógenas como son los extractos y a sus efectos significativos en el organismo, los niveles sanguíneos de la enzima disminuyen. esto se podría interpretar como el aumento de la protección de sustancias antioxidantes de fuente exógena, que haría innecesaria la expresión de los sistemas endógenos, porque esos antioxidantes son empleados por las células del organismo para eliminar los radicales libres.31,32
Estudios previos determinaron la composición de los extractos acuosos de hoja y corteza de Bauhinia kalbreyeri Harms, al encontrar flavonoides, taninos, fenilpropanoides, quinonas, terpenos o esteroides, e iridoides, además (en menor proporción) saponinas y cumarinas; todos ellos con algún grado de actividad antioxidante. Asimismo se ha determinado in vitro que el potencial antioxidante del vegetal es igual o superior a 90 % en concentraciones relativamente pequeñas y que esa actividad se deriva de las propiedades conjuntas de sus metabolitos secundarios (principalmente de los flavonoides y taninos) que le dan poder reductor del ion Fe+3, habilidad para quelar Fe+2 y descomponer el peróxido de hidrógeno, así como también aptitud para capturar especies reactivas de nitrógeno, entre ellas el óxido nítrico (NO). los compuestos fenólicos pueden contribuir directamente a la acción antioxidante y son también efectivos donadores de hidrógenos, lo cual los hace buenos antioxidantes.3,9,23
Aunque se ha determinado que la acción sinérgica de los constituyentes de los extractos es la clave para sus actividades antioxidantes y antiinflamatorias, cabe resaltar que a los flavonoides y los compuestos fenólicos presentes en el género Bauhinia se les han atribuido una variedad de efectos biológicos en numerosos sistemas celulares, tanto in vitro como in vivo y se ha demostrado que tienen actividades antimicrobianas, antivirales, antiulcerosas, citotóxicas, antineoplásicas, antiinflamatorias, antioxidantes, antihepatotóxicas, antihipertensivas, hipolipémicas y antiplaquetarias; eso daría un punto de partida para probar los compuestos aislados de Bauhinia kalbreyeri en modelos animales diferentes, como aquellos modificados genéticamente, que brinden información más precisa y se controlen las variables de manera más rigurosa.20
Todos estos resultados permiten entonces determinar que la administración oral de extractos acuosos de hoja y corteza de Bauhinia kalbreyeri tiene un efecto moderado sobre el modelo agudo de enteritis inducida por indometacina, con una ventana de observación de una semana posterior a la inducción de la lesión y el tratamiento, con la disminución concomitante de los parámetros clínicos, patológicos e inflamatorios; así como en la regulación de la enzima glutatión peroxidasa, responsable de la eliminación de especies reactivas del oxígeno presentes en los procesos inflamatorios y que permite el análisis de la fisiopatogenia de diversas enfermedades. ]]>
Este es el primer estudio reportado hasta el momento que apuntó a determinar la actividad antiinflamatoria y antioxidante in vivo de Bauhinia kalbreyeri, el cual brinda bases para otros y soporte adicional a las investigaciones locales previas sobre esta planta, que validan su uso etnobotánico y genera mayor interés en el estudio de los recursos vegetales en pro del beneficio local y mundial en el tratamiento de la enfermedad inflamatoria intestinal.
AGRADECIMIENTOS
A la Oficina de Investigaciones y Desarrollo de la Universidad del Tolima, que financió esta investigación.
REFERENCIAS BIBLIOGRÁFICAS
]]>
1. Da Silva K, Filho V. Plantas do gênero Bauhinia: Composição química e potencial farmacológico. Química Nova. 2002;25(3):449-54.
2. Fuentes O, Arancibia-Avila P, Alarcón J. Hypoglycemic activity of Bauhinia candicans in diabetic induced rabbits. Fitoterapia. 2004;75(6):527-32.
3. Murillo E, Tique M, Ospina L, Lombo O. Evaluación preliminar de la actividad hipoglicemiante en ratones diabéticos por aloxano y capacidad antioxidante in vitro de extractos de Bauhinia kalbreyeri Harms. Rev Col Cienc Quím Farm. 2006;35(1):64-80.
4. Dugasani S, Balijepalli M, Tandra S, Pichika M. Antimicrobial activity of Bauhinia tomentosa and Bauhinia vahlii roots. Pharmacognosy Magazine. 2010;6:204-7.
5. Borikar V, Jangde C, Rekhe D. Study of antiulcer activity of Bauhinia racemosa Lam in rats. Veterinary World. 2009;2(6):215-6. ]]>
6. Rajani G, Ashok P. In vitro antioxidant and antihyperlipidemic activities of Bauhinia variegata Linn. Indian J Pharmacol. 2009;41(5):227-32.
7. Ortiz H, Sánchez W, Mendez J, Murillo E. Potencial antioxidante de hojas y corteza de Bauhinia kalbreyeri Harms: Contribución de sus flavonoides en esta actividad. Rev. Acad Colomb Cienc. 2009;33(127):183-91.
8. Shreedhara C, Vaidya V, Vagdevi H, Latha K, Muralikrishna K, Krupanidhi A. Screening of Bauhinia purpurea Linn. for analgesic and anti-inflammatory activities. Indian J Pharmacol. 2009;41(2):75-9.
9. Ortiz H, Sánchez W. Actividad antioxidante de los flavonoides de las hojas y corteza de Bauhinia kalbreyeri Harms. [Tesis de pregrado]. Ibagué-Tolima, Colombia: Programa de Licenciatura en Educación Básica con énfasis en ciencias naturales y educación ambiental. Facultad de Ciencias de la Educación, Universidad del Tolima; 2007.
10. Escamilla C, Cuevas E, Guevara J. Flavonoides y sus acciones antioxidantes. Rev Fac Med UNAM. 2009;52(2):73-5. ]]>
11. Ballester I, Camuesco D, Gálvez J, Sánchez de Medina FA. Flavonoids and inflammatory bowel disease. Rev Ars Pharmaceutica. 2006;47(1):5-21.
12. Angulo P, Díaz D, Espinoza J, Fernández V, Figueroa M, Galarza A. Implicaciones farmacológicas y toxicológicas del óxido nítrico en la inflamación intestinal: II. Enteritis inducida por AINEs como Modelo Experimental para el Estudio Científico de la Flora Medicinal Peruana. Rev Ciencias Vet. 2001;17(3):21-6.
13. Calderón J, Góngora Z. Clinical and pathological similarities between paratuberculosis and Crohn's disease. ¿A possible zoonotic link? Revisión de literatura. Rev MVZ Córdoba. 2008;13(1):1226-39.
14. Utilization and care of vertebrate animals used in testing, research and training. Institute of Laboratory Animal Resources Commission on Life Sciences National Research Council. 1995. Available at: http://www.nal.usda.gov/awic/pubs/noawicpubs/careuse.htm
15. Ramos D, Angulo P, Chavera A, Ayón M. Propuesta de un modelo experimental de esteritis aguda inducida por indometacina en ratas albinas. Rev Inv Vet Perú. 2004;15(1):37-43.
16. Zúñiga J, Tur J, Milocco S, Piñero R. Ciencia y tecnología en protección y experimentación animal, Madrid: Ed. McGraw Hill-Interamericana; 2001. p. 3-22.
17. Yamada T, Deitch E, Specian R, Perry M, Sartor R, Grisham B. Mechanisms of acute and chronic intestinal inflammation induced by indomethacin. Inflammation. 1993;17(6):641-62.
18. Anthony A, Pouder R, Dhillon A, Wakefied A. Similarities between ileal Crohn´s disease and indomethacin experimental jejunal ulcers in the rat. Aliment Pharmacol Ther. 2000;14:241-5.
19. Elson C, Sartor B, Tennyson G, Riddell R. Experimental models of inflammatory bowel disease. Gastroenterology. 1995;109:1344-57.
20. Baggio C. Mecanismos envolvidos na atividade gastroprotetora do extrato aquoso dos folhas de Achillea millefolium L. [Tesis de maestría]. Setor de Ciências Biológicas da Universidade Federal do Paraná. Brasil: Programa de Pós-Graduação em Farmacologia do Departamento de Farmacologia; 2004. p. 150. Disponible en: http://dspace.c3sl.ufpr.br/dspace/bitstream/handle/1884/22372/DISSERTACAO%20COMPLETA.pdf?sequence=1
21. Molina Martínez JL, Cuesta Mazorra M, Silveira Prado EA, Castro Gutiérrez M, González Madariaga Yl, Sánchez Álvarez C, et al. Electroacupuntura en el tratamiento de la colitis ulcerosa experimental en ratas Sprague Dawley. REDVET Rev electrónica de Veterinaria. 2010;11(8):1-14. ]]>
22. Porras M. Inflamación intestinal y dismotilidad en un modelo experimental de enfermedad inflamatoria intestinal en la rata: mecanismos de acción implicados en la ciclicidad y cronicidad. [Tesis doctoral]. Universidad autónoma de Barcelona: Facultad de veterinaria; 2006. p. 65-71. Disponible en: http://www.tdx.cat/bitstream/handle/10803/3775/mpp1de1.pdf;jsessionid=CF67CB10E69B062B389CD6514447B851.tdx2?sequence=1
23. Kumar R, Sivakumar T, Sunderam R, Gupta M, Mazumdar U, Gomathi P, et al. Antioxidant and antimicrobial activities of Bauhinia racemosa L. stem bark. Brazilian J med biological research. 2005;38:1015-24.
24. Lichtman SN, Sator RB. Extra intestinal manifestations of IBD, clinical aspects and natural history. Inflammatory bowel disease from bench to beside. Baltimore: Eds. Williams & Wilking; 1994. p. 327-36.
25. Giraldo L, Hernández M, Angulo P, Fuertes C. Actividad antinitrosativa y antiinflamatoria de los flavonoides de las hojas de Uncaria tomentosa Willd. D.C. (Uña de gato). Rev Soc Quim. Perú. 2003;69(4):229-42.
26. Aceituno M, Panés J. Patogenia e inmunoterapia de la enfermedad inflamatoria intestinal: lecciones de los modelos animales. Gastroenterol Hepatol. 2005;28(9):576-90
27. Midwood KS, Williams LV, Schwarzbauer JE. Tissue repair and the dynamics of the extracellular matrix. The International Journal of Biochemistry & Cell Biology. 2004;36(6):1031-37
28. Shils M, Olson J, Shike M, Ross A. Diet and nutrition in case of the patient with surgery, trauma and sepsis. Modern nutrition in health and disease. 1999;7:1589-90.
29. Rao C, Ghosh A. Does metronidazole reduce lipid peroxidation in burn injuries. Indian J Pharmacol.1997;29:30-2.
30. Paglia D, Valentine W. Studies on the quantitative and qualitative characterization of erythrocyte glutathione peroxidase. J Lab Clin Med. 1967;70:158-69.
31. Bailón E. UR-1505, ¿un nuevo salicilato para la enfermedad inflamatoria intestinal? [Tesis doctoral]. Universidad de Granada. España: Departamento de Farmacología. Facultad de farmacia; 2009. p. 211. Disponible en: http://tesis.com.es/documentos/ur1505-nuevo-salicilato-enfermedad-inflamatoria-intestinal/
32. Ramírez I. Efecto de la administración oral de extractos vegetales con actividad antioxidante, sobre los niveles sanguíneos de glutatión peroxidasa en la rata [Tesis de pregrado]. Universidad de San Carlos de Guatemala: Facultad de ciencias químicas y farmacia. Guatemala; 2004. p. 72. Disponible en: http://biblioteca.usac.edu.gt/tesis/06/06_2263.pdf
]]>
Recibido: 12 de enero de 2012.
Aprobado: 17 de junio de 2012.
Liliana Francis Turner. Universidad del Tolima. Colombia. A.A 546. Barrio Santa Elena. Universidad del Tolima. Teléf.: 578-2779049, ext. 9358. Correos electrónicos: lilycolcuba@gmail.com; lfrancist@ut.edu.co ]]>