ARTÍCULO ORIGINAL
Avaliação da atividade antibacteriana das cascas das raízes de Xylosma ciliatifolia (Clos) Eichler (Flacourtiaceae/Salicaceae sensu lato)
Validación de la actividad antibacteriana de corteza de raíces de Xylosma ciliatifolia (Clos) Eichler (Flacourtiaceae/Salicaceae sensu lato)
Validation of the antibacterial activity of root bark of Xylosma ciliatifolia (Clos) Eichler (Flacourtiaceae/Salicaceae sensu lato) ]]>
MSc. Andressa Frizzo Philippsen, Dr. Obdulio Gomes Miguel, Dra. Marílis Dallarmi Miguel, Dra. Cristina Peitz de Lima, MSc. Milena Kalegari, Dra. Ana Luísa Lacava Lordello
Universidade Federal do Paraná. Curitiba/PR, Brasil.
Introdução: Xylosma ciliatifolia (Clos) Eichler (Flacourtiaceae/Salicaceae sensu lato), espécie conhecida popularmente como sucará, açucará ou espinho-de-judeu é uma árvore de pequeno porte, que se desenvolve em regiões de vegetação de mata ciliar. ]]>
Objetivos: avaliar o potencial antibacteriano de frações e substância isolada das cascas das raízes de Xylosma ciliatifolia sobre Staphylococcus aureus, Staphylococcus epidermidis, Salmonella typhimurium e Escherichia coli.
Métodos: o material vegetal seco foi extraído em etanol 96 % em aparelho de Soxhlet com aquecimento. O extrato etanólico obtido foi submetido à partição líquido-líquido em hexano, clorofórmio e acetato de etila e, após, concentrados em banho-maria, obtendo-se, respectivamente, as frações hexano, clorofórmio e acetato de etila. Por cromatografia em coluna da fração hexano obteve-se o composto ugandensidial. A atividade antibacteriana foi avaliada pelo ensaio da difusão em disco e pela medida da concentração inibitória mínima.
Resultados: a atividade antibacteriana foi evidenciada nas frações hexano e clorofórmio sobre as bactérias: Staphylococcus aureus e Staphylococcus epidermidis. O composto ugandensidial mostrou-se ainda mais bioativo sobre as cepas Staphylococcus aureus e Staphylococcus epidermidis com inibição do crescimento bacteriano na concentração de 62,5 µg/mL.
Conclusão: os ensaios antibacterianos realizados neste trabalho com as cascas das raízes de Xylosma ciliatifolia foram capazes de inibir o crescimento de duas cepas gram positivas. Estes resultados contribuem para o conhecimento fitoquímico dessa espécie vegetal que ainda não apresenta dados em literaturas científicas.
Palavras chave: Xylosma ciliatifolia, Flacourtiaceae (Salicaceae sensu lato), ugandensidial, atividade antibacteriana.
Introducción: Xylosma ciliatifolia (Clos) Eichler (Flacourtiaceae/Salicaceae sensu lato), especie conocida en la población como sucará, acucará o espinho-de-judeu es un árbol de pequeño porte, que se desarrolla en las regiones de vegetación de ribera.
Objetivos: evaluar la actividad antibacteriana de las fracciones y sustancias aisladas de la corteza de raíces de Xylosma ciliatifolia sobre Staphylococcus aureus, Staphylococcus epidermidis, Salmonella typhimurium y Escherichia coli.
Métodos: el material seco se extrajo en etanol 96 % en un aparato de Soxhlet con calentamiento. El extracto etanólico obtenido se sometió a partición líquido-líquido en hexano, cloroformo y acetato de etilo; después se concentró en un baño de agua, produciendo, respectivamente, las fracciones hexano, cloroformo y acetato de etilo. Por cromatografía de columna de la fracción hexano se obtuvo el compuesto ugandensidial. La actividad antibacteriana se evaluó mediante la prueba de la difusión en disco y mediante la medición de la concentración inhibitoria mínima.
Resultados: la actividad antibacteriana se observó en las fracciones hexano y cloroformo sobre las bacterias: Staphylococcus aureus y Staphylococcus epidermidis. El compuesto ugandensidial resultó aún más bioactivo sobre las bacterias Staphylococcus aureus y Staphylococcus epidermidis, con inhibición del crecimiento bacteriano en la concentración de 62,5 µg/mL. ]]>
Conclusiones: los ensayos antibacterianos realizados en este estudio con corteza de raíces de Xylosma ciliatifolia fueron capaces de inhibir el crecimiento de ambas cepas grampositivas. Estos resultados contribuyen al conocimiento fitoquímico de esa especie vegetal que aún no presenta datos en la literatura científica.
Palabras clave: Xylosma ciliatifolia, Flacourtiaceae (Salicaceae sensu lato), ugandensidial, actividad antibacteriana.
Introduction: Xylosma ciliatifolia (Clos) Eichler (Flacourtiaceae/Salicaceae sensu lato), a species known by the general public as sucara, acucara or espinho-de-judeu, is a small tree growing in riverside areas.
Objectives: evaluate the antibacterial activity of fractions and substances isolated from root bark of Xylosma ciliatifolia against Staphylococcus aureus, Staphylococcus epidermis, Salmonella typhimurium and Escherichia coli.
Methods: the dry material was extracted into 96% ethanol in a Soxhlet device with heating. The ethanolic extract thus obtained was subjected to liquid-liquid partition in hexane, chloroform and ethyl acetate. It was then concentrated in a water bath to obtain hexane, chloroform and ethyl acetate fractions, respectively. The ugandensidial compound was obtained by column chromatography of the hexane fraction. Antibacterial activity was evaluated by the disc diffusion test and by measurement of the minimum inhibitory concentration.
Results: antibacterial activity against Staphylococcus aureus and Staphylococcus epidermis was observed in the hexane and chloroform fractions. The ugandensidial compound was found to be even more bioactive against the bacteria Staphylococcus aureus and Staphylococcus epidermis, with inhibition of bacterial growth in the 62.5 µg/mL concentration.
Conclusions: the antibacterial assays conducted in this study with root bark of Xylosma ciliatifolia revealed inhibition in the growth of both gram-positive strains. These results provide phytochemical information about this plant species, for which there are no data in the scientific literature.
Key words: Xylosma ciliatifolia, Flacourtiaceae (Salicaceae sensu lato), ugandensidial, antibacterial activity.
]]>
INTRODUÇÃO
O estabelecimento de regras efetivas para o uso racional de antibióticos e o incentivo para estudos que envolvam a pesquisa de novas drogas são os principais objetivos atuais para a manutenção do controle das doenças de origem infecciosa.
Recentemente, a Agência Nacional de Vigilância Sanitária publicou uma resolução (RDC Nº 20, de 5 de maio de 2011), que dispõe sobre o controle de medicamentos à base de substâncias classificadas como antimicrobianos, de uso sob prescrição médica, tanto na forma isolada quanto em associação. Conforme a legislação, a dispensação dos medicamentos disponíveis no mercado será de caráter controlado em virtude do uso disseminado e não criterioso até então realizado.1 A administração não adequada dos antimicrobianos acarretou no aparecimento de patógenos resistentes aos antibióticos. Aliado aos prejuízos para a saúde dos cidadãos há a elevação dos gastos públicos relacionados aos tratamentos extras e à assistência médica.2
Atentando-se para o fenômeno da resistência dos microrganismos aos medicamentos de uso convencional, a pesquisa de espécies vegetais pouco conhecidas é incentivada na busca de novas drogas. Isto se deve ao fato de que o metabolismo das plantas apresenta várias rotas de síntese secundárias, capazes de originar diferentes classes de compostos como alcaloides, flavonoides, taninos, cumarinas, glicosídeos, terpenos, entre outros.3 A riqueza de estruturas químicas sintetizadas pelas plantas constitui uma importante alternativa para a introdução de fármacos inovadores na área terapêutica. Atualmente, cerca de 120 substâncias puras isoladas de plantas são utilizadas com finalidade terapêutica.4
Presente entre os exemplares da biodiversidade, a família Flacourtiaceae, ainda pouco estudada sob o ponto de vista terapêutico, está representada por aproximadamente 86 gêneros e 1 300 espécies,5 distribuídas nas Américas, África, Ásia, Austrália e nas costas do Pacífico. Na América do Sul foram catalogados 32 gêneros e, na flora brasileira ocorrem 19 gêneros com 92 espécies.6,7 Em recentes estudos sobre a filogenia das flacourtiáceas, com base no seqüenciamento de plastídeos de rbcL de DNA, foi evidenciado que a família apresenta afinidade junto ao clado das Salicaceae.8 Sendo assim, as publicações recentes utilizam na grande maioria das vezes a descrição da família Flacourtiaceae seguido pela denominação entre parênteses de Salicaceae sensu lato como nomenclatura atual.
Em estudos prévios com algumas espécies da família foram reportadas várias atividades biológicas relevantes, tendo como exemplos: propriedades antibacterianas, antivirais, hipolipêmicas e hipoglicemiantes,9 anti-ofídicas e citotóxica.10,11
Xylosma ciliatifolia (Clos) Eichler, espécie conhecida popularmente como sucará, açucará ou espinho-de-judeu é uma árvore de pequeno porte, que se desenvolve em regiões de vegetação de mata ciliar.12 Esta espécie foi selecionada para os estudos porque até o momento não existem relatos com informações químicas e biológicas em literaturas técnicas e científicas.
Desta maneira, o presente trabalho teve como objetivo avaliar o potencial antibacteriano das cascas das raízes, embasando-se no fato de que, muitas das substâncias obtidas de produtos naturais podem ser fontes promissoras de novos agentes antibióticos frente ao arsenal terapêutico atual, por vezes, não efetivo diante do fenômeno da resistência bacteriana. ]]>
MÉTODOS
Coleta e identificação do material vegetal
As raízes de X. ciliatifolia foram coletadas no município de Curitiba em julho de 2008 (coordenadas 25°42' S e 49°27' W). A identificação botânica da espécie foi realizada no Museu Botânico Municipal de Curitiba pelo botânico Gert Hatschbach, em comparação com a exsicata catalogada no herbário sob o número 208.965.
Extração, fracionamento e isolamento
As cascas das raízes (290 g) secas e trituradas foram extraídas em etanol 96 % em aparelho de Soxhlet sob aquecimento (40 ºC). O extrato etanólico obtido foi submetido à partição líquido-líquido em hexano, clorofórmio e acetato de etila e, após, concentrados em banho-maria, obtendo-se, respectivamente, as frações FH, FC e FA.13
Por cromatografia em coluna da FH isolou-se um composto denominado como Xc2 (252,2 mg). Este foi identificado por RMN 1H e 13C em comparação com dados da literatura. Os espectros foram obtidos utilizando-se o equipamento AC 200 Bruker operando em pulsos seqüenciais de 200 e 50 MHz para 1H e 13C, respectivamente, em clorofórmio deuterado. Tetrametilsilano foi utilizado como padrão interno nas análises. ]]>
Avaliação da atividade antibacteriana
O ensaio da atividade antibacteriana foi realizado frente às cepas de Staphylococcus aureus (ATCC 6538), Staphylococcus epidermidis (ATCC 12228), Salmonella typhimurium (ATCC 14028) e Escherichia coli (ATCC 25922) pelo método de difusão em disco.14 A partir de soluções diluídas de cada uma das frações e substância isolada, foram aplicados 10 µL das amostras em discos estéreis de 6 mm, obtendo-se as concentrações teste de 250, 500 e 1000 µg por disco, em triplicata. Cloranfenicol (30 µg) foi utilizado como controle positivo e metanol (solvente para diluição das amostras) como controle negativo.
Amostras com halos maiores que 7 mm foram consideradas ativas e submetidas ao ensaio da determinação da concentração inibitória mínima (CIM).15 As cepas bacterianas utilizadas nos testes: Staphylococcus aureus (ATCC 6538) e Staphylococcus epidermidis (ATCC 12228) foram reativadas em caldo tríptico de soja e incubadas a 35 °C, 24 h antes do teste. Após o subcultivo, as suspensões dos inóculos foram ajustadas com solução estéril de cloreto de sódio 0,9 % em comparação com o padrão de turbidez do tubo 0,5 da escala de McFarland (1,5 x 108 UFC.mL-1). Em seguida, uma alíquota de 2 mL de cada uma das suspensões bacterianas foi diluída em solução estéril de Tween 80 a 2 %.
O preparo das amostras consistiu na diluição sequencial de cada uma das frações e substância isolada nas concentrações que variaram de 500 a 7,8 µg/mL (proporções de 1:1, 1:2, 1:4, 1:8, 1:16, 1:32 e 1:64) em caldo tríptico de soja. Cada tubo contendo a amostra na respectiva concentração recebeu 1 mL da suspensão bacteriana e 1 mL do caldo tríptico de soja. No tubo utilizado como controle positivo foi utilizado o caldo de cultura e a suspensão de bactérias. O controle negativo foi composto somente pelo caldo de cultura e a amostra.
A CIM foi definida pela visualização do último tubo na qual a amostra inibiu o crescimento de microrganismos em comparação ao controle negativo.
RESULTADOS ]]>
No estudo realizado neste trabalho, as frações FH e FC mostraram-se ativas frente às cepas de S. aureus e S. epidermidis em todas as concentrações testadas. A fração FA não apresentou inibição sobre o crescimento das cepas teste. Os halos de inibição para as frações FH e FC apresentaram valores médios de 9,16 mm (250 µg) e 9,33 mm (250 µg), para a cepa de S. aureus. Para o microrganismo S. epidermidis foi verificada a formação de halos médios de 10 mm (250 µg) e 9,66 mm (250 µg), respectivamente, para as frações FH e FC. A CIM das frações hexano e clorofórmio apresentaram valores que variaram de 250 a 500 µg/mL (tabela 1).
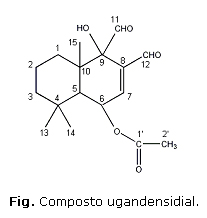
Da fração hexano foi isolada uma substância denominada de Xc2. O composto Xc2 foi identificado em comparação com dados espectroscópicos de RMN 1H e de RMN 13C de outras substâncias estruturalmente semelhantes,16 como sendo o composto ugandensidial (6-acetoxi-9-alfa-hidroxidrim-7-eno-11,12-dial) (Fig.).
O isolado Xc2 ugandensidial apresentou atividade inibidora sobre o crescimento de duas cepas bacterianas: S. aureus e S. epidermidis (tabela 2). Foram observados halos de inibição entre 15 e 19 mm de diâmetro nas concentrações testadas. Os valores de CIM para os dois microrganismos foram de 62,5 µg/mL.
DISCUSSÃO
Os resultados obtidos neste trabalho evidenciaram que a atividade antibacteriana das cascas das raízes de X. ciliatifolia pode ser atribuída em grande parte ao composto ugandensial, isolado da fração hexano que também demonstrou biatividade sobre as cepas de S. aureus e S. epidermidis. Estes dados representam um novo achado no estudo da fitoquímica de espécies vegetais, pois até o momento não existem relatos em literaturas científicas com informações químicas e biológicas sobre X. ciliatifolia. ]]>
A substância ugandensidial - um sesquiterpeno dialdeído da classe dos drimanos - foi igualmente isolada das espécies medicinais africanas: Warburgia stuhlmanii e Warburgia ugandensis (Canelaceae), sendo que a última espécie citada é utilizada para tratamento de dores de estômago, constipação, dores de dente, febre e dores musculares.17Dentre os diferentes compostos conhecidos da classe dos sesquiterpenos dialdeídos muitos apresentam atividade antimicrobiana comprovada. Poligodial, um dos prováveis precursores do composto ugandensidial apresentou atividade inibidora do crescimento bacteriano, com valores de CIM de 100 µg/mL, em estudo realizado sobre sete diferentes cepas de S. aureus.18 Os mesmos autores relataram que o mecanismo da ação antibacteriana do poligodial pode estar relacionado ao efeito surfactante da molécula, ocorrendo o rompimento das proteínas integrais na camada lipo-protéica das membranas com a consequente inibição das funções celulares.
Desta maneira, pode-se considerar que o efeito antibacteriano obtido neste trabalho para o composto isolado - ugandensidial (CIM= 62,5 µg/mL) mostrou-se ainda mais expressivo quando comparado aos resultados descritos anteriormente na literatura.
Jansen & Groot19 em revisão publicada sobre esta classe de sesquiterpenos relataram que os compostos apresentam atividades antimicrobianas sobre diversas espécies patogênicas de bactérias, fungos, vírus e helmintos. Do ponto de vista químico, Jonassohn20 descreveu que a porção da molécula dos sesquiterpenos formada pelo grupamento aldeído a, ß-insaturado está fortemente ligada às atividades biológicas reportadas para esta classe de compostos.
Relatos de atividade antimicrobiana para este mesmo gênero da família Flacourtiaceae foram publicados a partir dos estudos realizados com as espécies Xylosma terrae-reginae e Xylosma sp. Na pesquisa, o extrato metanólico das raízes de Xylosma terrae-reginae mostrou atividade moderada contra S. aureus e Candida albicans, com valores de CIM de 2,5 mg/mL e 1,2 mg/mL, respectivamente.21
Castro e outros22 realizaram um estudo para avaliar a atividade antibacteriana in vitro de diferentes extratos de plantas brasileiras contra bactérias patogênicas para peixes. Dentre as espécies avaliadas, as folhas de Xylosma sp. II apresentaram inibição do crescimento de Flavobacterium columnare com valor de 375 µg/mL para a concentração inibitória mínima.
Os resultados obtidos constituem em grande incentivo para a continuidade dos estudos de avaliação da atividade antibacteriana da espécie X. ciliatifolia, bem como, para pesquisa e identificação de outros compostos com potencial farmacológico.
AGRADECIMENTOS ]]>
Os autores agradecem ao apoio financeiro da Fundação Araucária e ao botânico Gert Hatschbach, do Museu Botânico de Curitiba, pela identificação da espécie.
REFERÊNCIAS
1. Brasil. Resolução da Diretoria Colegiada nº 20, de 5 de maio de 2011. Dispõe sobre o controle de medicamentos à base de substâncias classificadas como antimicrobianos, de uso sob prescrição, isoladas ou em associação. Diário Oficial da União. 9 de maio de 2011. Seção 1.
2. Hardman JG, Limbird LE, Gilman AG. Goodman e Gilman: As bases farmacológicas da terapêutica. Rio de Janeiro: McGraw-Hill; 2003. p. 859.
3. Bresolin TMB, Cechinel Filho V. Ciências Farmacêuticas: contribuição ao desenvolvimento de novos fármacos e medicamentos. Itajaí: UNIVALI; 2003. p. 136.
4. Kinghorn AD. Pharmacognosy in the 21st century. J Pharm Pharmacol. 2001;53:135-48.
5. Joly AB. Botânica: introdução à taxonomia vegetal. São Paulo: Companhia Editora Nacional; 1998. p. 470.
6. Jaszczerski JC. Flacourtiaceae D.C. do estado do Paraná, Brasil [Mestrado]. Curitiba: Universidade Federal do Parana, Setor de Ciências Biológicas; 1987 . p. 12.
7. Barroso GM, Guimaraes EF, Ichaso CLF, Costa CG, Peixoto AL. Sistemática de Angiospermas do Brasil. São Paulo: Editora da Universidade de São Paulo; 1978. p. 171.
8. Mosaddik MA, Forster PI, Booth R, Waterman PG. Phenolic glycosides from some Australian species of Flacourtiaceae (Salicaceae sensu lato). Biochem Syst Ecol. 2007;35:166-8.
9. Xing-Yun C, Ya-Nan L, Hong-Yan R, Peng-Fei T. Advances in studies on chemical constituents and bioactivities of plants from Flacourtiaceae. Zhongguo Zhong Yao Za Zhi. 2006;31:269-79.
10. Recio MC, Giner RM, Máñez S, Talens A, Cubells L, Gueno J, et al. Anti-inflammatory activity of flavonol glycosides from Erythrospermum monticolum depending on single or repeated local TPA administration. Planta Med. 1995;61:502-4.
11. Esteves I, Souza IR, Rodrigues M, Cardoso LGV, Santos LS, Sertie JAA, et al. Gastric antiulcer and anti-inflammatory activities of the essential oil from Casearia sylvestris Sw. J Ethnopharmacol. 2005;101:191-6.
12. Marquete R. Reserva Ecológica do IBGE (Brasília - DF): Flacourtiaceae. Rodriguésia. 2001;52:5-16.
13. Carvalho JLS. Contribuição ao estudo fitoquímico e analítico do Nasturtium officinale R. BR., Brassicaceae [Mestrado]. Curitiba: Universidade Federal do Paraná, Mestrado em Ciências Farmacêuticas; 2001.
14. Romeiro RS. Métodos em bacteriologia de plantas. Viçosa: UFV; 2001. p. 127-62
15. Koneman EW, Allen SD, Dowwel Jr VR, Sommers HM. Diagnóstico microbiológico - texto e atlas colorido. São Paulo: Medicina Panamericana Editora do Brasil; 1993.
16. Cortes M, Razmilic I, Lopez J. Synthesis of (-)-ugandensidial. J Nat Prod. 1990;53:1369-71.
17. Wube AA, Bucar F, Gibbons S, Asres K. Sesquiterpenes from Warburgia ugandensis and their antimycobacterial activity. Phytochemistry. 2005;66:2309-15. ]]>
18. Kubo I, Fujita K, Lee SH, Ha TJ. Antibacterial activity of polygodial. Phytother Res. 2005;19:1013-7.
19. Jansen BJM, Groot AD. Occurrence, biological activity and synthesis of drimane sesquiterpenoids. Nat Prod Rep. 2004;21:449-77.
20. Jonasson M. Sesquiterpenoid unsaturated dialdehydes. Sweden: Lund University; 1996.
21. Mosaddik MA, Forster PI, Booth R, Waterman PG. Screening of some Australian Flacourtiaceae species for in vitro antioxidant, cytotoxic and antimicrobial activity. Phytomedicine. 2004,11:461-6.
22. Castro SBR, Leal CAG, Freire FR, Carvalho DA, Oliveira DF, Figueiredo HCP. Antibacterial activity of plant extracts from Brazil against fish pathogenic bacteria. Braz J Microbiol. 2008,39:756-60. ]]>
Recibido: 5 de junio de 2012.
Aprobado: 30 de diciembre de 2012.
Andressa Frizzo Philippsen. Departamento de Farmácia, Laboratório de Fitoquímica. Universidade Federal do Paraná, Rua Prefeito Lothário Meissner 632. Jardim Botânico, 80210-170. Curitiba/PR, Brasil. Telef.: (41) 33604066. Correio eletrônico: andifp@bol.com.br ]]>