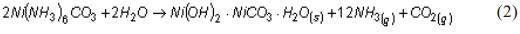
Medición del pH durante la destilación del licor producto del proceso Caron. Parte (III)
Measuring the pH During the Distillation Product of the Process Liquored. Part (III)
Ing. Armando Rojas-Vargas, Ing. María Elena Trujillo-Nieves
Centro de Investigaciones del Níquel (CEINNIQ), Moa, Holguín, Cuba. arojas@eros.moa.minbas.cu
]]>
Resumen
Se refleja la importancia de la medición del pH durante la destilación del licor producto procedente del proceso de Lixiviación Carbonato Amoniacal de níquel. La evaluación se realizó en una columna de destilación industrial, operada mediante el Sistema de Supervisión y Control de Procesos Tecnológicos EROS. El rango de flujo de licor alimentado fue de 25 m3/h y para la temperatura en el tope, 10 ºC. La concentración de amoníaco, dióxido de carbono, azufre y níquel del licor alimentado fue variable. La concentración de amoníaco posee una dependencia potencial del pH en la descarga de la columna y el níquel, polinomial de segundo orden. Se determinó el pH de la pulpa de descarga para el cual el costo es mínimo en cuanto a consumo de reactivo de precipitación de níquel y pérdidas de amoníaco, recomendando un rango entre 8,10 d≤ pH d≤ 8,30 con una pérdida mínima de 0,111 C.U.C./(m3/h) y un ahorro de 0,674 C.U.C./(m3/h). Un incremento de la concentración de azufre en el licor alimentado, incrementa la disolución del níquel y los gastos de operación. Se obtuvo una ecuación para predecir la concentración de níquel en el efluente de la destilación en dependencia de la concentración de azufre en el licor alimentado y del pH en la descarga de la columna.
Palabras clave: amoníaco, níquel, destilación.
Abstract
The importance of pH mensuration during product liquor distillation coming from ammonium carbonates leaching of nickel Was studied. The evaluation Was carried out in a column of industrial distillation, operated by means of Supervisory Control and Data Acquisition EROS. The range of fed liquor Was 25 m3/h and of temperature at the top, 10 ºC. The ammonia concentration Was variable, as well as dioxide of carbon, sulfur and nickel of the fed liquor. The concentration of ammonia possesses a potential dependence of the pH in the unload of the column and the nickel, polynomial of second order. The pH of the discharge pulp Was determined for which the cost is minimum as for consumption of reagent of nickel precipitation and losses of ammonia, recommending a range among 8,10 d≤ pH d≤ 8,30 with a minimum loss of 0,111 C.U.C./(m3/h) and a saving of 0,674 C.U.C./(m3/h). An increase of the concentration of sulphur in the fed liquor, increases the dissolution of the nickel and of the expenses of operation. An equation Was obtained to predict of the nickel concentration in the effluent of the distillation in dependence of sulfur concentration in the fed liquor and the pH in the discharge of the column.
Keywords: ammonium, nickel, distillation.
INTRODUCCION
]]> Este trabajo centra su atención en el proceso de extracción de níquel y cobalto por la Tecnología Carbonato-Amoniacal (TCA) o proceso «Caron», específicamente, en la etapa de destilación del Licor Producto. Este licor se obtiene al poner en contactoel mineral reducido con el licor carbonato amoniacal en presencia de oxígeno, cuya reacción química principal se representa por la ecuación (1) donde x toma valores para (Fe) y (Cu) de 2, 3 y 4 y para el (Ni) y (Co) de 2, 3, 4, 5 y 6 [1, 2].En las torres de destilación, se pone en contacto directo el Licor Producto con el vapor de agua y se obtienen como productos, por el fondo una suspensión carbonato de níquel–agua con níquel y amoníaco disuelto y por el tope, gases con contenido de amoníaco y dióxido de carbono enviados a absorción, como se refleja por la reacción (2).
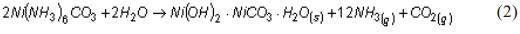
Posterior a la sedimentación, el níquel disuelto no recuperado en forma de carbonato, precipita en un reactor tubular; mientras que el amoníaco constituye una pérdida. Estudios desarrollados en una minicolumna de destilación [4-6], reflejaron la relación entre el pH y la concentración de níquel y amoníaco disuelto, indicando los valores en los que se realiza una sobre destilación o redisolución de níquel, incrementando los costos por consumo de vapor y de reactivo de precipitación, o en caso contrario, subdestilación incrementando las pérdidas de amoníaco y también de níquel. En la medida que el pH de la suspensión disminuye su carácter básico, disminuye la concentración de amoníaco y de níquel, pero a partir de determinado pH, el carbonato de níquel se redisuelve.
Este trabajo tuvo como objetivos: verificar los resultados obtenidos en la minicolumna de destilación, en una columna industrial; determinar el pH de la pulpa de descarga para el cual el costo de operación es mínimo en cuanto a consumo de reactivo de precipitación de níquel y pérdidas de amoníaco y determinar la influencia del azufre disuelto en el licor sobre el incremento de los costos.
FUNDAMENTO TEORICO
En la suspensión carbonato de níquel-agua suceden varias reacciones en equilibrio, como se resumen en la tabla 1. Cuando el amoníaco se disuelve en agua, parte del gas disuelto reacciona (5) para formar hidróxido de amonio que se disocia parcialmente en sus iones (6). El amoníaco disuelto sin ionizar depende de la ley de Henry [14, 15], donde KHa[18, 20] representa su constante y P representa la presión parcial.
El dióxido de carbono es un anhídrido ácido, cuando se disuelve en agua baja el pH de la disolución. La disolución ocurre en tres pasos, interviniendo en cada uno, un equilibrio químico. El primer paso (8) es la disolución del CO2 en agua para formar el ácido carbónico, su constante de equilibrio es la constante de la Ley de Henry del CO2(KHC) [16,18]; el segundo, la reacción ácido-base (9) de obtención de bicarbonato; el tercero (10) es la formación del carbonato. El dióxido de azufre reacciona con el agua para formar el ión bisulfito (13) y sulfito (14), siendo su constante de Henry (KHS) [17].
Tabla 1 ]]> Reacciones de equilibrio, expresión de la constante de equilibrio Sistema NH3-SO2-CO2-H2O
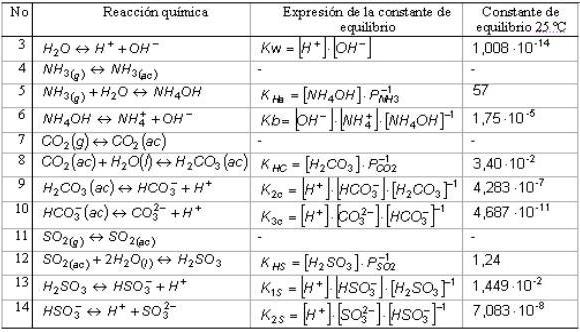
La constante de equilibrio [13] se puede calcular por la ecuación (15) para las reacciones reflejadas en la tabla 2 y además, verificarse mediante otros modelos reflejados en la literatura para CO2-H2O, SO2-H2O [16, 17].
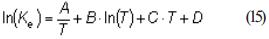
Tabla 2
Parámetros para estimar la constante de equilibrio, ecuación (10)
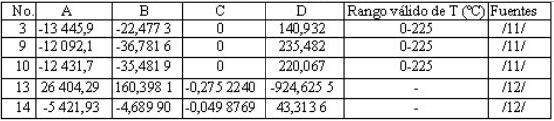
En la suspensión carbonato de níquel–agua, la concentración de azufre ha alcanzado valores de 2,01 g/l +/- 0,41, amoníaco 1,32 g/l +/- 0,36 y CO2 de 119 ppm. +/- 50,1 (promedio +/- desviación estándar) [6]. Puede ocurrir un desplazamiento del carbonato por la siguiente reacción irreversible, incluso hasta desprenderse el CO2[11].
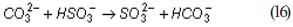
La neutralización de la suspensión se puede plantear según (17). Despreciando la concentración de iones carbonato y sulfito, el equilibrio NH3-CO2-SO2-H2O y su relación con el pH se puede representar por (18) aplicando las ecuaciones (3) a (14). Una caracterización realizada al sistema SO2-NH3-H2O, aplicando técnicas como espectroscopia de absorción (Infrared Absorption Spectra) medición de pH y conductividad eléctrica, determinaron la presencia de especies químicas como H+, OH-, HSO3-, SO32-, NH4+, y formas solvatadas de NH3 y SO2 en cantidad significativa [19].
]]>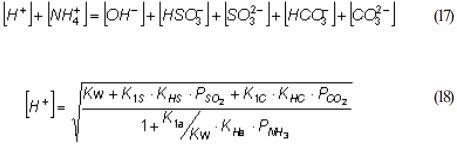
En trabajos reportados tras realizar perfiles de concentración de [Ni] y [NH3] en los platos de las columnas de destilación, se observó que el níquel puede redisolverse por lo que se estableció una norma de concentración de amoníaco en el plato controlante, inicialmente denominado 5to plato [4, 6-8]. En dicho plato se inicia la precipitación profunda del níquel a alrededor de 20 g/l de (NH3) y se obtiene además elevada correlación con la concentración de amoníaco y níquel en la descarga de la columna [6, 7, 8].
La norma de amoníaco en el 5to plato es diferenciada en dependencia de la concentración de azufre en el licor, siendo la concentración de azufre la causa fundamental de su redisolución [3, 5-7]. Las reacciones (19, 20 y 21) pudieran explicar la redisolución del níquel a bajo pH, por lo que es recomendable estudiar la solubilidad del carbonato de níquel en solución sulfato amoniacal mediante un diseño experimental; en [10] se explica la formación de estos complejos por lixiviación sulfato amoniacal de lateritas.
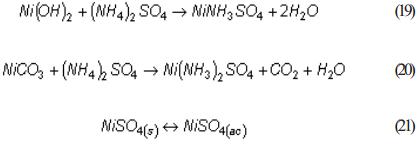
En un estudio donde se realizó la alimentación lateral de licor carbonato amoniacal, enriquecido en CO2, por un plato superior al plato controlante en una mini columna de destilación, se obtuvo un carbonato de níquel más enriquecido en fracciones gruesas (fracción -40 +30 micrones), menor humedad y resistencia específica de la torta; el carbonato de níquel poseyó mayor contenido de CO2 que cuando no se realizó la alimentación lateral, quedando por investigar ¿Cuál es la capacidad de redisolución ante licores de diferente composición iónica en cuanto a concentración de NH3, SO2, CO2 y pH? [6].
MATERIALES Y METODOS
Descripción de la instalación
El estudio de la destilación del licor producto carbonato amoniacal se realizó en una torre de destilación (alambique) a escala industrial, con platos de copas de burbujeo y las especificaciones siguientes:
- Altura total: 18,0 m ]]>
- Diámetro interior: 3,4 m
- Número de platos: 18
- Copas por platos: 24
Para el control de la operación se utiliza el Sistema de Supervisión y Control de Procesos (SCADA) Tecnológicos EROS, el cual permite accionar sobre los autómatas de proceso desde un panel de control; se determina la concentración de amoníaco en el 5to plato y compara con la norma, como medida correctiva se acciona sobre el flujo de vapor o de licor producto, reflejándose en una variación en norma de la temperatura del tope de la columna.
Las variables medidas son: flujo, temperatura y presión del vapor de alimentación, flujo de licor producto de alimentación, temperatura en el tope de la columna y presión en el fondo.
Muestreo
Durante el periodo de evaluación se tomaron muestras de licor producto de alimentación, pulpa en el plato controlante y la descarga cada 4 h. Al licor de alimentación se le determinó concentración de amoníaco, dióxido de carbono, níquel, cobalto, azufre, sulfato, tiosulfato y pH. La pulpa de carbonato de níquel se dejó sedimentar en frascos tapados y se pipeteó directamente el volumen necesario para determinar amoníaco y níquel, en el caso de la descarga, se determinó además dióxido de carbono y azufre. A la pipeta se le adicionó un filtro en la punta, para evitar la succión de carbonato de níquel.
Para el análisis químico se empleó un equipo de Absorción Atómica SP-9, métodos volumétricos y gravimétricos y para la medición del pH, un pHmetro de modelo Philips PW-9420, con precisión de +/-0,01. El pH se midió luego de enfriar la muestra hasta 25 ºC. El carbonato de níquel se almacenó para análisis posteriores.
Procedimiento de análisis
Los datos (Dj) se organizaron según las variantes siguientes:
]]> 1. La concentración (g/l) de azufre y relación amoníaco–dióxido de carbono (NH3/CO2).2. Por relación níquel-azufre (Ni/S) en el licor producto, con la siguiente variabilidad: Ni/S<2,0; 2,0<Ni/S<2,5; Ni/S>2,5 y por relación (NH3/CO2), para un total de cuatro subgrupos (Dj).
Los que a continuación se discuten, se analizan por la variante dos la cual ofreció mayor calidad de ajuste. Para el análisis de la interacción del pH con los gastos de operación por consumo de reactivo de precipitación de níquel y pérdidas de amoníaco, se aplicó el siguiente procedimiento:
1. Cálculo del flujo de pulpa por el fondo del alambique (Wf) considerando que se incrementa un 15 % con respecto al flujo alimentado (Wa) por condensación del vapor (ecuación 22).
2. Cálculo de la concentración de sólidos (ecuación 23).
3. Cálculo del flujo de licor por el fondo del alambique (ecuación 24)
4. Cálculo de la concentración de amoníaco y níquel en el efluente del alambique para varios valores de pHien la descarga, aplicando las ecuaciones obtenidas para cada grupo Dj.
5. Determinación del costo para cada pHicomo la suma del costo por pérdida de amoníaco y por consumo de reactivo de precipitación de níquel.
6. Multiplicación del costo para cada pHi, por la frecuencia fi con que apareció ese valor de pHi del Grupo Dj.
7. Cálculo de la sumatoria de los costos correspondientes a cada pHi del grupo Dj
]]> 8. Cálculo de la sumatoria del producto de los costos del grupo Dj por la frecuencia con que este aparece fj (los pasos del 4 al 8 por la ecuación 25)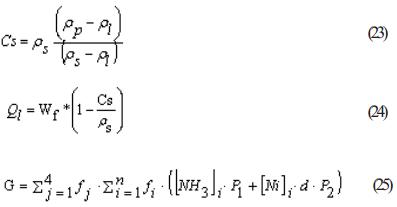
RESULTADOS Y DISCUSION
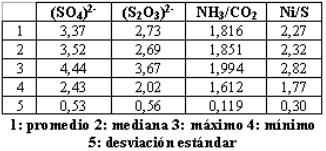
En la tabla 3 se muestra la concentración de algunos componentes en el licor producto, como es el caso de iones sulfato (g/L), tiosulfato (g/L) y la relación amoníaco/dióxido de carbono y níquel/azufre.
Tabla 3
Caracterización del licor producto
En cuanto a la operación del alambique industrial, el rango de temperatura en el tope fue de 10 ºC y el flujo de licor alimentado, 25 m3/h. La relación flujo de licor alimentado/flujo de vapor tuvo un valor promedio de 5,28 y una desviación estándar de 1,32. Estos datos se generaron directamente del SCADA EROS.
Resultados de la interacción del pH con la concentración de amoníaco y níquel en el plato controlante y en el efluente
]]> Se analizó la interacción entre el pH con la concentración de amoníaco y níquel en el plato controlante y la descarga (o efluente) del alambique. En la figura 1 se muestra dicha interacción para el subgrupo de datos D1, con relación NH3/CO2 entre 1,81-2,0 y de Ni/S entre 1,77-2,0. Tal como ocurrió con los resultados obtenidos a escala de banco [2, 3], en la medida que disminuye el pH, disminuye la concentración de amoníaco, siendo el comportamiento de forma potencial (27); mientras que el contenido de níquel disminuye hasta un mínimo de concentración y posteriormente comienza a redisolverse (sobre destilación), siendo el comportamiento parabólico (26). Para el resto de los subgrupos se obtuvieron ecuaciones homólogas a la (26) y (27), con estadígrafos de regresión (R2) entre 0,95 – 0,97 para el níquel y 0,92 – 0,94 para el amoníaco.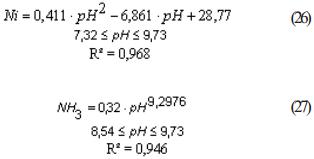
Como se observa en la figura 1, a valores de pH en el intervalo de 8,2<pH<8,5 se obtuvieron bajas concentraciones de níquel (g/l) en el licor efluente del alambique, con valor promedio de 0,232 g/l, correspondiente a una concentración de amoníaco entre 1,71<NH3<1,81 (en g/l). A pH inferiores a 8,54, el amoníaco disminuyó ajustado a una función lineal con pendiente 0,508, intercepto 2,460 y R2 = 0,922.
Se obtuvo una ecuación de predicción del contenido de níquel disuelto en el destilado, aplicando el programa Statgraphic en la opción Regresión No Lineal, en función de la concentración de azufre en el licor de alimentación y pH en la descarga del alambique. De acuerdo a este resultado, cuando se incrementa la concentración de azufre, la concentración de níquel en el destilado aumenta y para atenuar este efecto, se debe operar a pH más alcalino. Esta ecuación se puede aplicar para calcular el flujo de reactivo de precipitación de níquel, de alimentación al reactor tubular; dicho flujo de reactivo, depende de la concentración de níquel disuelto y del flujo de licor efluente de la columna.

En la tabla 4 se caracterizan los grupos de muestras, por relación NH3/CO2, Ni/S y S (g/l) en el licor producto alimentado a destilación. Si se comparan los grupos extremos según la figura 2, en D1 se obtienen mayores pérdidas que en D2, poseyendo D1 superior concentración de azufre, igual sucede entre los grupos D3 y D4. Estos resultados confirman el análisis de la ecuación (28) y el azufre como factor causal importante de la redisolución del níquel.
Tabla 4
Caracterización de los grupos de muestras

Sustituyendo valores actualizados de precios de amoníaco y reactivo de precipitación en (25), podrán establecerse nuevos rangos de pH. Ahora, bajo las condiciones actuales de operación en cuanto a variación de la composición iónica del licor producto y estado técnico de la instalación ¿será posible estabilizar la operación en el rango recomendado?
Fig. 2 Interacción del pH con el gasto.
En la figura 3 se muestra la frecuencia con que se obtuvieron varios intervalos de pH en la descarga de la columna de destilación durante el período de evaluación, utilizada para determinar los gastos (G) por la ecuación (25). Se propone realizar la medición continua del pH e introducirla como una restricción al lazo de control actual. ¿Cómo realizar la medición efectiva del pH en este sistema?
Fig. 3 Gráfico de frecuencia del pH en la descarga de la columna de destilación Industrial.
CONCLUSIONES
1. Los resultados obtenidos en la minicolumna de destilación se validaron a escala industrial.
]]> 2. Controlar los valores de pH de la pulpa efluente de la destilación permite disminuir la redisolución del níquel, los gastos por pérdidas de amoníaco y consumo de reactivo de precipitación de níquel.3. Operar a un rango de pH entre 8,10 – 8,30 representa un ahorro de 0,674 C.U.C./(m3/h) de licor destilado.
4. Un incremento de la concentración de azufre en el licor alimentado, incrementa la redisolución del níquel y los gastos de operación, requiriéndose operar a pH más alcalino.
5. Se obtuvo una ecuación de predicción de la concentración de níquel disuelto en el efluente de la destilación, en función de la concentración de azufre en el licor producto alimentado y el pH de la suspensión.
NOMENCLATURA
Cs: Concentración de sólidos (kg/m3)
d: Dosis de reactivo de precipitación de níquel (t/t)
Dj: Conjunto de muestras agrupadas según relación NH3/CO2 y Ni/S.
fi: frecuencia con que se obtiene dentro de un mismo grupo Dj, un valor de pHi ]]>
fj: frecuencia con que se obtiene en la descarga, el grupo Dj
G: gastos por pérdidas de amoníaco y consumo de reactivo de precipitación, C.U.C. / (m3/h)
KH: constante de Henry (mol m-3atm-1)
[NH3]i: concentración de amoníaco en la descarga del alambique, para un valor de pH (g/l)
[Ni]i: concentración de níquel en la descarga del alambique, para un valor de pH (g/l)
P: presión parcial (atm)
P1: precio amoníaco anhidro (C.U.C. / t)
P2: precio reactivo precipitación de níquel (C.U.C./t)
pHd: pH en la descarga de un alambique.
Q1: Flujo de licor por el fondo del alambique (m3/h) ]]>
T: temperatura (K)
Wa: pulpa alimentada al alambique (m3/h)
Wf: pulpa efluente del alambique (m3/h)
ρ1: densidad del licor (kg/m3)
ρp: densidad de la partícula (kg/m3)
ρs: densidad del sólido (kg/m3)
BIBLIOGRAFIA
1. CHANG C. A. Conferencia Internacional de aprovechamiento de recursos minerales: CINAREM. Moa, 2000.
]]>2. CHANG, C. A. R. Análisis de la Solubilidad de los complejos Amoniacales de Co (II). Revista Minería y Geología. N1. 1984. Págs. 173-184.
3. CHANG C. A.; ROJAS-VARGAS, A. "La lixiviación del Proceso CARON: síntesis del conocimiento para su perfeccionamiento industrial. Parte 1". Revista Tecnología Química. Vol. XXIX, No. 1. 2009.
4. ROJAS, A., TRUJILLO, M. E. "Medición del pH durante la destilación del licor producto del proceso de lixiviación amoniacal". Revista Tecnología Química. Vol. XXVII No. 1. 2007. Págs. 34-40.
5. ROJAS, A., TRUJILLO, M. E. "Medición del pH durante la destilación del licor producto del proceso de lixiviación amoniacal (II)". Revista Tecnología Química. Vol. XXVII, No. 3. Págs. 56-60, 2007.
6. ROJAS, V. A. et al. Destilación del licor producto en una columna de destilación a escala de banco. Informe de proyecto de investigación. Centro de Investigaciones del Níquel, Unidad de Proyecto, Nicaro, 2006.
]]>7. RODRÍGUEZ, M. C., RODRÍGUEZ, C. R. Disminución del gasto energético y de las pérdidas de níquel en la operación de los alambiques de licor. Informe técnico. Nicaro. 1985.
8. MARZÁN, M. A. Análisis de la relación entre la concentración de amoníaco en el anillo controlante y la descarga de los alambiques de licor. Informe Técnico. Nicaro, 1977.
9. OSSEO-ASARE, S. W. Heterogeneous equilibrium in Ammonia/Laterite Leaching system. Department of materials of Science and Engineering the Pennsylvania State University.
10. KAZUYOSHI SHIMAKAGE, MASAYOSHI HOSHI, TATSUHICO EJIMA. Kinetics and Mechanism of the Ammonia Pressure Leaching of Lateritic Ore Containig Nickel.
11. EDWARD, T. J., MAURER, G., & PRAUSNITZ, J. M. "Vapour liquid equilibria in multicomponent aqueous solutions of volatile weak electrolytes". A.I.Ch.E. Journal, vol. 24 No. 6, 1978. Págs. 966-975.
]]>12. XIA, J., RUMPF, B., & MAURER, G. Solubility of sulfur dioxide in aqueous solutions of acetic acid, sodium acetate, and ammonium acetate in the temperature range from 313 to 393 K at pressures up to 3:3 MPa: Experimental results and comparison with correlations/predictions. Industrial & Engineering Chemistry Research, Vol. 38 No. 3, 1999. Págs. 1149 -1158.
13. S. EBRAHIMIA; C. PICIOREANUA; R. KLEEREBEZEMA; J. J. HEIJNENA; M. C. M. VAN LOOSDRECHTA. Rate-based modelling of SO2 absorption into aqueous NaHCO3=Na2CO3 solutions accompanied by the desorption of CO2. Chemical Engineering Science vol. 58, 2003. Págs. 3589-3600.
14. MCCABE, W.L.; SMITH, J.C. Unit Operation of chemical Engineering. Edición Revolucionaria. La Habana, 1966. Págs. 596.
15. MATOS, T. R., HING, R. C. Aspectos Fundamentales de la Química-Física. Editorial Pueblo y Educación, La Habana, 1976. Págs. 230-232.
16. HARNED, H. S. AND R. DAVIS. The ionization constant of carbonic acid in water and the solubility of carbon dioxide in water and aqueous salt solutions from 0- 50 ºC. J. Am. Soc. Vol. 65, 1943. Págs. 2030-2037.
]]>17. GOLDBERG, R. N. Y PARKER, V.B. "Thermodynamics of Solution of SO2 (g) in Water and Aqueous Sulfur Dioxide Solutions", J. Res. National Bureau of Standards. Vol. 90, No. 5, 1985. Págs. 341.
18. SCOTT, W. D., HOBBS, P. V. The Formation of sulfate in water Droplets. Journal of the atmospheric Sciences. Vol. 24, 1967.
19. SCOTT, W. D.; MCCARTHY, J. L. The System Sulfur Dioxide-Ammonia-Water at 25° C. Ind. Eng. Chem. Fundamen. Vol. 6, No. 1, 1967. Págs. 40-48.
20. CLEGG S. L., BRIMBLECOMBE P. Solubility of ammonia in pure aqueous and multicomponent solutions. J. Phys. Chem., vol. 93 No. 20, 1989. Págs. 7237-7248.
]]> Recibido: Abril 2012
Ing. Armando Rojas-Vargas. Centro de Investigaciones del Níquel (CEINNIQ), Moa, Holguín, Cuba. arojas@eros.moa.minbas.cu
]]>