Introducción
La enfermedad renal crónica se asocia a aumento de riesgo cardiovascular. Además de las alteraciones lipídicas relacionadas a la caída de la función renal, que se suman a los factores de riesgo cardiovascular clásicos, se produce una alteración progresiva en el metabolismo óseo-mineral que promueve calcificaciones vasculares y adiciona riesgo de enfermedad cardiovascular. El trastorno mineral y óseo asociado a enfermedad renal crónica, definido en 2006, integra anormalidades del metabolismo mineral y óseo, esqueléticas y calcificaciones extraesqueléticas, algunas de las cuales comienzan tempranamente en la enfermedad renal crónica.1 La progresión de la enfermedad renal crónica conlleva alteraciones del metabolismo óseo-mineral que se agravan a medida que avanza la enfermedad. Dentro de las alteraciones fisiopatológicas que se reconocen presentes en etapas precoces y que son iniciales se encuentra la regulación descendente (downregulation) de Klotho a nivel renal a pesar de que la disminución de la tasa de filtración glomerular sea leve todavía. La deficiencia de Klotho es una de las primeras causas para la alteración de la homeostasis del fósforo en la enfermedad renal crónica, asociada estrechamente al trastorno mineral y óseo asociado a enfermedad renal crónica. Klotho actúa como correceptor del factor de crecimiento de fibroblastos 23 (FGF23) y su efecto fostatúrico disminuye progresivamente con la disminución del primero.2
El magnesio tiene efectos proosteogénicos dado que promueve la diferenciación de células stem mesenquimales de la médula ósea a osteoblastos y hay varios mecanismos propuestos a través de los que este catión protege de las calcificaciones vasculares. Por otro lado, el exceso de magnesio sérico se asocia a desmineralización ósea y osteomalacia.3 Se acepta que en la enfermedad renal crónica la filtración glomerular de magnesio disminuye con la progresión de la enfermedad y la reabsorción tubular de magnesio se reduce por el daño túbulointersticial lo que produce un aumento de la excreción fraccional de magnesio, situación que en general se mantiene compensando la magnesemia hasta los 30 mL/min/1,73 m2 y luego puede provocar hipermagnesemia.4
En humanos sin enfermedad renal crónica prácticamente no hay publicaciones que aporten conocimiento del comportamiento de analitos e indicadores bioquímicos del metabolismo óseo-mineral y del magnesio, menos aún en jóvenes con tasa de filtración glomerular normal a alta G1 (tasa de filtración glomerular mayor o igual a 90 mL/min/1,73m2) y ligeramente disminuida G2 (tasa de filtración glomerular entre 60 mL/min/1,73m2 y 89 mL/min/1,73m2).
Este grupo de investigación considera importante obtener resultados del comportamiento de estos metabolitos en quienes no tienen enfermedad renal y se encuentran en categoría G1 y G2 de tasa de filtración glomerular. Los mismos aportarán información para futuras investigaciones que la confronten con quienes tienen enfermedad renal crónica en las mismas categorías de tasa de filtración glomerular y franja etaria.
Objetivos
En una muestra de estudiantes sin enfermedad renal, en categorías tempranas de disminución de la tasa de filtración glomerular estimada por clearance de creatinina de 24 h se propuso evaluar:
Valores séricos de magnesio, excreción urinaria de 24 h de magnesio y excreción fraccional de magnesio.
Algunos analitos e indicadores bioquímicos clásicos del metabolismo mineral y óseo: valores séricos de fosfatasa alcalina, parathormona, calcio y fósforo, excreciones urinarias de 24 h de calcio y fósforo, excreción fraccional de calcio y fósforo.
Material y método
Se realizó un estudio analítico de corte transversal donde participaron 61 estudiantes voluntarios de las carreras de Bioquímica y de Licenciatura en Nutrición de la Universidad Nacional del Litoral de la República Argentina, en el periodo comprendido entre noviembre de 2018 y noviembre de 2019, todos ambulatorios. Por protocolo no se incluyeron embarazadas, amputados ni afectados por enfermedades consuntivas o patologías agudas o en tratamiento con diuréticos, vegetarianos o voluntarios con índice de masa corporal extremos (menor de 18 kg/m2 o mayor o igual a 35 kg/m2. Para explorar la presencia de enfermedad renal se utilizó un cuestionario de datos generales e historia clínica que recabó información de antecedentes personales, familiares en relación a patologías diversas y renales en particular, medicación y hábitos de vida. Posteriormente a cada voluntario se midió la tensión arterial y se le practicaron análisis bioquímicos. A los estudiantes que presentaron alguna alteración compatible con la definición de enfermedad renal crónica se les repitieron los análisis a los tres meses. Los estudiantes que reiteraron en ese periodo la alteración quedaron clasificados como personas con enfermedad renal crónica según criterios bioquímicos de la definición de KDIGO 2012. Este trabajo previo fue realizado para definir la muestra de individuos sin enfermedad renal crónica a incluir en el estudio. Así de los 61 participantes se excluyeron seis mujeres y la muestra quedó conformada por 55 estudiantes sin enfermedad renal, 49 mujeres y 6seis varones, de 18 a 35 años, con una mediana de 25 años.
A cada voluntario se determinaron los analitos en estudio en suero o en suero y orina de 24 h, según correspondiera. Se utilizó la ecuación de Walser para verificar la correcta recolección de la orina de 24 h. Se utilizaron diferentes métodos: creatinina: Jaffé cinético trazable a Isotopic Dilution Mass Spectroscopy (IDMS); calcio: NM-BAPTA; fósforo: molibdato de amonio; magnesio: clorofosfanazo-III; parathormona: quimioluminiscencia, fosfatasa alcalina: p-NPP cinético.
Los valores del clearance de creatinina se clasificaron en categorías G de tasa de filtración glomerular según KDIGO 2012, lineamientos que se adoptaron para esta comunicación.5) Levey et al. ratificaron recientemente su empleo para la descripción del nivel de tasa de filtración glomerular independientemente de la presencia o ausencia de enfermedad renal.6
El protocolo fue evaluado y aprobado por el Comité de Ética de la Facultad de Bioquímica y Ciencias Biológicas de la Universidad Nacional del Litoral, incluyó consentimiento informado y cuestionario de datos generales e historia clínica del estudiante y su familia y sus hábitos de vida.
Por estadística se evaluó mediante el test de Shapiro-Wilk si las distribuciones de los datos eran o no normales, aplicando pruebas paramétricas o no, según correspondiere. Se empleó la prueba de rangos de Mann-Whitney para evaluar si existían diferencias entre los valores de los analitos e indicadores según la categoría G. Para evaluar correlación entre magnesio sérico y excreción fraccional de magnesio se usó el coeficiente de Pearson. En todos los casos se utilizó un nivel de confianza del 95 % (p < 0,05) y se utilizó el programa estadístico MedCalc.
Resultados
Los resultados obtenidos de creatinina sérica, clearance de creatinina, calcio, fósforo y magnesio séricos y en orina de 24 h, fosfatasa alcalina y parathormona séricas y la excreción fraccional de calcio, fósforo y magnesio calculadas (Tabla 1).
Tabla 1 Media, desviación estándar y nivel de significación asociado a la prueba de Mann-Whitney (p) de los analitos e indicadores para el total y según categoría G (n = 55)
| Variable | Total Media ± DE n = 55 | G1 Media ± DE n = 46 | G2 Media ± DE n = 9 | p* |
|---|---|---|---|---|
| Creatinina sérica (mg/dL) | 0,77 ± 0,13 | 0,75 ± 0,11 | 0,89 ± 0,16 | 0,0127 |
|
|
107,20 ± 16,71 | 111,41 ± 14,88 | 85,67 ± 3,87 | < 0,0001 |
| Calcio sérico (mg/dL) | 9,28 ± 0,31 | 9,26 ± 0,31 | 9,39 ± 0,32 | 0,1485 |
| Fósforo sérico (mg/dL) | 3,76 ± 0,48 | 3,75 ± 0,49 | 3,81 ± 0,41 | 0,5167 |
| Magnesio sérico (mg/dL) | 2,07 ± 0,13 | 2,10 ± 0,12 | 1,92 ± 0,09 | 0,0003 |
| Fosfatasa alcalina (U/L) | 55,56 ± 14,81 | 55,98 ± 15,70 | 53,44 ± 9,37 | 0,9184 |
| Parathormona (ng/mL) | 38,38 ± 10,62 | 38,49 ± 11,07 | 37,79 ± 8,50 | 0,8289 |
| Calcio urinario (mg/24h) | 140,91 ± 48,94 | 142,41 ± 51,74 | 133,22 ± 32,14 | 0,5241 |
| Fósforo urinario (mg/24h) | 700,96 ± 207,22 | 720,30 ± 211,09 | 602,11 ± 161,43 | 0,1191 |
| Magnesio Urinario (mg/24h) | 82,93 ± 28,24 | 83,91 ± 30,09 | 77,89 ± 16,06 | 0,7761 |
| Excreción fraccional de calcio | 1,04 ± 0,37 | 1,00 ± 0,38 | 1,20 ± 0,29 | 0,0967 |
| Excreción fraccional de fósforo | 12,84 ± 3,78 | 12,72 ± 3,88 | 13,44 ± 3,36 | 0,6087 |
| Excreción fraccional de magnesio | 3,96 ± 1,45 | 3,76 ± 1,45 | 4,93 ± 1,00 | 0,0055 |
Nota: G1: clearance de creatinina mayor o igual a 90 mL/min/1,73m2; G2: clearance de creatinina entre 60 mL/min/1,73 m2 y 89 mL/min/1,73 m2. *Valor hallado al contrastar los valores obtenidos en G1 y G2 con la prueba de Mann-Withney.
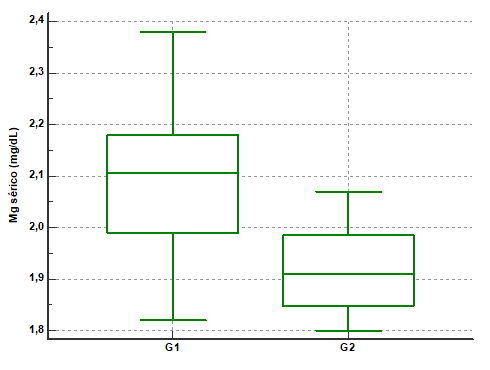
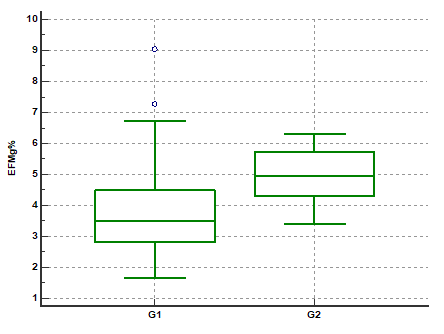
En la muestra no se halló diferencia entre las edades de los estudiantes según categoría G (p = 0,2637). De los analitos e indicadores estudiados, el magnesio sérico y la excreción fraccional de magnesio mostraron diferencias significativas según categoría G (test de Mann-Whitney, p = 0,0003 y p = 0,0055). Los niveles séricos de magnesio se hallaron en todos los casos dentro de los valores de referencia para el método, 1,60 mg/dL a 2,60 mg/dL, por lo que las concentraciones mínima y máxima halladas de 1,80 mg/dL y 2,38 mg/dL, respectivamente. En G2 el magnesio sérico se halló relativamente descendido respecto a G1 (Fig. 1) y la excreción fraccional de magnesio aumentada (Fig. 2).
Se estudió la relación entre la concentración sérica de magnesio y la excreción fraccional de magnesio. Se halló que están inversamente relacionadas. La concentración sérica de magnesio disminuyó, en promedio, 0,26 mg/dL cuando la excreción fraccional de magnesio subió una unidad con un nivel de significación ligeramente superior a 0,05 (p = 0,0502).
No se obtuvo diferencia por categoría G en la excreción fraccional de fósforo (p = 0,6087). Por otro lado, se observó una tendencia a mayor excreción fraccional de calcio en G2, que no fue estadísticamente significativa (p = 0,0967) para el nivel de confianza adoptado.
Discusión
No se hallaron trabajos que hayan estudiado indicadores bioquímicos del metabolismo óseo en individuos sin enfermedad renal, especialmente en personas tan jóvenes y que incluyan el comportamiento del magnesio.
Luján Ramos en un estudio de 2 026 enfermos renales de Antioquía, Colombia, halló hiperfosfatemia en 243 pacientes, 2,89% en G1 y 12,40% en G2; resultaron con hipocalcemia el 1,7 % y el 1,2 % de los evaluados categorizados en G1 y G2, respectivamente. El estudio se realizó en individuos con edad media de 74 años, con enfermedad renal crónica, comorbilidades y tratamientos varios.7) En este trabajo no se encontraron voluntarios con hiperfosfatemia o hipocalcemia ni en G1 ni en G2.
Respecto a la parathormona se ha reportado su incremento al pasar de G1 a G2 en pacientes renales crónicos.8 En la muestra de estudiantes sin enfermedad renal no se observaron variaciones significativas de la concentración de parathormona entre G1 y G2.
Al analizar estos hallazgos en los niveles séricos de las concentraciones de calcio, fósforo, parathormona y de la actividad de fosfatasa alcalina en base a las recomendaciones de controlarlos a partir de que los pacientes con enfermedad renal crónica adultos ingresan a la categoría G3a (tasa de filtración glomerular entre 45 mL/min/1,73 m2 y 59 mL/min/1,73 m2) y los niños a la categoría G2 y se encontraron que los valores estuvieron dentro del rango de referencia y no se hallaron diferencias significativas al comparar entre las categorías G1 y G2.1 No obstante, es útil contar con mayor evidencia de la variación de estos metabolitos en adultos jóvenes con enfermedad renal crónica en las categorías G1 y G2 para valorar su utilidad en el diagnóstico precoz de la trastorno mineral y óseo asociado con enfermedad renal crónica.
Hsiao comparó la excreción fraccional de diferentes electrolitos en pacientes en distintos estadios de enfermedad renal crónica definidos según KDIGO 2002. La media de edad de sus pacientes en G1 era de 51,55 años y en G2 de 60,23 años. Halló una excreción fraccional de magnesio de 2,24 ± 1,45 % en G1 y de 3,30 ± 1,45 % en G2, excreción fraccional de fósforo de 11,53 ± 6,30 % y 14,71 ± 13,05 % y excreción fraccional de calcio 0,99 ± 0,94 % y 0,90 ± 0,83 %, respectivamente. El autor indica las limitaciones de su estudio referidas a que las excreción fraccional fueron calculadas en muestras aisladas.9 En el estudio de Hsiao, que abarca todas las etapas de enfermedad renal crónica, el menor valor hallado para excreción fraccional de calcio fue encontrado en pacientes en G2, situación que no se observó en los estudiantes de la Universidad Nacional del Litoral en G2 sin enfermedad renal. Las diferencias entre los estudios pueden atribuirse a la presencia/ausencia de enfermedad renal crónica en las muestras, al grupo etario o a la metodología para calcular la excreción fraccional (muestra aislada vs. orina de 24 h).
Ferrè en un estudio analizó los valores séricos de magnesio en 2 056 participantes en el Dallas HeartStudy, 44,2 ± 10,0 años, tasa de filtración glomerular estimada por MDRD-4 mayor de 60 mL/min/1,73m2 y albuminuria menor de 30 mg/g al inicio del estudio. En el seguimiento a 7 años halló que magnesio sérico era una variable independiente asociada a la disminución de la tasa de filtración glomerular en la muestra. Por cada 0,2 mg/dL de disminución de magnesio sérico se asoció una disminución media de la tasa de filtración glomerular de 0,23 mL/min/1,73 m2 por año, más acentuado en el grupo de diabéticos que en los no diabéticos.10
Tin estudió 13 226 participantes del estudio Atherosclerosis Risk in Communities, de 45 a 65 años, con una tasa de filtración glomerular estimada mayor o igual a 60 mL/min/1,73m2 seguidos desde los años 1987 a 19889 hasta 2010. Encontró que los riesgos para caer a una tasa de filtración glomerular estimada menor de 60 mL/min/1,73m2 con una disminución de la tasa de filtración glomerular estimada del 25 % respecto al valor basal (en los controles de los tres o nueve años) era 1,5 veces mayor para los que se hallaban en el primer cuartilo, magnesio sérico menor o igual a 1,68 mg/dL, respecto a los del cuarto cuartilo, magnesio sérico mayor o igual a 16 mg/dL.11
Joosten obtuvo resultados similares en participantes del estudio PREVEND, complementando observaciones que asocian bajos niveles de magnesio sérico con riesgo de enfermedad renal crónica.12 En concordancia con los estudios de Ferrè, Tin y Joosten, en un corte transversal los estudiantes de la muestra tienen relativamente más bajo el magnesio sérico en G2 que en G1. Los estudios transversales no permiten demostrar la evolución, pero los resultados concuerdan con los de estos autores. Una de las interpretaciones de la asociación hallada es que la disminución de los niveles de magnesio sérico que se observa al caer el clearance de creatinina se explique por el aumento concomitante de la excreción fraccional de magnesio.
El estudio tiene como limitación que el tamaño de la muestra es pequeño. Los estudios transversales como este son menos potentes que los longitudinales para demostrar causalidad. Los resultados solo pueden extrapolarse a la población de la que provienen los estudiantes.
Conclusión
Los mecanismos que relacionan a la hipomagnesemia con la función renal son varios y están en estudio. Según los resultados en la muestra de estudiantes sin enfermedad renal se observan diferencias significativas en el magnesio sérico y la excreción fraccional de magnesio al comparar los hallazgos en G1 y G2. Los demás indicadores bioquímicos estudiados no mostraron diferencias por categoría G. Deben confirmarse en una muestra mayor y a lo largo del tiempo, con diseños de corte longitudinal. Estas observaciones en individuos sin enfermedad renal pueden contribuir al desarrollo de futuras investigaciones que pueden aportar a la comprensión de cambios bioquímicos del metabolismo óseo-mineral en períodos iniciales de disminución de la tasa de filtración glomerular. Conocerlos facilita tomar tempranamente decisiones médicas que permitan postergar lo máximo posible el impacto de la enfermedad renal crónica en tal metabolismo.