INTRODUCCIÓN
Según la Organización Mundial de la Salud (OMS), 2 000 millones de personas padecen de caries dentales,1 afecta a la mayoría de los adultos; su prevalencia es alta en Europa y Latinoamérica.2 De acuerdo con la Federación Dental Internacional (FDI)3 son la cuarta enfermedad más costosa de atender.
El personal militar corre un alto riesgo de desarrollar afecciones bucodentales debido al tiempo que pasan en los conflictos armados.4 Se destacó una alta prevalencia de caries dental en la Primera Guerra Mundial,5 durante el conflicto en Irak, de cada 100 soldados 10 presentaron caries,6 y un 40 % de los soldados de la operación Atalanta también la manifestaron.7
Streptococcus mutans es una bacteria grampositiva, anaerobia facultativa, se ubica en la cavidad bucal formando parte de la placa dental; es uno de los principales responsables del desarrollo de caries dental debido a la síntesis de polisacáridos extracelulares y la capacidad de metabolizar carbohidratos en ácidos orgánicos que corroen el esmalte dental. Según estudios recientes8,9,10 se ha vuelto resistente a diversas sustancias, tales como la clorhexidina.
Clorhexidina es uno de los antisépticos más importantes usados en odontología como enjuague bucal,8 es muy eficaz contra la inflamación gingival y los índices de placa; presenta un amplio espectro contra bacterias grampositivas y gramnegativas, su actividad puede ser bacteriostática o bactericida, dependiendo de la dosis.11 Diversos investigadores,8,11,12 refieren que el uso prolongado de clorhexidina genera pigmentación marrón de los dientes y reacciones anafilácticas, entre otras.
La familia Solanaceae presenta especies tan importantes como la patata, la berenjena y el tomate; abarca 98 géneros; se caracteriza por incluir desde hierbas pequeñas hasta árboles perennes; se distribuye en todos los continentes excepto en la Antártida, con preferencia por zonas cálidas a tropicales.13 El género Solanum tiene importancia alimentaria, agrícola y medicinal.14
La especie Solanum sessiliflorum Dunal, se distribuye en la Amazonía y se le conoce como cocona.15 Su fruto posee una amplia variedad de efectos terapéuticos como hipolipemiante, antioxidante, antimicrobiano, cicatrizante y antinflamatorio,16,17 su cáscara exhibe constituyentes químicos orgánicos de tipo flavonoides, compuestos fenólicos, carotenoides, vitamina C, pectina, etc.18,19
Las caries dentales representan un problema de salud pública.1,2 Por esta razón, uno de los objetivos de la medicina militar es que la tropa no se vea comprometida con una enfermedad bucodental.20 En consecuencia se deben buscar alternativas a clorhexidina con especies de origen vegetal y que cuenten con investigaciones estructuradas y validadas.
El objetivo de la investigación es evaluar el efecto antibacteriano del extracto hidroalcohólico de Solanum sessiliflorum Dunal (cocona) sobre Streptococcus mutans.
MÉTODOS
Se realizó un estudio experimental, in vitro y comparativo, en el laboratorio de investigación y desarrollo farmacéutico de la Universidad Inca Garcilaso de la Vega, durante los meses comprendidos entre agosto del 2019 y marzo del 2020.
La recolección de la especie vegetal fue aleatorizada en campos de cultivo, cuya ubicación geográfica fue en el distrito de La Banda de Shilcayo, provincia de San Martín, departamento de San Martín en el Norte del Perú. La caracterización taxonómica se realizó en el Herbario del Museo de Historia Natural de la Universidad Nacional Mayor de San Marcos.
Los frutos fueron limpiados, lavados y seleccionados, cerciorándose de que no tuvieran daño en la cáscara y que fueran de similar tamaño y color.15 Después se procedió a separar la cáscara de la pulpa con el manejo de un cuchillo de acero quirúrgico; las cáscaras se cortaron en fracciones pequeñas, posteriormente se realizó el secado a una temperatura de 40 °C ± 2 °C durante 72 horas, luego se trituró en un molino de acero quirúrgico común.15,21
El extracto hidroalcohólico se obtuvo mediante el método de maceración en 1 500 mL de etanol al 70 % con 550 g del pulverizado durante 10 días con agitación cada 12 h,22 después se filtró con papel Whatman N° 40 y se ubicó en una estufa (Memmert®) a 40 °C ± 2 °C hasta agotar el solvente y lograr peso constante, con lo cual se obtuvo 150 g de extracto seco. A continuación, se realizaron diluciones con etanol al 70 %, hasta obtener concentraciones de 25 %, 50 % y 75 %.
La detección de metabolitos secundarios se ejecutó mediante el análisis fitoquímico preliminar, por técnicas químicas de precipitación y coloración, como la reacción de Borntrager (antraquinonas), tricloruro férrico (compuestos fenólicos), Liebermann - Burchard (triterpenoides y esteroides), Dragendorff (alcaloides), Baljet (lactonas sesquiterpénicas), gelatina - sal (taninos), Rosenheim (antocianinas), Shinoda (flavonoides), Molish (hidrato de carbono) y ninhidrina (aminoácidos libres).23,24
La reactivación de Streptococcus mutans (ATCC 25175) se realizó según el Instituto de Normas Clínicas y de Laboratorio,25 se utilizó el agar Mueller - Hinton (Merck®),26 para obtener colonias bien aisladas se realizó la técnica de siembra por estrías escocesas, se trasladó el cultivo a la incubadora (Memmert®) en posición invertida a 36,5 °C por 24 horas.27 En la preparación del inóculo, se emplearon 7 colonias separadas de la resiembra en agar Mueller - Hinton suplementado con 5 % de sangre de carnero, sembradas con un hisopo estéril y se transfirieron a 5 mL de caldo infusión cerebro corazón (Merck®), a 37 °C por 4 horas hasta lograr una turbidez idónea.10
La estandarización del inóculo se realizó por turbidimetría en espectrofotómetro Thermo Scientific®️ Genesys 10S a 620 nm comparándola con la densidad estándar del tubo 0,5 de la escala McFarland, se obtuvo como resultado una suspensión equivalente a 1,5 x 108 UFC/mL.10,28
El experimento in vitro se realizó en el laboratorio de investigación y desarrollo farmacéutico, se cumplieron de forma estricta las directrices de bioseguridad.28,29 Se emplearon placas de Petri con agar Mueller - Hinton, las cuales fueron elaboradas y homogenizadas con anterioridad según los lineamientos de Merck®.26
Se realizaron 48 siembras y se repartieron en 6 grupos de n= 8 placas, empleando hisopos estériles los cuales se sumieron en los inóculos homogenizados a 0,5 de la escala McFarland.25,27 La siembra se realizó de forma paralela y compacta, se rodeó todo el diámetro del medio de cultivo, se repitió la actividad girando el medio 60 ° 2 veces más y se dejó en reposo por 10 minutos antes de agregar los discos.27,29
Se prepararon discos de papel filtro Whatman N° 3 estériles de 6 mm de diámetro, los cuales fueron distribuidos en los medios de cultivo utilizando una pinza quirúrgica a 15 mm del borde de la placa de Petri,25,29 presionando suave la superficie para favorecer su integración, se colocaron 4 discos por placa. Con anticipación los discos fueron cargados con 30 uL de los extractos hidroalcohólicos de cáscara de Solanum sessiliflorum Dunal, volúmenes que permitieron depositar 7,5 mg de extracto al 25 %; 15 mg de extracto al 50 % y 22,5 mg de extracto al 75 %, se dejaron secar y todo el proceso se llevó a cabo en un ambiente estéril.21,28
Distribución de las siembras en los grupos:
Grupo I: blanco, discos con agua destilada
Grupo II: control negativo, discos con etanol al 70 %
Grupo III: control positivo, discos con clorhexidina al 0,12 %
Grupo IV: experimental 1, discos con extracto de Solanum sessiliflorum Dunal al 25 %.
Grupo V: experimental 2, discos con extracto de Solanum sessiliflorum Dunal al 50 %.
Grupo VI: experimental 3, discos con extracto de Solanum sessiliflorum Dunal al 75 %.
De inmediato, las placas que contenían el medio y los discos se colocaron de manera invertida en una incubadora (Memmert®) a 37 °C por 24 h.29 Posterior al tiempo de incubación, los halos sin crecimiento que se originaron alrededor de los discos se evaluaron como halos de inhibición y se midieron con calibrador Vernier marca Truper.21,29
Para la evaluación de tipo cualitativa se usó la escala de Duraffourd y para la valoración de tipo cuantitativa se manejaron las zonas de los diámetros de los halos de inhibición y el porcentaje del efecto inhibitorio relativo en contraste al control positivo.27
Las medidas de las zonas de inhibición fueron formuladas como promedio aritmético ± SE a un nivel de confianza del 95 % y un error relativo del 5 %; se manejó la prueba de homogeneidad de varianzas de Hartley, Cochran y Bartlett; el ANOVA de una vía y el HSD de Tukey. Se consideró como nivel de significación (p< 0,05), a través del software estadístico IBM SPSS Statistic for Windows versión 25.
El trabajo fue aprobado por el Comité de Ética para la investigación de la Facultad de Ciencias Farmacéuticas y Bioquímica de la Universidad Inca Garcilaso de la Vega con la resolución 841-2019-DFCFB.
RESULTADOS
En el análisis fitoquímico preliminar se detectó la presencia de compuestos fenólicos, antocianinas, quinonas y glicósidos cardiotónicos (tabla 1).
Tabla 1 - Evaluación fitoquímica del extracto hidroalcohólico de Solanum sessiliflorum Dunal
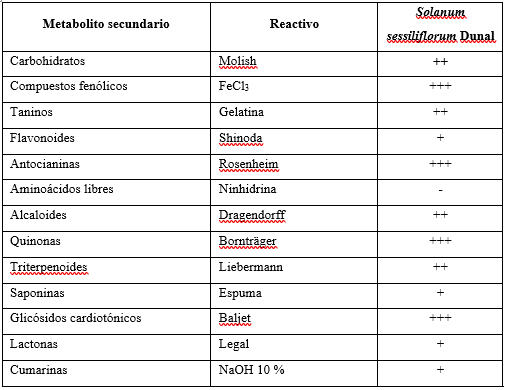
+++ Abundante, ++ Moderado, + Escaso, - No presenta
La información anotada a las 24 horas (tabla 2) muestra que todas las medias se encuentran dentro de los límites establecidos, a un intervalo de confianza del 95 % y un error relativo del 5 %, por ello, ningún dato se excluye.
Tabla 2 - Estadística descriptiva del promedio de los halos de inhibición en milímetros de los grupos de ensayo sobre Streptococcus mutans ATCC 25175
| n | ||||||||
|---|---|---|---|---|---|---|---|---|
| Grupo I | 32 | 0,000 | 0,0000 | 0,0000 | 0,000 | 0,000 | 0,0 | 0,0 |
| Grupo II | 32 | 10,159 | 0,1663 | 0,0294 | 10,099 | 10,219 | 9,8 | 10,5 |
| Grupo III | 32 | 19,956 | 0,2435 | 0,0431 | 19,868 | 20,044 | 19,6 | 20,5 |
| Grupo IV | 32 | 13,653 | 0,4295 | 0,0759 | 13,498 | 13,808 | 12,9 | 14,3 |
| Grupo V | 32 | 16,181 | 0,4138 | 0,0732 | 16,032 | 16,330 | 15,1 | 16,7 |
| Grupo VI | 32 | 19,831 | 0,3126 | 0,0553 | 19,719 | 19,944 | 19,0 | 20,3 |
| Total | 192 | 13,297 | 6,8817 | 0,4966 | 12,317 | 14,276 | 0,0 | 20,5 |
De acuerdo con los valores obtenidos a las 24 horas (tabla 3), el grupo III: control positivo, grupo V: experimental 2 y grupo VI: experimental 3 alcanzaron según la escala Duraffourd, muy sensible = ++ y un efecto antibacteriano alto, según el porcentaje del efecto inhibitorio sobre S. mutans ATCC 25175.
Tabla 3 - Escala de Duraffourd y porcentaje del efecto inhibitorio de los grupos de ensayo sobre S. mutans ATCC 25175
|
|
|
|
|---|---|---|
| Grupo I | - | 0 |
| Grupo II | + | 50,90 |
| Grupo III | ++ | 100 |
| Grupo IV | + | 68,41 |
| Grupo V | ++ | 81,08 |
| Grupo VI | ++ | 99,37 |
*Del promedio de las zonas de inhibición de 32 discos por grupo.
Al efectuar la prueba de homogeneidad de varianzas de Hartley, Cochran y Bartlett, se determinó para Streptococcus mutans ATCC 25175 (p= 0,305), se aprecia que las varianzas son iguales.
En la tabla 4, al realizar el ANOVA de una vía, se determinó p< 0,05, que indica diferencias significativas entre los grupos de ensayo sobre S. mutans ATCC 25175.
Tabla 4 - Anova de un factor de los grupos de ensayo sobre S. mutans ATCC 25175
| F | |||||
|---|---|---|---|---|---|
| Inter - grupos | 9028,565 | 5 | 1805,713 | 20047,759 | 0,000 |
| Intra - grupos | 16,753 | 186 | 0,090 | - | - |
| Total | 9045,318 | 191 | - | - | - |
*De 192 discos por 6 grupos de ensayo.
Al aplicar el post-hoc HSD de Tukey, se determinó que todos los grupos exhiben diferencias estadísticas significativas (p< 0,05), con excepción del grupo III: control positivo con grupo VI: experimental 3 (p= 0,554) que no presentan diferencia significativa.
DISCUSIÓN
En la última década se ha incrementado el estudio de productos naturales que puedan prevenir enfermedades bucodentales, sobre todo para inhibir el sobre crecimiento de Streptococcus mutans, que en conjunto con otros factores pueden desencadenar caries dental.8
Perú es considerado uno de los países con mayor biodiversidad del planeta, la cual se encuentra distribuida en su mayoría en la selva tropical.13,30 La especie Solanum sessiliflorum Dunal, posee un fruto utilizado por la población local en forma de refresco, al efectuar la prueba de solubilidad, se verificó su afinidad en agua y etanol al 70 %.15,17
Se ha descrito el método de extracción y el solvente usado, para la obtención de los constituyentes químicos orgánicos, fundamental para la evaluación del efecto antibacteriano. Al respecto Akanmu y otros,22 refieren que el uso de agua y etanol en el método de maceración son ideales para la extracción de los fitoconstituyentes de las especies vegetales.
Al realizar el análisis fitoquímico preliminar se detectaron abundantes compuestos fenólicos, antocianinas, quinonas, glicósidos cardiotónicos y mediana cantidad de taninos, alcaloides y triterpenoides, responsables en conjunto del efecto antibacteriano. Estos resultados son consistentes con lo declarado por Ramon-Valderrama y otros,14Mascato y otros,15Espinoza y otros,21 y Vargas y otros.30
En el estudio se evaluaron in vitro los extractos hidroalcohólicos de Solanum sessiliflorum Dunal sobre S. mutans ATCC 25175, la técnica utilizada fue de difusión de disco. Al respecto Gallardo-Vásquez y otros,31 señalan que la técnica de Kirby - Bauer es utilizada para evaluar el efecto antibacteriano de cualquier compuesto químico o especie vegetal.
Esta investigación se limitó a evaluar concentraciones de extractos hidroalcohólicos de Solanum sessiliflorum Dunal, al 25 %, 50 % y 75 %, teniendo en cuenta lo reportado por Espinoza y otros.21
Los datos extraídos de las tablas 2 y 3 muestran, que la media de los diámetros de los halos de inhibición aumenta conforme se incrementan las concentraciones del extracto, lo cual demuestra que el extracto hidroalcohólico a diferentes concentraciones tiene un efecto sobre el crecimiento de S. mutans ATCC 25175. Estos resultados son consistentes con lo declarado por Espinoza y otros.21 Asimismo, en todos los grupos los diámetros fueron mayores a las del grupo II: etanol al 70 %, con excepción del grupo I: agua destilada.
Los resultados indican que el extracto de Solanum sessiliflorum Dunal al 75 % no presenta diferencia significativa con respecto al control positivo: clorhexidina al 0,12 %. No obstante, se juzgó como resultado preliminar y es importante plantear la base farmacológica del efecto sobre la cepa en estudio.
Dado al aumento de cepas resistentes a los antimicrobianos,28,31 evidencias de efectos secundarios del flúor y clorhexidina.8,11,12 Las especies vegetales como Solanum sessiliflorum Dunal son una alternativa interesante porque podrían aumentar la eficacia de los tratamientos terapéuticos convencionales.27,28
Se concluye que el extracto hidroalcohólico de Solanum sessiliflorum Dunal al 75 % presenta efecto antibacteriano in vitro sobre cepas de Streptococcus mutans ATCC 25175 con valores similares a clorhexidina al 0,12 %.














