Introducción
Aunque clásicamente el tracto gastrointestinal no ha tenido relevancia clínica en el paciente crítico, en los últimos años esta visión ha cambiado y cada vez se pone más de manifiesto su importancia en el desarrollo de multitud de infecciones nosocomiales y en el fracaso multiorgánico. (1
La digestión y la absorción de nutrientes, el mantenimiento de la perfusión visceral y el papel dentro del sistema inmunitario, mediado fundamentalmente por el tejido linfoide asociado al intestino (del inglés Gut Associated Lymphoid Tissue, GALT) son tres de los aspectos más importantes de este sistema. (2
La alteración de la función gastrointestinal es una situación común en los pacientes críticos: desde el momento del ingreso aparecen alteraciones digestivas que demuestran un fallo del órgano: esta disfunción es subestimada, sin apreciar que el intestino es un protagonista de la respuesta al estrés del paciente crítico.
Estas alteraciones severas en muchas ocasiones son subestimadas por el personal asistencial y no se tiene en cuenta en la evolución del paciente crítico, aspectos que motivan al autor a realizar la revisión del tema.
El presente trabajo tiene como objetivo brindar a los profesionales de la salud las bases teóricas esenciales que sustenten su autopreparación en la entidad clínica fallo intestinal agudo en cuanto a definición, clasificación según su gravedad, alteraciones gastrointestinales en el paciente crítico, implicaciones clínicas, diagnóstico y tratamiento.
Desarrollo
Definición
Fallo intestinal Agudo (FIA):es la reducción de la función intestinal bajo el mínimo necesario para absorción de macronutrientes y/o electrolitos, de tal forma que se requiere suplementación intravenosa para mantener la salud y/o el crecimiento. La reducción de la función intestinal de absorción que no requiere suplementación intravenosa, puede considerarse como insuficiencia o disfunción intestinal. El FGI agudo se convierte así en el motor de la sepsis y del mal curso clínico. Todo este complejo mecanismo aún es poco conocido y abre un campo de estudio en el tratamiento del paciente crítico. (3
El grupo de trabajo de problemas abdominales Working Group on Abdominal Problems (WGAP) de la Sociedad Europea de Medicina Intensiva (European Society of Intensive Care Medicine (ESICM)) propuso la graduación de las alteraciones GI agudas del paciente crítico según su gravedad en 4 tipos. (4
Grado I (riesgo): nauseas postoperatorias o vómitos durante los primeros días post cirugía; ausencia de sonidos intestinales, disminución de motilidad intestinal en la fase precoz del shock.
Grado II (disfunción GI): gastroparesia con aumento del residuo gástrico, parálisis del tracto GI, diarrea, aumento de la presión intraabdominal (PIA) entre 12-15 mm Hg, aparición de sangre en contenido gástrico o en las heces. Existe intolerancia a la NE (se considera si a las 72 horas no se ha podido aportar 20 kcal/kg).
Grado III (fallo intestinal agudo): persistencia de la intolerancia a pesar de intervención terapéutica con residuo gástrico aumentado, parálisis GI, aumento de distensión intestinal, elevación de la PIA (15-20 mm Hg), y presión de perfusión abdominal baja (< 60 mm Hg).
Grado IV (fallo intestinal agudo): isquemia intestinal con necrosis, hemorragia GI, incluso shock hemorrágico, síndrome de Ogilvie, síndrome compartimental abdominal. Pone en peligro la vida de forma inmediata.
Alteraciones gastrointestinales en el paciente crítico
Las alteraciones GI son muy frecuentes en el paciente crítico: desde el 15% en los pacientes quirúrgicos, el 50% en la sepsis, > 60% en pancreatitis y > 80% si existe hipertensión endocraneal: estas alteraciones varían desde disfunción intestinal hasta FGI agudo. (5
Las manifestaciones clínicas son múltiples: intolerancia a la alimentación enteral, vómitos, regurgitación, diarrea, ausencia de ruidos abdominales, aumento del residuo gástrico, hemorragia GI, distensión abdominal, aumento de la presión intraabdominal. Aparecen desde el primer día de ingreso en UCI. 6(Tabla 1)
Alteraciones de la integridad intestinal en el paciente crítico
En el paciente crítico existe una hipoperfusión generalizada, que es mayor en el intestino, llegando a producirse isquemia intestinal, debido a esto, durante la resucitación obligada con fluidos se produce un edema intestinal que causa mayor disfunción intestinal (daño por reperfusión) e incluso la perpetua. Así se producen alteraciones tanto en la función como en la anatomía. Desde el primer momento se produce una alteración de la motilidad gastrointestinal: gastroparesia, disminución de la contractilidad duodenal, relajación del intestino delgado y colon, debido fundamentalmente a alteraciones hormonales del propio tubo digestivo, todo esto favorece la producción de citoquinas, que además de su acción proinflamatoria alteran el peristaltismo normal. El mismo tratamiento de la situación crítica va a favorecer la alteración de la motilidad (ventilación mecánica, sedación, catecolaminas i.v.).7-9
Tabla 1. Alteraciones gastrointestinales en el paciente con fallo intestinal agudo.
| Alteración anatómica | -Atrofia de vellosidad intestinal |
| Peristaltismo | -Paresia gástrica -Alteración peristaltismo intestinal |
| Digestión | -Alteración secreción gástrica y pancreática -Perdida de enzimas del epitelio |
| Absorción | -Insuficiente digestión y absorción por isquemia y edema de la mucosa. -Alteración de la motilidad intestinal |
| Barrera | -Aumento de permeabilidad por isquémica -Translocación bacteriana y de endotoxinas -Alteración absorción agua en el colon |
| Inmunidad | -Reperfusión/isquemia intestinal -Disminución de la producción de IgA -Disminución de la masa del GALT |
| Microbiota | -Disbiosis, aumento de virulencia de gérmenes |
El equilibrio existente entre la luz intestinal y las células intestinales se deteriora: las células intestinales presentan una apoptosis acelerada, las uniones entre las células se rompen, existe una disminución de la proliferación epitelial, y una menor producción de moco, por lo que la capa mucosa se vuelve más delgada, se rompe su integridad pierde su hidrofobicidad, y se hace permeable al paso de toxinas o gérmenes. (10
La afectación y disminución de cierto tipo de bacterias condiciona aumento de otro tipo (disbiosis intestinal), pero, además, bacterias presentes habitualmente en el intestino se pueden hacer virulentas. La pérdida del equilibrio habitual se debe a la misma injuria, pero se ve favorecida por el uso de fármacos (antibióticos, inhibidores de la bomba de protones). (11
Puesto que la microbiota tiene una función estructural en la barrera intestinal, el desequilibrio puede conducir a una respuesta inmune anómala, aumento de la permeabilidad del epitelio intestinal, paso de bacterias o sus toxinas a través del epitelio (translocación bacteriana). (12
La translocación bacteriana está muy discutida, por lo que se han propuesto otros mecanismos:
las bacterias o endotoxinas no serían las responsables directas del SIRS, sino que aumentarían el proceso inflamatorio intestinal, produciéndose citoquinas y otros mediadores que afectarían al sistema inmune, tanto local como sistémico. Así el intestino actúa como un “absceso no drenado”: la disbiosis de la microbiota y el delicado equilibrio de todo el intestino alterado condicionan alteraciones sistémicas, disminución de la inmunidad, situación proinflamatoria, mayor susceptibilidad a infecciones nosocomiales, sepsis y síndrome de fracaso multiorgánico. (13) (Fig. 1)
las bacterias, los restos proteicos de las bacterias muertas, citoquinas, podrían llegar a través de los linfáticos mesentéricos al conducto torácico (linfa tóxica) volcándose posteriormente a la circulación sistémica, activando los macrófagos alveolares en el pulmón, contribuyendo al SIRS y FMO. Se ha postulado también que las enzimas pancreáticas pueden atravesar los canales intestinales del epitelio intestinal dañado, dando lugar a una linfa tóxica que pueden propagar la lesión a sitios distantes y así contribuir al FMO. (14
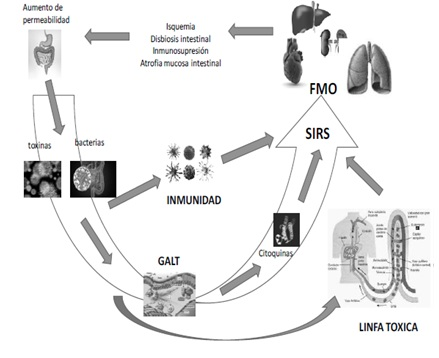
Fig. 1. Etiopatogenia del síndrome de respuesta inflamatoria sistémica y fallo multiorgánico en el fallo intestinal agudo.
Implicaciones clínicas de la disfunción gastrointestinal
Hay dos principales efectos clínicos, sobre la nutrición y sobre el riesgo de infección.
Nutrición: la alteración GI impide la administración de NE. Incluso en aquellos pacientes que pueden tolerarla, esta reporta solo 40-60% de los requerimientos nutricionales (35% de los pacientes de UCI). La paresia GI, y, por otro lado, la disbiosis intestinal que se produce con la consiguiente diarrea contribuye a la imposibilidad de nutrir correctamente al paciente. (15
Consecuencias infecciosas: La disminución de la motilidad GI altera la eliminación del contenido, existiendo una exposición prolongada a la microbioma, ya alterada por otros factores, especialmente por la medicación. Esto junto al aumento de permeabilidad de la barrera intestinal condiciona el paso de las bacterias, o sus productos tóxicos. Además la exacerbación de la respuesta inmune sistémica puede predisponer a sepsis y neumonía asociada a ventilación mecánica. Se ha demostrado que una disbiosis intestinal se asocia con complicaciones sépticas y mayor mortalidad en pacientes con SIRS.16
Diagnóstico de fallo intestinal agudo
El diagnóstico mediante los síntomas y signos no permite conocer la gravedad del cuadro clínico. Se han propuesto distintos marcadores y test para evaluar la pérdida de integridad de la barrera intestinal, entre ellos la medida del D-lactato en sangre (producto de fermentación de muchas bacterias del tracto gastrointestinal). (17
También se utilizan los biomarcadores derivados del daño de los enterocitos: Citrulina, amino ácido derivado de la glutamina, que es sintetizado principalmente en los enterocitos de intestino delgado y el ácido graso intestinal unido a proteína, (intestinal fatty acid-binding protein: I-FABP) producto de la necrosis del enterocito. Cuando existe una necrosis del enterocito, se produce una elevación de la I-FABP plasmática o urinaria. Su elevación es reflejo directo de la gravedad del daño de la mucosa intestinal. También es útil el ácido graso hepático unido a proteína (liver fatty acid binding protein (L-FABP). (18
Se ha propuesto la ultrasonografía intestinal para la valoración del fallo intestinal, siguiendo un protocolo, para valorar la anatomía y la función intestinal mediante medidas de luz intestinal, la pared, estructuras circundantes intestinal y gástrica peristalsis y flujo sanguíneo). Según la suma de cada una de las alteraciones se podrá correlacionar con los grados de disfunción/fallo intestinal agudo propuestos por el grupo ESICM. (19,20
Tratamiento del FGI agudo en paciente crítico
Recientemente se publicó un documento de recomendaciones de tratamiento en el que consideran el FGI Agudo como una entidad exclusiva.21 El tratamiento a seguir contempla varios puntos:
Resucitación precoz: corregir la acidosis y anormalidades electrolíticas, manteniendo una perfusión adecuada sin sobrecarga hídrica: manteniendo una presión de perfusión abdominal superior a 50 mm Hg.
Estricto control glucémico: además del mejor control metabólico, mejora la motilidad intestinal.
Tratamiento de la dismotilidad intestinal: se debe minimizar la medicación que altere la función intestinal; pero muchas veces es imposible pues los sedantes (Midazolam, Propofol), analgésicos (opioides, ketamina) y las catecolaminas, son obligados en el tratamiento. Los procinéticos como metoclopramida (10 mg iv) o domperidona (30-40 mg) actúan fundamentalmente sobre el tracto GI superior. La eritromicina, (100 mg iv c/8 horas durante 3 días), agonista de la motilina, más efectiva por vía iv que por vía oral, favorece el vaciado gástrico y actúa sobre la motilidad del tubo digestivo. Incluso se ha mostrado que la eritromicina es más eficaz que la metoclopramida para la mejoría de la motilidad intestinal. Otras drogas procinéticas (naloxona, neostigmina) no son útiles por sus efectos secundarios. (22,23
Control de sepsis: si existe foco quirúrgico tratable, la cirugía es la acción inmediata. Si no se existe foco séptico y la causa inicial del FGI es la situación del paciente crítico, la sepsis puede ser causada por translocación bacteriana y se debe sospechar el abdomen como fuente de sepsis (“absceso no drenado”). Se deben seguir las guías preconizadas por el grupo internacional “Surviving Sepsis Campaing” (cultivos precoces, antibioterapia empírica precoz y cambio de la misma tras resultado del cultivo). (24
Soporte nutricional (SN): se debe realizar un SN para intentar aminorar los efectos del catabolismo aumentado y evitar la malnutrición. Se recomienda iniciarlo en las primeras 24-48 horas, una vez el paciente esté hemodinámicamente estable. Las guías actuales de nutrición recomiendan siempre nutrición enteral (NE) precoz, y posponer la nutrición parenteral (NP) varios días (incluso hasta 7 días post ingreso), salvo que el paciente esté malnutrido:25
Nutrición parenteral (NP): aunque la NE precoz ha demostrado ser la solución más beneficiosa para el paciente crítico, el paciente con FGI agudo grave presenta una intolerancia total a la NE. Por esta razón, se plantea la NP como alternativa. Según las últimas recomendaciones internacionales, se podría esperar hasta 1 semana después del ingreso para iniciarla, salvo que el paciente esté malnutrido o con alto riesgo nutricional. (25
Nutrición enteral: el FGI imposibilita el uso de NE precoz; se intentará aportar lo antes que se pueda, incluso en pequeñas cantidades. Aparte del aporte nutricional que significa, la NE tiene otros efectos (tróficos sobre las células epiteliales, mantenimiento de la integridad de la mucosa GI, aumento de la masa del tejido GALT (Gut-Associated Lymphoid Tissue) y de la producción de Ig A,), amén de su acción sobre la flora intestinal, reduciendo la virulencia de los organismos patógenos. Además, aumenta la función inmune, promueve la sensibilidad a la insulina al estimular las incretinas, controla mejor la hiperglucemia y atenúa el stress metabólico al utilizar un sistema más fisiológico que la NP. (26
Estrategias sobre la Microbiota: el tratamiento de la disbacteriosis es uno de los objetivos actuales en estudio. Las posibilidades terapéuticas son descontaminación intestinal, lavado intestinal, secuestro intraluminal de endotoxinas, trasplante fecal y empleo de probióticos. (27
Descontaminación intestinal selectiva: el objetivo es disminuir las bacterias patogénicas de la orofaringe e intestinales; comprenden pautas cortas de AB parenterales, más AB no absorbibles vía enteral y pastas de gel de la misma composición aplicadas en la orofaringe, Su uso ha demostrado disminución de infecciones respiratorias, de bacteriemias y del número de pacientes con FMO. (28
Lavado intestinal: puesto que existe una alteración de la barrera intestinal, el lavado intestinal a través de una sonda yeyunal con una solución de poli etilenglicol puede reducir el número de bacterias y las toxinas proinflamatorias de la luz intestinal. (29
Trasplante fecal: existe un gran interés por el trasplante de materia fecal de donante sano para mejora la microbiota. Se ha comprobado que el aporte de materia fecal es tres veces más eficaz que el tratamiento convencional en la infección por Clostridium difficile. (30,31
Secuestro intraluminal de endotoxinas: diferentes experiencias demuestran que la infusión luminal de sustancias con capacidad de unirse a las endotoxinas e inhibir su absorción, como es el caso de la colesteramina o la polimixina B, disminuyen los efectos deletéreos locales y sistémicos en el FGI. (32
Probióticos: son microorganismos no patógenos que han demostrado efectos beneficiosos en la prevención y tratamiento de enfermedades graves. Puesto que existe una disbiosis grave en el FGI agudo, la restauración de la microbiota mediante el aporte de probióticos (generalmente miembros del genero lactobacilus, biofidobacterium y otros), podrá conseguir efectos beneficiosos los probióticos producen bacteriocinas que inhiben gérmenes patógenos, estimulan la producción de mucina, disminuyen la afectación. (30
Conclusiones
Los síntomas del FGI son muy variados y muchas veces no se puede determinar la gravedad de la situación, reconocerlo es fundamental, pues la enfermedad crítica altera la motilidad intestinal y la integridad del intestino: se altera la permeabilidad, se afecta el moco de la mucosa, aumenta la apoptosis del epitelio y disminuye la proliferación del mismo. Se rompe así la barrera intestinal; la microbiota intestinal alterada o sus toxinas pueden atravesar esta barrera, afectando el GALT, creando una disfunción inmune que puede alterar de forma sistémica al resto de los órganos, produciéndose un síndrome de respuesta inflamatoria, sepsis, shock séptico y FMO. Los test actuales para la evaluación de la disfunción GI son de valor limitado y precisamos encontrar nuevos marcadores fiables. Es fundamental reconocer la situación precozmente, y conseguir estrategias profilácticas. Actualmente no existe un tratamiento bien conocido dirigido al intestino, salvo el uso de la nutrición enteral, (que muchas veces es imposible por gran intolerancia), y los procinéticos.














