INTRODUCCIÓN
Los tumores del estroma gastrointestinal (GIST, por sus siglas del inglés) son raros.1,2,3 Este término se utilizó por vez primera en 1983, Mazur y Clark lo emplearon para designar unos tumores no epiteliales del tubo digestivo que carecían de rasgos ultraestructurales de músculo liso y características inmunohistoquímicas de célula de Schwann.4 Los GIST pueden ser el resultado de mutaciones de proto-oncogenes c-Kit o del receptor alfa polipeptídico del factor de crecimiento derivado de plaquetas, lo que aumenta la actividad de receptor tirosina kinasa y lleva a una proliferación descontrolada de células madre que se derivarían a células de Cajal. Desde 1998 se conoce que estos tumores se originan a partir de las células intersticiales de Ramón y Cajal, ubicadas en los plexos mientéricos de la pared gastrointestinal.2
En el 90% de los pacientes esta enfermedad está relacionada con una mutación en el gen del receptor denominada Kit -es un receptor tirosina cinasa tipo III (4q11-12)-. El receptor Kit está implicado en la regulación de la proliferación célular. Por consiguiente, una mutación que se produce en el gen del receptor KIT puede provocar que la célula se transforme en una célula maligna y una proliferación incontrolada.4
Los GIST representan del 0,1 al 3% de todas las neoplasias primarias gástricas. Su incidencia mundial al año es, aproximadamente, de 15 por un millón de habitantes,5 aunque varía entre 10 y 20 casos por un millón de habitantes en países desarrollados; entre el 20 y 45% son malignos.2 Debido a que los GIST se originan de las células antes mencionadas, ubicadas en los plexos mientéricos de la pared gastrointestinal, pueden localizarse en cualquier localización del tubo digestivo desde el esófago hasta el ano; sin embargo, el estómago (39 a 60%) y el intestino delgado (30 a 42%) son los sitios más frecuentes de localización de estos tumores.2,6 Las ubicaciones más raras del GIST son el colon, el recto, el apéndice, el esófago, el mesenterio, el retroperitoneo y otros órganos.2 El síntoma más frecuente es el dolor abdominal, leve al inicio, pero que empeora a lo largo de meses o años. Es bastante común la aparición de anemia debido a pequeñas pérdidas de sangre continuadas en el tiempo, también lo son la sensación de protuberancias abdominales, el sangrado masivo del tracto digestivo o su oclusión interna en el caso de tumores más voluminosos,4 aunque la obstrucción intestinal es rara debido a que el crecimiento tumoral no es concéntrico. Entre el 20 y el 30% son asintomáticos y su diagnóstico es incidental,1 por lo que para llevar a cabo el diagnóstico se requiere un alto índice de sospecha y recurrir a diferentes procedimientos:5 la endoscopia digestiva con biopsia aporta gran cantidad de datos, lo mismo la ultrasonografía endoscópica, los estudios contrastados del tracto gastrointestinal superior muestran el defecto de lleno en la pared gástrica y la tomografía axial computadorizada (TAC) permite visualizar el tumor exofítico que se origina en la pared del estómago y en otras partes del tubo digestivo, que está bien delimitado y puede presentar hemorragia, necrosis o componente quístico.7
El diagnóstico definitivo se hace por medio de la inmunohistoquímica, mediante la expresión del CD 117, que es positivo en el 95% de los casos. Su comportamiento es distinto al de los carcinomas. Las metástasis se desarrollan comúnmente en el hígado y el peritoneo, pero son extremadamente raras en nódulos linfáticos regionales; generalmente muestran un crecimiento extraluminal y raramente a la cavidad abdominal. Aún cuando su comportamiento sea maligno, tiene tendencia al desplazamiento de órganos adyacentes y no a la infiltración.5
La intervención quirúrgica es el tratamiento para los GIST primarios, es la estrategia terapéutica que puede ofrecer una cura permanente del tumor. La resección completa, evitando la ruptura y el daño de la pseudocápsula tumoral, es el tratamiento inicial para el GIST primario localizado cuando el riesgo de mortalidad y morbilidad como consecuencia de la operación son aceptables. El objetivo de la intervención quirúrgica es la resección completa del tumor, con márgenes macroscópicos y microscópicos negativos, y la preservación de la funcionalidad cuando sea aplicable.8
Las técnicas de mínimo acceso muestran una alternativa muy favorable para el tratamiento de estos tumores.5 El tratamiento de elección es la resección quirúrgica completa por el método laparoscópico, que muestra alternativas muy favorables,5,7 o por vía laparotómica. Existe riesgo de recurrencia del tumor después de la operación, por una resección quirúrgica deficiente, o por patrones genéticos encargados de la reaparición de la enfermedad.7
Los criterios de Fletcher clasifican a los GIST según el riesgo de malignidad por el tamaño y el índice mitótico.8 El pronóstico de los GIST presenta cierta asociación con la localización anatómica y la presencia de metástasis.9 Otros autores refieren que la localización extragástrica, la presencia de necrosis tumoral, el tipo histológico diferente al fusocelular, la ausencia de marcadores inmunohistoquímicos como CD 117 y CD 34 y la expresión de diferentes reguladores del ciclo celular son más frecuentes en tumores con comportamiento maligno.2
En una búsqueda realizada en Cochrane con las palabras clave gastrointestinal stromal tumors, tumores del estroma gastrointestinal y tumores de estroma gastrointestinal se encontraron cinco pacientes informados con tumor del estroma gastrointestinal en Cuba desde 2015 hasta 2018. Esta es una enfermedad nosológica que apenas hace 20 años que comienza a dilucidarse. Si bien es cierto que se han logrado avances relacionados con el diagnóstico, el manejo y el pronóstico de estos tumores aún es un tema en discusión para los Especialistas en Cirugía, en Oncología, en Gastroenterología y en Anatomía Patológica porque los estudios de seguimiento respecto al pronóstico, que se encuentran aún en curso y de los que se esperan sus resultados para decidir qué conductas diagnósticas y terapéuticas son las más beneficiosas así lo demuestran. Por tales motivos se hace necesario presentar las particularidades del siguiente paciente.
INFORMACIÓN DEL PACIENTE
Paciente masculino de 76 años de edad, con antecedentes de hipertensión arterial esencial hace 40 años y fibrilación auricular desde hace un año, ambas controladas con tratamiento médico. Ha tenido ingresos previos por sangrados digestivos altos en forma de melena. En esta ocasión acudió a la Consulta de Cirugía gastroduodenal del Hospital Universitario Clínico Quirúrgico “Arnaldo Milián Castro” de la Ciudad de Santa Clara, Provincia de Villa Clara, por presentar dolor abdominal en hipocondrio izquierdo. Al examen físico se constató una masa palpable, fija, de gran tamaño, dolorosa a la palpación, en la región abdominal antes mencionada. Por ese motivo se decidió su ingreso.
Se le realizaron los siguientes exámenes complementarios:
Hematocrito: 0,35vol%
Leucograma total: 7x109/l
Polimorfonucleares: 0,66
Linfocitos: 0,34
Tiempo de sangramiento: 1xminuto
Tiempo de coagulación: 8xminutos
Conteo de plaquetas: 196x109g/l
INR: 1,42
Tiempo de protrombina: control 13 segundos, paciente 17 segundos
Tiempo de tromboplastina parcial activado con kaolín: control 26 segundos, paciente 26 segundos
Ultrasonido abdominal: imagen quística polilobulada que mide 18x18 centímetros (cm) que puede estar en relación con la glándula suprarrenal izquierda o el paquete de adenopatía retroperitoneales.
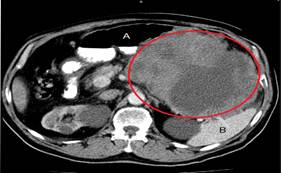
TAC de abdomen preoperatoria: se observa una gruesa imagen de aspecto tumoral a nivel del hemiabdomen izquierdo, posterior al estómago y en íntimo contacto con la curvatura mayor, que desplaza el estómago hacia la derecha, mide 13,7cmx16,8cm, en contacto con el bazo (Figura 1).
Con el cuadro clínico descrito se planificó para Cirugía electiva con diagnóstico de tumor gástrico.
Se le realizó una laparotomía exploradora y se constató una gran masa tumoral que se proyectaba en la cara posterior del estómago, con aparente infiltración esplénica. Se abrió la transcavidad de los epiplones y se dejó ver la masa tumoral, polilobulada, en la cara posterior del estómago hacia la curvatura mayor. Se procedió a su disección cuidadosa (Figura 2), se liberaron todas las estructuras y se realizó la resección de la tumoración con márgenes oncológicas más esplenectomía por encontrar ganglios y aparente infiltración tumoral (Figura 3). El resto de la cavidad sin alteraciones.
Se recibió el resultado histológico: tumor del estroma gastrointestinal tipo GIST con patrón de sarcoma fusocelular, con áreas de hemorragia y necrosis, talla tumoral de 19,5cmx16cmx15cm. Conteo mitótico 5/50HPF (high power field, HPF por sus siglas en inglés, que significan figuras mitóticas por 50 campos de alta potencia).
El resultado de la inmunohistoquímica reveló: tumor fusocelular tipo GIST, CD 117 positivo, CD 34 positivo, alfa actina positivo débil, KI 167 positivo en más del 20%.
Durante el postoperatorio se realizó una TAC que informó paredes gástricas engrosadas, con ausencia quirúrgica de la lesión (Figura 4). Al mes el paciente se encontraba bajo tratamiento médico con mesilato de imatinib y su evolución era favorable.
DISCUSIÓN
La edad de este paciente (76 años) es similar, en la mayoría de los casos, a la de los que aparecen en la Tabla 1. Fernández Tamayo1 informa que el desarrollo típico de estos tumores es en individuos con más de 40 años de edad, con un promedio de edad entre los 55 y los 65 años. Otros autores hacen referencia a la incidencia máxima entre la cuarta y la sexta décadas de la vida.9 A juicio de los autores del presente trabajo la mayoría de los investigadores informan rangos similares de edad en los que es más frecuente el GIST. La Tabla 1 muestra un amplio predominio de pacientes masculinos, lo que concuerda con este paciente. Otros trabajos afirman que no hay diferencias significativas en lo referente a la frecuencia entre los hombres y las mujeres, aunque se ve ligeramente más a menudo en estas últimas;1 otra investigación informa igual proporción para ambos sexos.9
Tabla 1 Revisión en la literatura de pacientes con tumor del estroma gastrointestinal

F: femenino; M: masculino
El tamaño del tumor es un aspecto importante: una dimensión mayor de cinco centímetros es considerada como uno de los factores pronósticos que definen malignidad. Los tumores muy grandes son más complejos debido a la necrosis, la hemorragia o los cambios degenerativos que presentan.1 El tamaño debe ser analizado junto a otros factores como el recuento mitótico y nunca debe verse por separado. Un estudio de 30 pacientes con diagnóstico de GIST intervenidos entre 1999 y 2010 mostró el recuento mitótico y el tamaño tumoral como los principales factores pronósticos identificados relacionados con la progresión de la enfermedad y la supervivencia; en ocasiones resultó difícil de predecir su comportamiento biológico (benigno/maligno), razón por la que las principales clasificaciones vigentes recomiendan catalogarlos de acuerdo al riesgo asociado a metástasis y supervivencia a partir de varios grupos pronósticos, hecho que demuestra el variable comportamiento de esta neoplasia y lo complejo que resulta tratar de definir si estos tumores presentan un comportamiento benigno, incierto (borderline) o maligno.10 El de este paciente y el del informado por Pérez Tauriaux y colaboradores11 son los dos tumores más grandes que aparecen en la Tabla; no se constataron evidencias de lesiones metastásicas a pesar de tratarse de un gran tumor. A más de 20 años del postulado de Kindblom acerca de los GIST y a pesar de los avances en su conocimiento lo anterior demuestra que queda mucho por dilucidar todavía sobre esta enfermedad nosológica, que es un reto para los Especialistas en Cirugía, en Gastroenterología y en Anatomía Patológica.
El estómago es el sitio más común para el desarrollo de los GIST.2,5,11 El pronóstico presenta cierta asociación con la localización anatómica, la localización en el duodeno es la más compleja para el tratamiento de estos tumores.9 En el presente paciente, al igual que en la mayoría de los que aparecen en la Tabla 1, se localizó en el estómago. El tipo histológico diferente al fusocelular es más frecuente en tumores con comportamiento maligno.2 De los pacientes que aparecen en la Tabla 1 tres presentaron un tumor fusocelular tipo GIST: uno epiteloide, en otro estaban presentes las tres morfologías y en un caso no se obtuvo el dato. El índice mitótico de estos pacientes osciló entre uno y 5/50HPF; el del presente fue el más elevado (5/50HPF). Los criterios de Fletcher clasifican a los tumores del estroma gastrointestinal según el riesgo de malignidad y tienen en consideración el tamaño y el índice mitótico.2,8 En este paciente, por presentar un tamaño mayor de 10cm y un índice mitótico =5/50HPF, es considerado como alto potencial de comportamiento agresivo. Solo un paciente presentó lesiones metastásicas. Los GIST con comportamiento maligno pueden dar metástasis al hígado y al peritoneo.9 El paciente informado por Pérez Tauriaux y colaboradores11 tenía un gran tumor con índice mitótico bajo y lesiones metastásicas; en este paciente se trata de un tumor grande, con índice mitótico de 5/50HPF, en el que no se encontraron lesiones metastásicas.
A pesar de ser los GIST una enfermedad poco frecuente son un reto para los Especialistas en Cirugía, en Oncología, en Gastroenterología y en Anatomía Patológica. Hay un campo abierto para la investigación relacionado con el pronóstico asociado a comportamiento maligno. Se presenta uno de los GIST de mayor tamaño e índice mitótico que aparece en la literatura revisada. Este trabajo revela la necesidad de un temprano reconocimiento y la realización de adecuadas investigaciones en pacientes con síntomas gastrointestinales.