INTRODUCCIÓN
La gastroparesia diabética es un síndrome caracterizado por retraso en el vaciado gástrico y síntomas gastrointestinales superiores que sugieren obstrucción de la salida gástrica, sin embargo, no están asociados. La prevalencia es mayor en mujeres que en hombres. El riesgo de presentarla es mayor en diabetes tipo 1 que en el tipo 2 con una relación 4 a 1, sin embargo, los pacientes con diabetes tipo 2 tienen síntomas más graves; generalmente ocurre 10 años después del inicio de la diabetes y en paralelo con otras formas de enfermedad microvascular diabética, que incluyen neuropatía y retinopatía, etc. 1
Es una de las complicaciones más comunes, por lo que casi una cuarta parte de esta población diabética describe síntomas gastrointestinales que se manifiestan especialmente en aquellos que evolucionan con un control glucémico inadecuado o con otras complicaciones al mismo tiempo. 2 La fisiopatología de la gastroparesia no se comprende bien, pero de las diversas causas de gastroparesia, la diabetes es la que mejor se comprende. En la gastroparesia diabética, los posibles mecanismos incluyen la denervación del nervio vago, la pérdida de óxido nítrico sintasa en los nervios entéricos, la pérdida de los ICC y la falta de expresión de óxido nítrico neuronal. 3
Los síntomas cardinales incluyen: saciedad temprana, plenitud posprandial, náuseas, vómitos, distensión, dolor abdominal y pérdida de peso, los síntomas graves provocan un control glucémico deficiente y desnutrición y aumentan el riesgo de hipoglucemia.
El diagnóstico se establece cuando se documenta vaciamiento tardío y se excluye la obstrucción de la salida gástrica mediante estudios de gabinete como son la endoscopia o la tomografía axial computarizada (TAC). La prueba diagnóstica estándar es la gammagrafía. El manejo se guía por la severidad de los síntomas y el estado nutricional. 1,2
La mayoría de los pacientes suelen presentar una enfermedad leve a moderada, y por tanto, responden a las recomendaciones nutricionales, modificaciones dietéticas y control glucémico adecuado, así como procinéticos o medicamentos antieméticos, ambas clases de fármacos a menudo se utilizan solos o en combinación con eficacia variable, si no hay respuesta a las medidas iniciales. Un pequeño porcentaje de pacientes tiene enfermedad grave caracterizada por tolerancia oral inadecuada, desnutrición crónica, pérdida de peso y hospitalizaciones frecuentes. 2
La gastroparesia es un trastorno funcional, que impacta en la calidad de vida, ocurre con más frecuencia en pacientes de sexo femenino, pero con afección considerable a pacientes del sexo masculino.
Se presenta el caso de un paciente que, tras el descarte dirigido e intencional de patología obstructiva como sospecha inicial ante el cuadro presentado, se realiza diagnóstico de gastroparesia diabética severa. Se describen hallazgos del abordaje diagnóstico implementado en este caso y se realiza revisión de la literatura. Es importante la presentación de este caso porque resulta sumamente imprescindible describir las herramientas diagnósticas a implementar para realizar un diagnóstico confirmatorio oportuno de este padecimiento.
PRESENTACIÓN DEL CASO
Se presenta el caso de un paciente de sexo masculino, de 75 años de edad, con antecedentes de diabetes tipo 2 de 30 años de evolución e hipertensión arterial de 30 años de evolución, con múltiples internamientos previos por descontrol metabólico. Este paciente acudió al Instituto Mexicano del Seguro Social de la Ciudad de México por padecimiento de dos meses de evolución caracterizado por intolerancia a la vía oral, náuseas y emesis posprandial, diarrea subaguda y consecuentemente pérdida de peso a razón de 20 kg aproximadamente.
A su ingreso se presentaron evacuaciones disminuidas en consistencia según la escala de Bristol, tipo 6, acompañadas de dolor abdominal, náuseas y emesis de contenido gastroalimentario e incontinencia fecal, asimismo, deterioro del estado de alerta, con recuperación espontánea tras 2 minutos.
A su llegada a la institución el paciente tenía presión arterial de 61/41 mmHg, frecuencia cardiaca 97 latidos por minuto, temperatura 36.5ºC, desorientado, con palidez y mucosa oral seca, el abdomen se encontraba doloroso a la palpación en epigastrio y mesogastrio, distensión abdominal, timpanismo a la percusión en epigastrio y peristalsis disminuida.
El resto del examen físico no mostró alteraciones. Ante la sospecha inicial urgente de desequilibrio hidroelectrolítico y descompensación metabólica secundaria se solicitaron los siguientes exámenes de laboratorio iniciales:
Química sanguínea:
Glucosa: 359 mg/dl.
Urea: 28 mg/dl.
Nitrógeno ureico en la sangre (BUN) (por sus siglas en inglés): 13 mg/dl.
Creatinina: 0,7 mg/dl.
Sodio: 129 mmol/L.
Potasio: 2,75 mmol/L.
Cloro: 80 mmol/L.
Biometría hemática completa:
Se inició tratamiento para corrección del desequilibrio hidroelectrolítico y alteraciones metabólicas presentadas, así como, protocolo de abordaje diagnóstico de síndrome constitucional secundario a intolerancia a la vía oral.
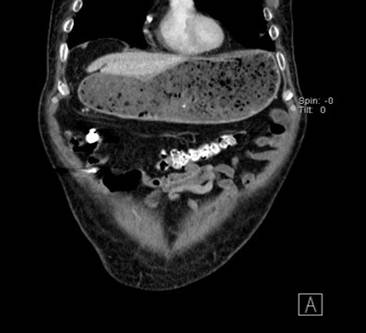
De forma inicial, se realizó búsqueda intencionada de patología quirúrgica abdominal por lo que se solicitó la realización de tomografía abdominal contrastada, que reportó estómago a máxima repleción de contenido gastro-alimentario, unión gastroduodenal con engrosamiento circunscrito de su pared y aumento del diámetro de la primera y segunda porción del duodeno. (Fig. 1).
Por los resultados mostrados se decidió realizar endoscopia de tubo digestivo alto donde se documentó la presencia de una gastritis no erosiva, esofagitis grado D, según la Clasificación de los Ángeles, sin patología obstructiva demostrada hasta este nivel, sin embargo, presentó eventualidad durante el procedimiento, relacionado con hipotensión de 50/40 mmHg y bradicardia de 38 latidos por minuto por lo que se interrumpió la realización del procedimiento y la toma de muestras para biopsia. Se inició reanimación hídrica con soluciones cristaloides con adecuada respuesta y se reprogramó el estudio de endoscopia. En la nueva endoscopia se procedió a la toma de muestra para la biopsia de unión gastroduodenal, pero no se pudo realizar valoración adecuada porque presentaba abundantes restos de alimentos que impedían una adecuada visualización. (Fig. 2).

Fig. 2 Endoscopia de tubo digestivo alto. No fue valorable por la presencia de abundantes restos de alimentos
Ante lo anterior se indicó ayuno, se colocó sonda nasogástrica a derivación y se realizó lavado gástrico y se obtuvieron 1500 ml de líquido gastro-biliar de olor fétido.
Posterior al lavado se repitió por tercera vez estudio de endoscopia y se obtuvo biopsia de píloro sin demostrar nuevamente patología obstructiva. La biopsia solo manifestó cambios crónicos inflamatorios y sin evidencia de hiperplasia pilórica, células malignas, reducción de innervación o algún otro hallazgo distinto.
Durante su evolución persistieron las náuseas para llegar hasta la emesis en múltiples ocasiones, así como, mayor distensión abdominal y aumento de dolor a la palpación, por lo que se inició manejo con procinéticos, para luego presentar mejoría parcial. Se descartó entonces, patología quirúrgica abdominal, y ante la sospecha de gastroparesia por la ausencia de etiología obstructiva que explicara las manifestaciones clínicas, en asociación al antecedente de diabetes tipo 2 de larga evolución, se realizó gammagrafía de vaciamiento gástrico donde se reportó retención de alimentos sólidos radiomarcados de más del 35 % al cabo de 4 horas. (Fig. 3).

Fig. 3 Gammagrafía de vaciamiento gástrico. Se observó retención de alimentos sólidos radiomarcados y no radiomarcados de más del 35 % al cabo de 4 horas
Se concluyó como diagnóstico, gastroparesia severa de etiología diabética, para lo que se inició manejo con doble procinético, sin embargo, no presentó respuesta favorable al tratamiento por lo que se envió al paciente a la Atención Terciaria para valorar inicio de protocolo quirúrgico.
DISCUSIÓN
La gastroparesia es un trastorno crónico generalmente asociado con diabetes complicada de larga duración y caracterizado por retraso en el vaciamiento gástrico (GE) (por sus siglas en inglés) en ausencia de obstrucción mecánica.1
Los síntomas de la gastroparesia incluyen: náuseas, vómitos, saciedad temprana, plenitud posprandial, distensión abdominal, eructos y molestias en la parte superior del abdomen. 2)
El diagnóstico de gastroparesia se puede realizar sobre la base de la historia clínica, excluyendo obstrucción de la salida gástrica o gastrointestinal (GI) mediante auxiliares diagnósticos como la endoscopia de vías digestivas altas y/o estudios imagenológicos de la vía digestiva alta. Se puede realizar una serie gastrointestinal alta con bario, sin embargo, no es un método sensible para diagnosticar gastroparesia, no obstante, puede sugerir retención gástrica por falta de vaciamiento de bario, o muy poco, a los 30 minutos y la retención de bario a las 6 horas sugieren gastroparesia; su valor se basa en la exclusión de lesiones en la mucosa y de obstrucción mecánica de la desembocadura gástrica.
La tomografía axial computarizada con medio de contraste intravenoso u oral mejora la sensibilidad para excluir estenosis pilórica, neoplasia o enfermedad ulcerosa activa en el antro, píloro o duodeno, sin embargo, la endoscopia es más sensible en la detección de lesiones de la mucosa, algunos pacientes con GE tardío pueden retener alimentos en el estómago después de un ayuno nocturno relacionado con el tipo de alimento ingerido o el uso de medicamentos que pueden retrasar el GE. 3
Una vez que se excluye una afección mecánica, se determina el índice de vaciamiento gástrico mediante gammagrafía de vaciamiento gástrico. 4 Este procedimiento está considerado como el más adecuado porque cuantifica el vaciamiento de una comida en fase sólida. En algunos centros se estandarizó el uso de un emparedado de huevo marcado con coloide de sulfuro y tecnecio 99 (99mTc) como comida de prueba, los datos muestran que las imágenes hasta 4 horas después del consumo de comida detectan más pacientes con vaciamiento gástrico retrasado que las imágenes de más de 90 o 120 minutos, se pueden realizar mediciones cada hora durante hasta 4 horas, porque proporciona un parámetro que evalúa el vaciado gástrico general; además, la interpolación lineal entre los porcentajes vaciados entre 1 y 4 horas permite estimar tiempo medio de vaciamiento gástrico.
Se puede definir GE retrasado como >60 % de retención a las 2 horas y/o 10 % a las 4 horas y GE tardío de moderado a grave como >20 % de retención a las 4 horas. Se deben tener en cuenta los posibles efectos de la glucemia sobre el vaciado gástrico, se recomienda que la glucemia sea inferior a 180 mg/dl en ayuno antes de iniciar la prueba de vaciamiento gástrico. La prueba del aliento de vaciamiento gástrico incorpora un isótopo estable, 13 C, en un sustrato como el ácido octanoico o la espirulina platensis (alga azul-verde). Este es un método no invasivo fácil de realizar, con un costo similar al de la gammagrafía y no implica exponer a los pacientes a una radiación ionizante. Se realiza durante un período de 4 horas después de un ayuno de 8 horas, recolectando muestras de aliento antes de las comidas, después se administra una comida de prueba especial y después de consumir la comida, se recolectan muestras adicionales (generalmente cada 30 minutos) en momentos específicos. Esta prueba tiene una sensibilidad del 89 % y una especificidad del 80 % para identificar el GE tardío, sin embargo, se deben validar los resultados en pacientes con enfisema, cirrosis, enfermedad celíaca o insuficiencia pancreática, ya que en estos pacientes el metabolismo del octanato puede estar alterado. 5 La cápsula de motor inalámbrico (WMC) sirve para la evaluación del vaciado gástrico y el tránsito colónico en pacientes con sospecha de estreñimiento de tránsito lento. Una vez ingerido, el WMC mide el pH, la temperatura y la presión en todo el tracto gastrointestinal (GI), con una sensibilidad de 65 % y especificidad del 87 %. 6
La mayoría de los pacientes suelen presentar una enfermedad de leve a moderada y un pequeño porcentaje de pacientes tiene enfermedad grave caracterizada por tolerancia oral inadecuada, desnutrición crónica, pérdida de peso y hospitalizaciones frecuentes. 2 Para estos pacientes, se han propuesto otras modalidades de tratamiento como son: la miotomía endoscópica gástrica peroral (G-POEM) y la estimulación eléctrica gástrica. A pesar de las diversas terapias, estas a menudo son difíciles de lograr y las manifestaciones siguen reapareciendo. Esto se debe principalmente al mal control glucémico, agravado por complicaciones como la deshidratación, el desequilibrio electrolítico y la desnutrición.7 Otros factores de riesgo y condiciones asociadas son las infecciones concomitantes, el antecedente de colecistectomía y la neuropatía autonómica. 7 Además, la mayor edad en el momento del diagnóstico se asoció con una peor supervivencia y se ha observado que los pacientes con gastroparesia no diabética tienen una mejor tasa de supervivencia que los pacientes con gastroparesia diabética.3
Se puede realizar de inicio tomografía o resonancia magnética para excluir obstrucción mecánica o enfermedad de la mucosa que altere el vaciamiento gástrico, así como, endoscopia donde se observa retención de contenido gastro alimentario, se cuenta con algunos nuevos estudios para diagnóstico como son: prueba de aliento de con isotopos estables o cápsula de motor inalámbrico, sin embargo, el estudio de elección sigue siendo la gammagrafía de vaciamiento gástrico ya que se puede observar y cuantificar la retención de contenido gástrico posprandial, para considerarla positiva se debe esperar un período de 4 horas posprandiales con una retención del >10 %. Las correcciones hidroelectrolíticas provocadas por la enfermedad son fundamentales para evitar aumento de morbimortalidad. Si bien existen diferentes terapéuticas descritas, su efectividad, aún no es la deseada, y los pacientes exhiben alta probabilidad de reincidir en la sintomatología.
La gastroparesia es un trastorno funcional que tiene serias implicaciones para la calidad de vida de quienes la padecen.