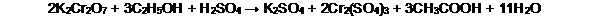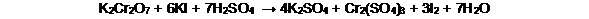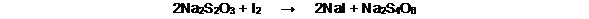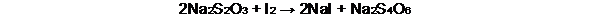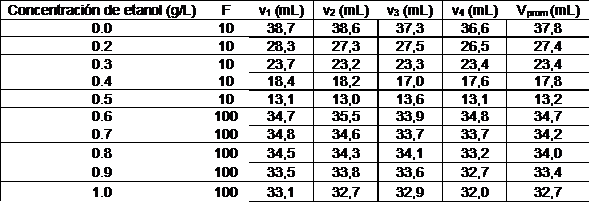Introducción
El programa alcoholero cubano y en especial la producción de etanol a partir de jugos mezclados de caña de azúcar necesita del desarrollo de nuevos procedimientos analíticos: precisos, de elevada productividad y de poca manipulación técnica que permitan mejorar la eficiencia global del proceso.1
Existen varias técnicas analíticas para conocer la concentración alcohólica en los vinos, licores, cerveza y ron. El desarrollo de técnicas analíticas rápidas es esencial para el seguimiento y control del proceso de fabricación de azúcar y la producción de etanol. Los datos que sirven de base deben ser obtenidos con técnicas analíticas confiables y precisas.2
En la industria de producción de etanol se realiza la determinación de la concentración del mismo por métodos espectrofotométricos que, aunque son de mayor uso en los laboratorios de las destilerías, precisan de la aplicación de las buenas prácticas de laboratorio porque se pueden presentar problemas de contaminación de solventes y alta imprecisión por las fuentes de error humano.
El etanol tiene alta demanda pues se emplea el 20 % de la producción anual en la rama farmacéutica y salud, 6,8 % en perfumería y 30,2 % en la elaboración de bebidas alcohólicas. El resto es empleado en procesos industriales como disolvente o combustible. Una de las vías de producción de etanol es a partir de la fermentación de productos del sector agrícola ricos en azúcares, aceites y almidones por microorganismos para pasar a un proceso de destilación. Este proceso está influenciado por factores como la concentración de azúcares del sustrato y el microorganismo fermentador que se emplee. Dentro de este, la fermentación alcohólica es la más utilizada.3
Los métodos para determinar la concentración de etanol se basan esencialmente en las siguientes técnicas: destilación seguida de medidas físicas o químicas, cromatografía, espectrometría infrarroja, inyección de flujo y valoración redox. Algunos de ellos son relativamente caros, consumen mucho tiempo, son complejos de realizar y requieren un laborioso pretratamiento de la muestra. Por tanto, existe una demanda creciente de métodos económicos, rápidos y fiables para la determinación de etanol. En el presente trabajo se discuten los más empleados, pues su objetivo es proponer el método analítico más adecuado para determinar la concentración de alcohol obtenido en una muestra por vía fermentativa.
Fundamentos teóricos
Cromatografía gaseosa
La cromatografía gaseosa (CG) es una técnica analítica que es utilizada frecuentemente, por tratarse de un analito volátil. Por otra parte, la cromatografía líquida de alta resolución, que es un poco menos popular, es también considerada una herramienta analítica importante para esta determinación y ha sido usada para determinar el rendimiento de la producción industrial de etanol, en el análisis de bebidas alcohólicas y de alimentos.4
En la CG, el principio fundamental es la separar dos o más compuestos con propiedades físicas diferentes que les permitan repartirse en las fases: la estacionaria y la móvil, que se mueve en dirección definida.
Se utiliza en la resolución de diversos problemas en la industria, en la medicina, en la biología y en el análisis ambiental, convirtiéndose en la actualidad como una herramienta para el control en una gran variedad de áreas. La cromatografía aprovecha las diferencias en la velocidad de retención de cada componente para separarlos, identificarlos y cuantificarlos. Existen dos tipos de cromatografía de gases: la cromatografía gas - sólido y la cromatografía gas-líquido.
Las ventajas del uso de la cromatografía radican en que son métodos automatizados, consumen una pequeña cantidad de muestra y los instrumentos pueden ser calibrados contra agua pura o soluciones estándar de etanol, lo que permite obtener un pico completamente resuelto de otros componentes de la muestra, por lo que la determinación es muy exacta. Se puede obtener buena exactitud en una amplia gama de concentraciones de la muestra, desde miligramos hasta nanogramos. Son métodos de alta sensibilidad con elevada eficiencia en la separación, por lo que son ampliamente reconocidos por toda la comunidad científica.
Una de las limitaciones de la CG es que todas las muestras deben ser volátiles; de lo contrario, no pasaran a través de la columna. En el caso de una muestra obtenida por fermentación, esto representa una limitante, porque no todos los componentes serán volátiles, cualquier traza de impureza puede tapar la columna y tendría que reemplazarse. Con la CG es difícil tratar compuestos iónicos, compuestos de elevada polaridad, y compuestos de peso molecular muy alto. Otra desventaja es que muchas veces es difícil confirmar la identidad de una muestra debido a que varios compuestos pueden tener tiempos de retención muy similares.5
Espectrofotometría
Los métodos espectrofotométricos empleados en la determinación de la concentración de etanol se basan en la oxidación catalítica de la enzima alcohol-deshidrogenasa en presencia de la coenzima NAD+.6
La espectrofotometría consiste en la cuantificación de analitos y en cómo puede determinar la concentración de un analito a partir de valores de absorbancia medidos a una determinada longitud de onda en un espectrofotómetro. Tiene la capacidad de manejar un de luz, separándolo en facilitar la identificación, calificación y cuantificación de su energía. Cuando la luz atraviesa una sustancia, parte de la energía es absorbida.
Las ventajas de la espectrofotometría son la alta sensibilidad y precisión de los resultados. El análisis es rápido, fácil de usar y requiere una preparación mínima de muestras. Como desventajas están el alto precio del equipo, que, además, requiere de lámparas especiales. Por otra parte, puede existir interferencia de otros compuestos y se destruye la muestra a analizar.
Valoración redox para determinar concentración de etanol
La valoración redox es uno de los métodos analíticos más antiguos y se aplica con frecuencia en la práctica analítica. Se basa en una reacción redox con dicromato para la determinación de etanol. El etanol se oxida a ácido etanoico al reaccionar con dicromato en medio ácido. La distinción colorimétrica de varias concentraciones de etanol se basa en la formación de iones cromato de color verde que, mezclados con el exceso de iones dicromato de color amarillo, producen colores diferenciables. Este método está validado para la detección cualitativa y cuantitativa de etanol en el condensado de aire exhalado de individuos a los que se les administró alcohol.7,8
Una valoración redox (también llamada volumetría redox, titulación redox o valoración de oxidación-reducción) es una técnica analítica muy usada, que permite conocer la concentración de una disolución, de una sustancia que pueda actuar como oxidante o reductor. Es un tipo de valoración basada en una reacción redox entre el analito (la sustancia cuya concentración se desea conocer) y la sustancia valorante.
En una valoración redox a veces es necesario el uso de un indicador redox o de un potenciómetro para conocer el punto de equivalencia o punto final. En otros casos las propias sustancias que intervienen experimentan un cambio de color que permite saber cuándo se ha alcanzado ese punto de equivalencia entre el número de moles de oxidante y de reductor, como ocurre en las iodometrías o permanganometrías.
La valoración redox se clasifica en valoración directa, donde el valorante reacciona directamente con la muestra. El consumo del mismo equivale directamente al contenido de muestra y se emplea para los cálculos. Otro tipo de valoración redox es la valoración por retroceso, donde se añade un exceso de valorante / reactivo conocido con exactitud a la muestra. Tras un período de reacción suficientemente largo, se valora este exceso con un segundo valorante. La diferencia entre la cantidad añadida del primer y el segundo valorante proporciona la cantidad equivalente de la muestra. Finalmente, en la valoración de valores en blanco compensados la muestra se disuelve en un solvente que también reacciona con el valorante y que conlleva un determinado consumo. Se le determina un valor en blanco para el solvente. El consumo total menos el consumo del solvente (valor en blanco) equivale en la muestra a la sustancia analizar.
Dentro de las principales ventajas se encuentran los bajos costos el análisis y que el equipamiento necesario se encuentra en cualquier laboratorio químico. El método es rápido porque las muestras pueden titularse y destilarse mientras se incuban otras. Dentro de las es desventajas se encuentra que, además de la dificultad de pipetear muestras de 1 mL con precisión, el método requiere cuidado al preparar la solución del estándar primario. Estas pueden oxidarse lentamente con el aire, por lo que deben estandarizarse con frecuencia. Además, se debe realizar un cálculo después de que se complete la titulación.
Materiales y métodos
Preparación de solución del dicromato de potasio (K2Cr2O7) a 1 mol/L
Se pesó 4,903 6 g de dicromato de potasio (K2Cr2O7) secados a 110 ºC por 1 h. Se disolvió en agua destilada, se vertió en un matraz y se aforó hasta 1 L (figura 1).
Preparación de solución del yoduro de potasio (KI) al 10 %
En la preparación de la disolución, se pesó 50 gramos de yoduro de potasio y se añadió a un beaker de 1000 mL. Se agregó 300 mL de agua para disolver el soluto, luego se vertió en un matraz volumétrico de color ámbar y se enrasó hasta 500 mL. Se rotuló con el nombre de la solución y fecha de preparación.
Preparación de solución de almidón como indicador
Este complejo señala el punto final en las titulaciones en las que se produce o consume yodo. En la preparación de la disolución se pesó 2 gramos de almidón soluble en agua y se añadió a un beaker de 1000 mL. Se agregó 500 mL de agua para disolver el soluto. Se vertió en un matraz volumétrico y se enrasó hasta 1000 mL. Se rotuló con el nombre de la solución y fecha de preparación (figura 2).
Preparación de solución de tiosulfato de sodio a 1mol/L
En la preparación de la disolución se pesó 27,2 g de tiosulfato de sodio (Na2S2O3ꟷ 5H2O) y se añadió a un beaker de 1000 mL. Se agregó agua destilada hasta disolver el soluto. Se vertió en un matraz volumétrico y se enrasó hasta 1000 mL. Se rotuló con el nombre de la solución y fecha de preparación (figura 3).
Valoración del tiosulfato de sodio (Na2S2O3ꟷ 5H2O)
El tiosulfato de sodio (Na2S2O3ꟷ 5H2O) no es una sustancia patrón primario, por lo que no se puede obtener concentraciones exactas por simple pesada. La estandarización de esta solución se basa en su titulación frente a sustancias patrones primarios como el dicromato de potasio (K2Cr2O7).
Donde el yodo es el oxidante y el dicromato es el reductor. El yodo liberado se valora con la solución de tiosulfato de sodio (Na2S2O3) utilizando almidón como indicador.
Mientras se agitaba el líquido se le añadió 2 mL de disolución de tiosulfato de sodio (Na2S2O3ꟷ 5H2O). Se le agregó 2 mL de disolución de almidón (C6H10O5)n y continuó la valoración hasta obtener un color verde claro (figura 4).

Fig. 4 Punto final de la titulación del tiosulfato de sodio para 0.1 N con almidón (C6H10O5)n como indicador.
La concentración exacta de la disolución tiosulfato de sodio (Na2S2O3) se calcula por la fórmula siguiente:
donde:
FN es un factor que se calcula según la ecuación:
donde:
V es el volumen gastado del valorante
Se realizaron diez mediciones para encontrar el valor promedio que se empleó en los cálculos.
Marcha analítica para la determinación de la concentración de etanol
Este método puede aplicarse solo con soluciones diluidas, por lo cual la muestra original debe diluirse a 100 o 1000 veces, según el grado de concentración. La muestra a diluir debe tomarse con pipeta automática, a fin de evitar vaporizaciones por succión. Tanto al llenar como vaciar la pipeta, su extremo debe encontrarse sumergido en el líquido. La marcha a seguir con la muestra diluida es la siguiente:
1. Preparar en un erlenmeyer una mezcla con 25 mL de dicromato de potasio (K2Cr2O7) 1 mol/L y 10 mL de ácido sulfúrico concentrado.
2. Agregar a la mezcla anterior 10 mL de la solución a analizar y dejar en reposo durante 30 minutos para que ocurra la reacción:
3. Añadir a la mezcla anterior 10 mL de solución de yoduro de potasio al 10%.
4. Valorar de inmediato el yodo puesto en libertad durante la reacción anterior con tiosulfato de sodio 1 mol/L y 0,5 mL de solución de almidón como indicador:
5. Preparar un blanco siguiendo el proceso descrito, pero con agua en lugar de la muestra.
La concentración de etanol en la muestra original se calculó por la ecuación siguiente:
Puesta a punto de la técnica de valoración redox para la determinar la concentración de etanol
Se preparan soluciones con concentración de etanol desde 0 g/L (blanco) hasta 1 gL.
Se pipeteó 25 mL de la disolución dicromato de potasio (K2Cr2O7) a 1 mol/L, se añadió a un erlenmeyer de 250 mL.
Se le agregó 10 mL de ácido sulfúrico concentrado.
Se le agregó 10 mL de las soluciones de etanol a valorar. Como este método se aplica a soluciones diluidas, se diluye la muestra en 100 veces. Este es el factor de dilución, F.
Se deja reposar 30 minutos y se añaden 10 mL de solución de KI al 10 % y 0.5 mL de disolución de almidón (C6H10O5)n
Se mezcló bien y se valoró con la disolución de tiosulfato de sodio (Na2S2O3ꟷ 5H2O) hasta obtener un color verde claro
Las muestras se analizaron por cuadruplicado.
Para la realización de esta técnica se tienen en cuenta los siguientes equipos y herramientas utilizadas que son de fácil obtención en cualquier laboratorio que son, una balanza analítica, una autoclave, microscopio óptico, centrífuga, matraz aforado, probeta, beaker, bureta, erlenmeyer, micropipeta, gradilla, tubos de ensayo y varilla de vidrio.
En la figura 5 se observa la muestra preparada con el blanco y la muestra con la adición de ácido sulfúrico concentrado.

Fig. 5 Solución de dicromato de potasio, a) preparada con el blanco y b) con adición de -ácido sulfúrico concentrado
Como se observa en la figura, ambas presentan la misma coloración.
A partir de los 15 min comienza a observarse en cambio de coloración en la muestra (Figura 6). A partir de los 20 minutos el color se mantuvo constante.

Fig. 6 Cambio de coloración en la muestra a) a los 15 minutos de reacción, b) a los 20 minutos de reacción
Al añadir la solución de yoduro de potasio al 10 % se notó un cambio de coloración (figura 7).
Al valorar el yodo puesto en libertad con tiosulfato de sodio (Na2S2O3→5H2O) y de almidón (C6H10O5)n como indicador se observó el cambio de coloración donde la muestra patrón vuelve al color inicial y la que se analiza toma un color verde claro (figura 8).
La reacción que ocurre es:
En la figura 9 se observa el punto final de la valoración.
En la tabla 1 se muestra el volumen de la solución de tiosulfato de sodio consumido en cada valoración
Con estos datos se calculó la concentración de etanol en función del volumen de la solución de tiosulfato de sodio consumido en la valoración redox (ecuación 3). Los resultados se muestran en la tabla 2.
En la tabla 2 se observa que los valores del error no sobrepasan el 10 %, lo que indica que se realizó adecuadamente la puesta a punto de la técnica, por lo que puede emplearse para determinar la concentración de etanol en una muestra obtenida por fermentación.
Un aspecto a tener en cuenta para la exactitud y precisión de la técnica de valoración redox es que pueden manifestarse algunos errores que influyen en la exactitud de la misma los cuales dependen de la habilidad del técnico que la realiza para determinar el punto de equivalencia.
Conclusiones
Se realizó un estudio bibliográfico con el cual se demostró que la técnica de valoración redox es una técnica confiable y económica, ya que no requiere de equipos costosos, fluido eléctrico o gas para ejecutarse.
Se puso a punto la instalación experimental y los resultados preliminares indicaron que la técnica de valoración redox es adecuada para la determinación de etanol con un error que no sobrepasa al 10%