My SciELO
Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Revista Cubana de Farmacia
Print version ISSN 0034-7515On-line version ISSN 1561-2988
Rev Cubana Farm vol.32 no.1 Ciudad de la Habana Jan.-Apr. 1998
Determinación de la disolución en tabletas de trifluoperazina 1 mg por el método de colorantes ácidos
Carlos Villalón Revilla,1 Marlen Vistel Vigo2 y Jorge Bosch Escobar3 1 Licenciado en Química. Especialista B en Tecnología Farmacéutica. Instructor Adjunto.2 Licenciada en Química. Especialista Principal en Investigaciones Químicas.
3 Técnico Medio en Tecnología Química.
RESUMEN
Se desarrolló un procedimiento espectrofotométrico por un método de colorantes ácidos con tropeolina OO para la determinación de la solución en tabletas de trifluoperazina 1 mg en las condiciones de disolución de la USP 23. El valor del pH seleccionado para la máxima partición del complejo colorante-trifluoperazina en cloroformo fue de 2,5, en el cual el complejo presentó una absorbancia máxima a 408 nm. La linealidad, precisión, exactitud y robustez del método se evaluaron en soluciones modelos de trifluoperazina de concentraciones exactamente conocidas, que permitieron demostrar la fiabilidad del procedimiento analítico desarrollado y determinaron su adopción como método alternativo de control de calidad del producto.Descriptores DeCS: ESPECTROFOTOMETRIA/métodos; TRIFLUOPERAZINA; COMPRIMIDOS; CALIDAD DE LOS MEDICAMENTOS; QUIMICA FARMACEUTICA.
La trifluoperazina es un psicofármaco indicado en el tratamiento de desórdenes psicóticos y en la ansiedad no psicótica;1 para su administración por vía oral se producen en el Laboratorio Farmacéutico "Oriente" tabletas en dosis de 1 mg.
Al comprobarse que el método analítico para la determinación de la disolución de las tabletas trifluoperazina establecido en la USP 232 no resulta apropiado por la baja concentración del principio activo en el medio, y dada la importancia de la disolución como un parámetro de control del proceso de fabricación lote a lote, que determina el alcance de los requerimientos de calidad exigidos al producto y su impacto en la biodisponibilidad del medicamento, nos llevó a revisar diferentes métodos de determinación de trifluoperazina.3-5 De acuerdo con nuestras condiciones se valoró el desarrollo de un procedimiento espectrofotométrico por el método de colorantes ácidos,5,6 en el cual se adicionan a la molécula de trifluoperazina de carácter básico a un valor fijo de pH controlado por una solución reguladora de éste, formando un ion par complejo coloreado que se extrae con un solvente orgánico, que presenta la máxima inten-sidad del color en la región de 400 a 420 nm y su validación conforme con los requerimientos exigidos en la USP 23,2 aspectos que constituyeron los objetivos de este estudio.
MÉTODOS
Determinación de la disolución. Las disoluciones de las muestras de tabletas y placebos se realizaron en un disolutor ERWEKA DT-6 de fabricación alemana, en las condiciones de disolución de la USP 23 2 Aparato I (cestas) 50 r.p.m., Medio 900 mL de HCl 0,1 M. Tolerancia: no menos del 75 % de la cantidad declarada de trifluoperazina (Q) debe disolverse en 30 min.Solución de tropeolina OO en solución reguladora. Se prepararon soluciones de tropeolina OO de 12 mg/100 mL en el rango de pH de 1,5 a 6,0 en solución reguladora de acetato,7 las que se lavaron con 2 porciones de 20 mL de cloroformo, desechándose la fase orgánica.
Soluciones patrones de trifluoperazina en solución reguladora. A partir de una solución patrón de trifluoperazina de 5,55 mg/mL en HCl 0,1 M (solución patrón), se prepararon soluciones de 111,1 mg/100 mL en solución reguladora de acetato en el rango de pH de 1,5 a 6,0.
pH para la máxima partición del complejo. De cada solución preparada anteriormente, se transfirieron 100,0 mL a un embudo separador de 250 mL a los que se adicionaron 10,0 mL de la solución de tropeolina OO con el mismo valor de pH y 10,0 mL de cloroformo, los que luego se agitaron mecánicamente durante 5 min. La fase clorofórmica se filtró a través de un aro de papel de filtro de 15 a 20 mm de diamétro, humedecido con cloroformo, a un tubo de ensayo adecuado con tapa y se registraron los espectros en el rango de 300 a 420 nm contra un blanco de HCl 0,1 M, tratado con las mismas condiciones en cada punto del rango estudiado de pH.
Validación. Se prepararon soluciones modelos de trifluoperazina con cantida-des disueltas exactamente conocidas del principio activo en el rango de 10 a 150 % de la cantidad declarada por diluciones de la solución patrón, que se ajustaron al rango de concentración con la adición de soluciones de placebos de ta-bletas obtenidas en las condiciones de disolución y se evaluaron los parámetros de linealidad, precisión, exactitud y ro-butez conforme a los criterios establecidos en la USP 23,2 mediante las pruebas de análisis de varianza de la regresión y prueba de hipótesis, con la utilización del paquete estadístico STATGRAPHICS.8 La decisión estadística se realizó al nivel de significación del 0,05 %.
RESULTADOS
El máximo de absorción del complejo en el rango de pH de 1,5 a 6,0 en cloroformo se halló a 408 nm, en el cual la máxima absorbancia para la partición del ion par complejo se halló en la zona estrecha de pH de 2,5 a 3,0 las cuales no difieren marcadamente entre sí (figura 1). El ajuste del medio a pH 2,5 " 0,05 en una solución patrón del principio activo de 111,1 mg/100 mL en HCl 0,1 M y en soluciones muestras de igual concentración con la adición de 10,0 mL de acetato de sodio 1 M, determinó su selección como el pH para la máxima partición del complejo. El efecto de la concentración del colorante, manteniendo constante la concentración del principio activo expresado como la razón molar tropeolina OO-trifluoperazina, se evaluó en soluciones patrones en el rango de concentración 1:1 a 18:1 en solución reguladora de acetato pH 2,5 y mostró una absorbancia máxima para el complejo en el intervalo de razón molar de 6:1 a 16:1 (figura 2), en el cual la concentración 14:1 presentó la máxima intensidad del color (0,645) y un valor mínimo para un blanco tratado en las mismas condiciones (0,013) y adecuada estabilidad a los propósitos de la determinación espectrofotométrica; a concentraciones mayores se observó la precipitación del colorante en la fase orgánica y un aumento de la intensidad del color en el blanco, resultados que permitieron establecer el procedimiento analítico para la determinación de la disolución (figura 3).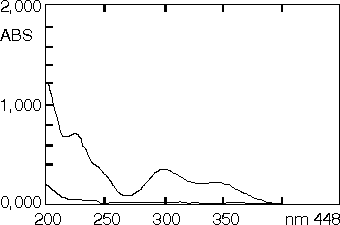
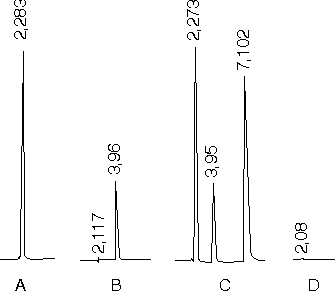
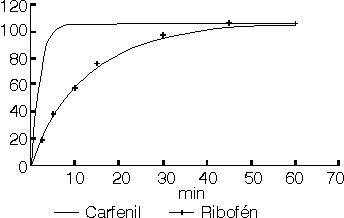
FIG. 3. Determinación de la disolución en tabletas de trifluoperazina 1 mg por el método de colorantes ácidos con treopolina OO.
La correlación de la intensidad del complejo en soluciones modelos de trifluoperazina en el rango de concentración de 10 a 150 % de la cantidad liberada del principio activo mostró una regresión linealmente significativa, en el cual a concentraciones menores del 50 %, por el aumento de la concentración del colorante, se producen variaciones en la absortividad del complejo que provocaron un aumento del coeficiente de variación de los factores respuestas superiores al 5 %; ello determinó el cumplimiento de los requerimientos de linealidad del método para la prueba de proporcionalidad del intercepto y la variación de los factores respuestas de 3,4 % en el rango del 50 al 150 % (tabla). La determinación de la repetibilidad en 5 réplicas a 3 niveles de concentración presentaron una variabilidad (CV) menor del 2 %, para los cuales se halló homogeneidad de varianza al contrastarse mediante la prueba de Cochran (C = 0,5044; p > 0,05), con la que se demostró que el factor de concentración no ejerció influencia en la precisión de los resultados obtenidos. Los resultados de reproducibilidad entre 2 analistas no mostraron diferencias significativas en la dispersión ni las medias obtenidas al contrastarse mediante la prueba de Fisher y t de Student respectivamente. La máxima variabilidad del procedimiento expresado mediante el coeficiente de variación global resultó 1,5 % con un límite de confianza para la determinación de 99,2 " 1,1 %, resultados que demostraron la precisión del método analítico.
Al expresar las cantidades disueltas halladas a los niveles de concentración evaluados como porcentajes de recuperación, no se evidenciaron diferencias estadísticas significativas contra el valor esperado al contrastarse mediante una prueba de hipótesis contra el valor de la t de Student (p < 0,05). En el análisis de varianza se constató que no existen diferencias significativas entre los recobrados promedio a los niveles de concentración estudiados, para un recobrado medio global del 100,3 " 0,8 % como medida de la exactitud. El cambio de solvente no produjo diferencias entre los valores medios de recobrado al contrastarse por una prueba de hipótesis, unido a los resultados de reproducibilidad entre 2 analistas corroboraron la robutez del método.
La evaluación preliminar en lotes de tabletas producidos recientemente y con 36 meses de almacenamiento en nuestro laboratorio, permitieron comprobar la practicabilidad del método en nuestras condiciones de trabajo y el cumplimiento de los requerimientos de disolución correspondientes al nivel S1 (figura 4), al hallarse cantidades promedio disueltas superiores al 80 %.
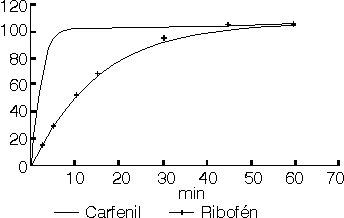
TABLA. Evaluación de la validación del procedimiento analítico para la determinación de la disolución en tabletas de trifluoperazina 1 mg con solución de tropeolina OO en solución reguladora pH 2,5
| Parámetros de validación | Estimado | EE | t | Probabilidad (> t) |
| Intercepto | 0,0365 | 0,0278 | 1,3105 | 0,2470 |
| Pendiente | 0,0054 | 0,0003 | 20,6833 |
| | ||||||
| Linealidad cuadrado medio | Fuente | Suma de GL | Cuadrado | Razón | F | Probabilidad (>F) |
| Modelo | 0,19549 | 1 | 0,19549 | 427,799 | 0,0003 | |
| Error | 0,0018279 | 4 | 0,0004570 | |||
| Total | 0,197308 | 5 | ||||
r2 = 0,9907
Error estándar de la determinación = 0,021
A: Repetibilidad
| Concentración teórica | (%) | Cantidad disuelta (Q) | (%) | Q media | (%) | DE | CV | (%) |
| 60 | 61,5 | 60,2 | 60,2 | 60,2 | 60,2 | 60,5 | 0,9 | 1,4 |
| 100 | 101,3 | 101,2 | 100,3 | 99,4 | 98,5 | 100,1 | 1,2 | 1,2 |
| 120 | 123,4 | 121,0 | 120,3 | 120,3 | 120,3 | 121,1 | 1,3 | 1,1 |
| Analista 1 | Analista 2 | |
| Q media (%) | 100,1 | 98,2 |
| DE | 1,2 | 1,7 |
| CV(%) | 1,2 | 1,7 |
| Número de determinaciones | 5 | 5 |
Q media (global) (%) 99,2
DE (global) 1,5
F = 2,00 (probabilidad F > 0,05)
t = 2,04 (probabilidad T > 0,05)
| Exactitud | | | | | | | | |
| 60 | | | | | | | | |
| 100 | | | | | | | | |
| 120 | | | | | | | | |
| | | | | | | | | | |
| | | | | | | | | | |
| | | | | | | | | |
DISCUSIÓN
En el desarrollo del método de colorantes ácidos para la determinación de la disolución en las tabletas de trifluoperazina 1 mg producidas en nuestro laboratorio, se seleccionó como colorante la tropeolina OO por presentar un rango de viraje (pH 1,2 a 2,8) próximo al pH del medio, donde la baja concentración del principio activo y el uso de celdas de 1 cm de paso de luz requirieron una alícuota de 100,0 mL para la determinación. La adición exacta de la solución de acetato de sodio 1 M facilitó el ajuste y control del medio a pH 2,5 " 0,05, que determinó su selección como el pH de máxima absorbancia para la partición del complejo de fase acuosa a la fase orgánica a 408 nm, en la cual la concentración molar del colorante 14:1 seleccionada presentó una absorbancia máxima donde no se produce la precipitación del colorante en la fase orgánica, condiciones que se establecieron como los parámetros que caracterizaron el método de colorantes ácidos para el sistema particular tropeolina OO-trifluoperazina en solución reguladora de acetato pH 2,5 y cloroformo como solvente espectrofotométrico.Los resultados obtenidos en los parámetros de validación exigidos en la USP 23,2 demostraron la fiabilidad, practicabilidad y sencillez del método desarrollado en nuestras condiciones, que permitieron su adopción como método alternativo de control para la evaluación de la calidad, con el cual se garantizó la determinación exacta y precisa de la disolución del producto.
SUMMARY
As spectrophotometric procedure was developed by using a methods of acid coloring matters with tropeolin 00 for the determination of the solution in trifluoperazine 1 mg tablets under the conditions of dissolution of the USP 23. The value of the ph selected for the maximun partition of the coloring matter-trifluoperazine complex in chloroform was of 2.5, in which the complex had a maximum absorbency at 408 nm. The lineality, accuracy, exactitude and robustness of the method were evaluated in model solutions of trifluoperazine of exactly known concentrations that allowed to demonstrate the reliability of the analytical process developed, and to determine its adoption as an alternative method to control the quality of the product.Subject headings: SPECTROPHOTOMETRY/methods; TRIFLUOPERAZINE; TABLETS; DRUG QUALITY; CHEMISTRY, PHARMACEUTICAL.
REFERENCIAS BIBLIOGRÁFICAS
- United States Pharmacopoeial Convention. The USP Drug Information. (USPDI). Rockville: Mack Printing; 1994:2108-10.
- United States Pharmacopoeial Convention. United States Pharmacopoeia. 23 ed. Rockville: Mack Printing;1995:1409.
- Pradas JN, Sivakumar M. HPLC quantification of tricomponent psychiatric formulation containing chlorpromazine, trifluoperazine and trihexyphenidyl. Pharmazie 1992;47:231-7.
- Martin C Mc, Street HV. Determination of trifluoperazine by GLC. J Chromatogr 1966;22 :274-6.
- Watson JR, Matsui F, French WN. Trifluoperazine tablets. Alternative methods of analysis. J Pharm Sci 1970;59:391-4.
- Higuchi T, Bodinin JJ. Alkaloids and other basic nitrogennus compounds. The acid dye method. En: Higuchi T, Brochman E. Pharmaceutical analysis. New York: Interscience Publishers;1961:314-8.
- British Pharmacopoeia Commision. British Pharmacopoeia. London: Her Majesty's Stationary Office;1988:A 68.
- Statgraphics 1.0 (paquete estadístico) STSC and Statical Graphics Corporation, 1985.
Lic. Carlos Villalón Revilla. Calle Sevilla, Carretera Siboney km 8 2, Santiago de Cuba, Cuba.














