My SciELO
Services on Demand
Article
Indicators
-
 Cited by SciELO
Cited by SciELO
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Revista Cubana de Farmacia
Print version ISSN 0034-7515
Rev Cubana Farm vol.48 no.1 Ciudad de la Habana Jan.-Mar. 2014
ARTÍCULO ORIGINAL
Desarrollo tecnológico de dorzolamida 2 % más timolol 0,5 % solución oftálmica
Techological development of 2 % dorzolamide plus 0.5 % timolol as eye solution
MSc. Armando Gato del Monte,I Lic. Aylema Romero Díaz,I MSc. Addis Bellma Menéndez,I Lic. Iván Morales Lacarrere,I MSc. Martha Botet GarcíaII
I Centro de Investigación y Desarrollo de Medicamentos (CIDEM). La Habana, Cuba.
II Empresa Laboratorio Farmacéutico "Julio Trigo". La Habana, Cuba.
RESUMEN
Objetivo: desarrollar una solución oftálmica de dorzolamida 2 % más timolol 0,5 % que cumpla con todos los requerimientos de calidad para proporcionar el efecto terapéutico deseado sin efectos adversos al paciente.
Métodos: se prepararon tres ensayos preliminares en los que se utilizaron clorhidrato de dorzolamida y maleato de timolol, una solución tampón que consistió en ácido cítrico monohidratado/citrato trisódico dihidratado, cuyo pH estuviese en el rango de 5 y 6, cloruro de benzalconio, y HPMC F4M (hidroxipropilmetilcelulosa) al 10 %. Se usaron estos componentes en sustitución de los recomendados en la literatura. Se estudió la estabilidad química y física de la formulación durante 3 meses en cuanto a las características organolépticas, concentración del ingrediente activo, el pH, así como las propiedades fluidimétricas, irritabilidad oftálmica y efectividad del preservo. Con la formulación de estudio se desarrolló y se validó la técnica analítica en el Centro de Investigación y Desarrollo de Medicamentos. Se determinó la linealidad, precisión, especificidad y exactitud de método. Se elaboraron tres lotes pilotos de 5 L cada uno. Se utilizó como material de envase frascos plásticos de polietileno de baja densidad con Master Batch de 5 mL de capacidad.
Resultados: los ingredientes activos, clorhidrato de dorzolamida y maleato de timolol, y los excipientes de calidad farmacéutica y el material de envase utilizado cumplieron con las especificaciones de calidad informados en la USP 33. Los análisis fisicoquímicos realizados a los tres lotes del escalado piloto e industrial cumplieron con las especificaciones de calidad de la técnica analítica desarrollada por el Departamento de Estabilidad del Centro de Investigación y Desarrollo de Medicamentos y con los análisis microbiológicos informados en la USP 33.
Conclusiones: los resultados obtenidos permiten la introducción industrial y sustituir la importación del referido medicamento.
Palabras clave: dorzolamida, timolol, estabilidad, reología.
ABSTRACT
Objective: to develop a 2 % dorzolamide plus 0.5 % timolol eye drop solution with all the quality requirements to provide adequate therapeutic effect without adverse reactions for the patients.
Methods: three preliminary trials were prepared with dorzolamide chlorhydrate and timolol maleate, a buffer solution based on monohydrated citric acid/dehydrated trisodic citrate with pH range 5-6, benzalkonium chloride and 10 % HPMC F4M (hydroxypropilmetylcellulose). These components replaced those recommended in the literature review. The chemical and physical stability of this formulation was studied for three months in terms of organoleptic characteristics, active ingredient concentration, pH, fluidmetric properties, eye irritability and effectiveness of preserver. The study formulation allowed developing and validating the analytical technique of the Center for the Drug Research and Development. Linearity, precision, specificity and accuracy of the method were determined. Three 5 L pilot batches were prepared. Master Batch 5 mL low-density polyethylene plastic bottles were used for packing.
Results: active ingredients, dorzolamide chlorhydrate and timolol maleate, the pharmaceutical quality excipients and the packing material met the quality specifications according to USP 33. The physical and chemical analysis of the three batches at pilot and industrial scales met the quality specifications of the analytical technique devised by the Department of Stability of the Center for Drug Research and Development and the microbiological analysis reported in USP 33.
Conclusions: the achieved results allowed introducing the formulation at industrial scale and replacing the imported drug.
Key words: dorzolamide, timolol, stability, rheology.
INTRODUCCIÓN
El clorhidrato de dorzolamida es un inhibidor potente de la anhidrasa carbónica II humana. La inhibición de la anhidrasa carbónica en los procesos ciliares del ojo disminuye la secreción de humor acuoso, presumiblemente al enlentecer la formación de iones bicarbonato con la subsecuente reducción de sodio y líquidos.1,2
El maleato de timolol es un bloqueante no selectivo de los receptores beta adrenérgicos que no tiene actividad simpaticomimética intrínseca, depresora miocárdica directa no anestésica local (estabilizadora de membrana) significativa (Cosopt. Ficha técnica de registro sanitario en FDA). El efecto combinado de estos dos agentes resulta en una reducción adicional de la presión intraocular, en comparación a cualquiera de los componentes administrados en forma individual.3
Luego de la administración tópica, la dorzolamida y el timolol reducen la presión intraocular elevada, esté o no asociada con glaucoma. La presión intraocular elevada es un factor de riesgo fundamental en la patogenia del daño al nervio óptico y en la pérdida del campo visual glaucomatoso.4 Cuanto más alto es el nivel de presión intraocular, mayor será la probabilidad de pérdida del campo visual glaucomatoso y daño al nervio óptico. La dorzolamida y el timolol reducen la presión intraocular sin los efectos colaterales comunes de los mióticos, tales como ceguera nocturna, espasmo de acomodación y constricción pupilar.5
En el mercado internacional se encuentra el Cosopt® sol. de la Merck Sharp & Dhome, de principios activos similares a los que se utilizan en el presente trabajo, pero no así en algunos de los excipientes, además este medicamento se importaba a los centros oftalmológicos del país para su uso en pacientes aquejados de presión intraocular elevada. Por tanto, el objetivo es desarrollar una solución oftálmica de dorzolamida 2 % más timolol 0,5 % que cumpla con todos los requerimientos de calidad para proporcionar el efecto terapéutico deseado sin efectos adversos al paciente y así sustituir importaciones.
Por consiguiente, se propuso comprobar la calidad farmacéutica de los ingredientes activos y de las sustancias auxiliares que se utilizarían en la formulación. De ahí realizar los ensayos de preformulación necesarios para la posterior selección de la formulación más prometedora, así como la selección del envase adecuado; caracterizar la formulación reológicamente; realizar los estudios de efectividad de preservos y desarrollar un método analítico para los estudios de estabilidad de la dorzolamida y el timolol en el producto terminado por cromatografía líquida de alta resolución (CLAR) e introducir el medicamento a nivel industrial.
MÉTODOS
Se realizó el análisis del clorhidrato de dorzolamida, lote 00299/C062, España, y maleato de timolol, lote 20071408P, India según la USP 33,6 así como de los excipientes que intervienen en la formulación.
Se prepararon tres ensayos preliminares utilizando los ingredientes activos, una solución tampón que consistió en ácido cítrico monohidratado/citrato trisódico dihidratado cuyo pH estuviese en el rango de 5 a 6, cloruro de benzalconio y HPMC F4M (hidroxipropilmetilcelulosa). Se usaron estos componentes en sustitución de los recomendados en el PDR, 2007.
Se utilizó la HPMC F4M al 0,1 %7 en el estudio de la estabilidad química y física de la formulación durante 3 meses en cuanto a características organolépticas, concentración del principio activo, pH, así como propiedades fluidimétricas, irritabilidad oftálmica y efectividad del preservo. Se seleccionó la formulación del estudio, se desarrolló y se validó la técnica analítica en el Centro de Investigación y Desarrollo de Medicamentos (CIDEM), determinándose la linealidad, precisión, especificidad y exactitud de método.
Para el estudio reológico se emplearon equipos de la firma Haake; entre estos, un reómetro, modelo RV 20, acoplado a un ordenador mediante un equipo Rheocontroller, modelo RC 20, utilizado como interfase y un ultratermostato, modelo F3, para controlar la temperatura de los ensayos. La corridas se realizaron en un intervalo de gradientes de velocidad comprendido entre 0 y 600 s-1, en un tiempo de 2 min igual para la curva ascendente como para la descendente, con una programación de 100 puntos de medición para cada una, utilizando el sistema M5 y el sensor de cilindros concéntricos NV estándar, a una temperatura controlada de 25 ± 0,1 ºC, con el auxilio del programa Rot 2.3, también de la firma Haake (Instruction Manual. Software Rotation. Version 2.3. Haake Mess-Technik GmbH. Co. Dieselstr. 4. D-7500 Karlsruhe 41. Germany).
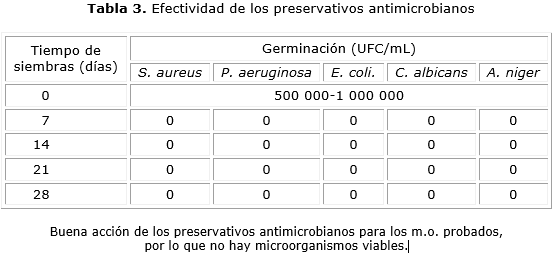
La efectividad antimicrobiana fue estudiada utilizando los ensayos generales de la USP 327 y los microorganismos estándar como: S. aureus, P. aeruginosa, E. coli, C. albicans y A. niger, a concentraciones de 500 000 a 1 000 000 de m.o./mL. Estos se analizaron inmediatamente después de contaminado el medicamento, y a los 7, 14, 21 y 28 días, se fueron observando los resultados obtenidos.
Se determinó la irritabilidad oftálmica en los tres lotes utilizando conejos albinos de Nueva Zelanda machos de 1,8 a 2,0 kg de peso corporal procedentes del Centro Nacional para la Producción de Animales de Laboratorio (CENPALAB), los cuales fueron mantenidos durante el ensayo en la sala con temperatura controlada de 2 ± 2 ºC y ciclo de luz-oscuridad 12/12 h. La alimentación consistió en dieta estándar para conejos CMO 1400 proveniente del CENPALAB y agua acidulada a libre demanda. El ensayo se realizó según la norma No. 405 de la OECD.8 Se le instilaron 0,1 mL de la sustancia en el ojo derecho de los animales. El ojo izquierdo fue tomado como control, ambos ojos fueron examinados a la 1, 24, 48 y 72 h de la aplicación inicial.
Con la formulación diseñada se elaboraron tres lotes pilotos (09002, 09003 y 09004) de 5 L cada uno en la Empresa Laboratorio Farmacéutico "Julio Trigo". El material de envase utilizado fue producido in situ durante la elaboración del medicamento y también respondió a las especificaciones de calidad para los frascos plásticos de polietileno de baja densidad con Master Batch y de 5 mL de capacidad, utilizando para su conformación y llenado la máquina Bottle Pack.
El estudio de estabilidad se realizó por el método acelerado y por vida de estante. Las condiciones utilizadas en el método acelerado fueron 40 ± 2 ºC, 75 % de Hr; se valoraron las muestras al inicio, 1, 2, 3 y 6 meses. En el estudio de estabilidad por vida de estante, las muestras fueron almacenadas a temperatura ambiente (30 ± 2 ºC), protegidas de la luz y se valoraron al inicio, 3, 6, 9, 12, 18 y 24 meses.
RESULTADOS Y DISCUSIÓN
Los ingredientes activos de clorhidrato de dorzolamida y maleato de timolol, y los excipientes de calidad farmacéutica utilizados en la formulación cumplieron con las especificaciones de calidad en cuanto a sus características físico-químicas de la USP 33, por lo que es posible utilizarlos en la formulación del colirio, cuyos parámetros de calidad fueron comprobados por la técnica de análisis desarrollada en el CIDEM para la determinación del principio activo, la cual mostró que es específica y precisa al cumplir con los criterios de linealidad y exactitud.
El medicamento desarrollado utilizando HPMC F4M7 y ácido cítrico monohidratado/citrato trisódico dihidratado para uso farmacéutico, cumplió con los requerimientos de calidad en los 3 lotes pilotos al inicio y transcurridos los 24 meses de estudios, almacenado en el envase propuesto certificado para su uso por el CIDEM.
El uso de frascos plásticos de polietileno de baja densidad con Master Batch de 5 mL de capacidad, producidos in situ por una llenadora Bottle Pack, permitió mantener estable al medicamento durante los estudios de estabilidad por 6 meses realizados a las muestras a temperatura de 40 ± 2 ºC, 75 % de humedad relativa y 24 meses a temperatura de 30 ± 2 ºC (tablas 1 y 2), lo que muestra que las formulaciones responden a las características organolépticas.
La concentración de los ingredientes activos se encuentró entre los límites establecidos (90,0-110,0 %) y no se observaron productos de degradación en el tiempo de estudio; el pH se mantuvo en el rango de 5,0-6,0 dado por la buena capacidad del sistema tampón utilizado. Esto demuestra que la formulación de clorhidrato de dorzolamida 2 % más maleato de timolol 0,5 % es estable en las condiciones estudiadas.
Los estudios de efectividad del preservo demuestran que el producto se comporta favorablemente ante la prueba de efectividad del agente antimicrobiano utilizado. Las muestras se contaminaron en la primera siembra en la que germinaron algunos microorganismos, pero al cabo de los 7 días no hubo germinación de ninguno de los microorganismos contaminantes e igualmente ocurrió a los 28 días del estudio (tabla 3); por lo que queda demostrado que la concentración del preservo utilizada en la formulación es adecuada para evitar crecimiento microbiano durante la preparación tecnológica del fármaco y en el período de almacenamiento, lo cual indica la eficacia de la concentración del preservo.
Después de la aplicación de la sustancia de prueba no se observaron lesiones en iris y conjuntiva en ninguno de los animales ensayados. Estas se observaron a la luz blanca para detectar presencia de eritema, edema y secreciones anormales, además de la reacción del iris a la luz, seguido del examen de la cornea por la tinción con fluoresceína y ante la luz de lámpara UV. Las lesiones de córnea se mantuvieron hasta las 24 h en tres animales, pero ya a las 48 h se mantuvo en un animal y no se observaron a las 72 h de iniciado el estudio (tabla 4).
Cabe destacar que dichas lesiones solamente involucraron un área muy pequeña de la córnea, las que resultaron poco significativas. El índice de irritación ocular fue de 2,5 lo cual se corresponde con la clasificación de no irritante. Estos resultados avalan el empleo de la formulación de dorzolamida 2 % más timolol 0,5 % sobre las estructuras oculares.
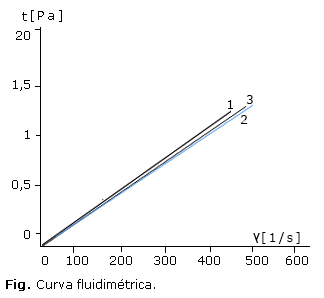
En la figura se presentan las curvas fluidimétricas prácticamente superpuestas en los tres lotes, las cuales caracterizan a la solución como un producto newtoniano, con una fluidez de 1,8 mPa.S a temperatura ambiente.
Se puede decir que mediante los estudios realizados se desarrolló un medicamento en forma de colirio que permite su introducción a nivel industrial y comercialización en el sistema de salud cubano para el tratamiento de diferentes afecciones oculares.
REFERENCIAS BIBLIOGRÁFICAS
1. Khaw PT, Shah P, Elkington AR. Glaucoma-1: Diagnosis. BMJ. 2004;328:97-9.
2. Grug Dex-Micromedex. [cited 2007 Jun 14]. Disponible en: http://www.thomsonhc.com/hime
3. Valk van der W. Intraocular pressure-lowering effect of adding Dorzolamide or Latanoprost to Timolol. A meta-analysis of clinical trials. Ophthalmology. 2007;114:40-6.
4. Demailly PH. Biodisponibilité des medicaments hypotonisants. J Français d'Ophthalmol. 2000:23:5.
5. Fechtner RD, Realini T. Fixed combinations of topical glaucoma medications. Curr Opin Ophthalmol. 2004 Apr.;15(2):132-5.
6. The United States of Pharmacopoeia 33 and The National Formulary 28 (USP 33-NF 28). User Guide Dorzolamide Hydrochloride, Timolol Maleate, microbiological test [CD-ROM]. Rockville: United Pharmacopoeial Convention, Inc.; 2010.
7. Gato del Monte A, Gómez Carril M, Morales Lacarrere I, Romero Díaz JA, Bellma Menéndez A, Botet García M. Desarrollo de Dorzolamida al 2 % solución oftálmica para el tratamiento de la presión intraocular. Rev Cubana Farm. 2011;45(4):471-9.
8. OECD Guideline for Testing of Chemical 405. Acute eye irritation/corrosion. Paris: Organization for Economic Cooperation and Development; 2002.
Recibido: 16 de septiembre de 2013.
Aprobado: 30 de octubre de 2013.
Armando Gato del Monte. Centro de Investigación y Desarrollo de Medicamentos (CIDEM). Ave. 19 de Mayo No. 13, Esq. a Amézaga, Plaza de la Revolución. La Habana, Cuba. Correo electrónico: armandogm@infomed.sld.cu