Introducción
La neumonía es una infección de las vías respiratorias inferiores (bronquios y alvéolos distales) causada por virus y bacterias. La neumonía adquirida en la comunidad (NAC) se refiere específicamente a los signos y síntomas clínicos de la neumonía adquirida fuera del entorno hospitalario. Se caracteriza por la aparición de fiebre o síntomas respiratorios, junto con la presencia de infiltrados pulmonares en la radiografía de tórax.1) A nivel mundial, más de 95 % de todos los episodios de neumonía clínica y más de 99 % de las muertes por neumonía en niños ocurren en países de bajos y medios ingresos.2) Según la Organización Mundial de la Salud la neumonía es la responsable del 15 % de los fallecimientos en niños menores de 5 años.3) La mayor proporción de muertes (81 %) se registró principalmente en niños menores de 2 años de edad que viven en países de ingresos bajos y medios.4
Streptococcus pneumoniae es el agente etiológico más frecuente en los casos de NAC bacteriana (2,2-50,9 %) en los niños menores de 5 años y puede causar complicaciones graves que requieren hospitalización.4) En la actualidad hay dos vacunas conjugadas en el mercado: 10 y 13 Valente (PCV10 y PCV13), de acuerdo con el número de los diferentes serotipos presentes. Hasta diciembre de 2019, 37 países y territorios de la región de las Américas usaban una de las vacunas contra el neumococo en sus programas regulares.2
A nivel global se ha estimado que la neumonía por neumococo disminuye por más de un tercio y que las muertes debido a infecciones por neumococo disminuyen por 51 % entre los años 2000 al 2015, después de la introducción de la vacuna conjugada contra el neumococo en muchos países.2) Luego de la implementación de las vacunas, los virus respiratorios se consideran los agentes etiológicos más frecuentes, pero la detección de virus en el tracto respiratorio superior no garantiza la causa de la neumonía ni excluye la presencia de un patógeno bacteriano.5
Aunque S. pneumoniae sigue siendo uno de sus principales organismos causales de NAC y, aunque la incidencia, la prevalencia y la mortalidad de la neumonía continúa elevada en niños y adultos en todo el mundo, se encontró que este microorganismo solo es el responsable del 10-15 % de las causas de NAC. Este hallazgo podría estar relacionado con la coexistencia de múltiples factores, como la vacunación contra S. pneumoniae, su inclusión en los calendarios nacionales a poblaciones en riesgo y el efecto que genera, la mayor incidencia de patógenos emergentes y la difusión y uso de las pautas de tratamiento vigentes.6
Por lo expuesto anteriormente, las neumonías bacterianas en niños menores de 5 años representan una importante carga para el sistema de salud debido a las hospitalizaciones y atención que demanda. La vacunación antineumocócica es una estrategia preventiva que puede modificar esta situación de salud. Por ello, el objetivo del presente trabajo fue realizar una revisión sobre el impacto de la vacuna antineumocócica en la incidencia y hospitalización en los niños menores de 5 años con neumonía adquirida en la comunidad.
Métodos
En este trabajo de revisión sistemática se utilizaron artículos en inglés y español publicados desde 2017 hasta 2021 en los sitios de búsqueda PubMed, ScIELO and Google Scholar. En el anexo se muestran los títulos en español de los artículos seleccionados. Se utilizó la pregunta clínica: ¿Cuál es el impacto de la vacuna antineumocócica en la incidencia y hospitalización de niños con neumonía adquirida en la comunidad? Población: niños. Exposición: Vacuna neumocócica. Resultado: Neumonía Adquirida en la Comunidad. Las palabras clave fueron: “Child” (MeSHTerm) en combinación con “Pneumococcal Vaccines” y “Pneumonia, Bacterial” (utilizados en PubMed); “Niños”, “vacuna neumocócica”, “neumonía adquirida en la comunidad” (utilizados en Scielo). El presente trabajo se encuentra en prioridades sanitarias “Infecciones Respiratorias y Neumonía”, según las “Prioridades de investigación en salud 2019-2023 del Instituto Nacional de Salud del Perú”.
Criterios de inclusión:
Artículos en español o inglés publicados en los últimos 5 años que incluyan, mediante combinaciones de palabras clave, en el título o en el resumen: “niños”, “vacuna neumocócica”, “neumonía adquirida en la comunidad” o “child”, “pneumococcal vaccines” y “pneumonia, bacterial”
Estudios analíticos
Criterios de exclusión:
Estudios que incluyan pacientes con neumonía nosocomial o intrahospitalaria.
Pacientes adultos.
Estudios descriptivos.
Estudios que no tengan relación directa con el tema que se analiza.
Artículos que no consignen autor o Digital Object Identifier (DOI)
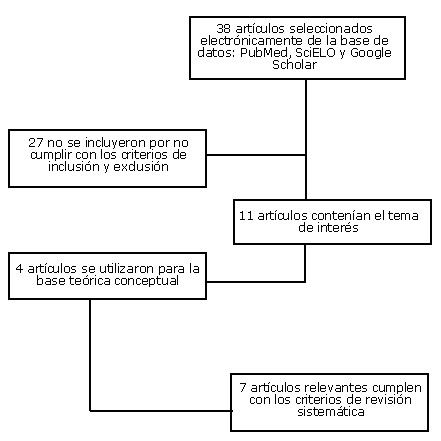
De los 136 artículos encontrados se descartaron 98 artículos por no cumplir con los criterios de combinaciones de palabras clave en el título o en el resumen. De los 38 artículos restantes, se descartaron 27 debido a que en los estudios incluían adultos, en otros estudios no estaba contenida la neumonía adquirida en la comunidad o no estaban enfocados al tema (Fig. 1).
Análisis y síntesis de la información
Para este estudio se incluyeron 7 estudios según los criterios de inclusión y exclusión ya mencionados. Se muestran las principales características de los estudios seleccionados publicados desde 2017 hasta 2021 (Tabla).
Tabla Títulos, autores y diseño de trabajos de investigación relacionados con el impacto de la vacuna antineumocócica en niños con neumonía adquirida en la comunidad
| Autores | Título | Año | País | Población | Diseño |
|---|---|---|---|---|---|
| Takeuchi N, |
Epidemiology of hospitalized pediatric community-acquired pneumonia and bacterial pneumonia following the introduction of 13-valent pneumococcal conjugate vaccine in the national immunization program in Japan | 2020 | Japón | 1,399 | Prospectivo, analítico, observacional |
| Zhang T, |
Effectiveness of 13-valent pneumococcal conjugate vaccine against community acquired pneumonia among children in China, an observational cohort study | 2021 | China | 139,127 | Prospectivo, analítico, observacional, cohorte |
| Jimenez Trujillo I, |
Decrease in the incidence and in hospital mortality of community-acquired pneumonia among children in Spain (2001-2014) | 2017 | España | 194,419 | Retrospectivo, analítico, observacional |
| Noel G, et al.10 | Evaluation of the Impact of Pneumococcal Conjugate Vaccine on Pediatric Community-Acquired Pneumonia Using an Emergency Database System | 2017 | Francia | 718,758 | Retrospectivo, analítico, observacional |
| Ruvinsky RO, |
Community acquired pneumonia incidence among children less than 5 years of age in Concordia, Argentina: vaccination impact | 2018 | Argentina | 330 | Prospectivo, analítico, observacional |
| Gönüllü E, |
Impact of the 13-valent pneumococcal conjugate vaccine on the incidences of community-acquired pneumonia and pneumonia-related hospitalizations in children ≤5 years after its implementation into the national immunization program of Turkey | 2020 | Turquía | 225,963 | Retrospectivo, analítico, observacional |
| Alvarado S, |
Efecto de la vacuna antineumocócica conjugada 10-valente en el área sur de Santiago de Chile, 2009-2015 | 2019 | Chile | 1’359,652 | Retrospectivo,ecológico |
Estudios prospectivos
En Japón, Takeuchi y otros7 realizaron un estudio con el objetivo de investigar los determinantes epidemiológicos y microbiológicos de hospitalizaciones por NAC y la neumonía neumocócica después de la introducción de la vacuna antineumocócica conjugada 13-valente (PCV13), entre abril de 2016 y marzo de 2019 en una ciudad llamada Chiba. La tasa de hospitalización por NAC en niños menores de 5 años en 2018 disminuyó en 45 y 32 en comparación con las tasas en los períodos pre-PCV7 y PCV7, respectivamente. La tasa de hospitalización por NAC en niños de 5 a 15 años aumentó en el período PCV7 en comparación con el período pre-PCV7, sin embargo, en el período PCV13, la tasa se redujo en 41 %, en comparación con las tasas en los períodos antes y después de la PCV7, respectivamente. Además, la proporción de NAC debida a S. pneumoniae disminuyó (de 16,4 % en el 2008 a 8,6 % en el 2018). El estudio reveló que después de la introducción de la PCV13, la incidencia de niños con NAC hospitalizados disminuyó no solo en los niños menores de 5 años, sino también en los de 5 a 15 años.
Zhang y otros,8) realizaron un estudio de cohorte observacional para investigar la efectividad directa de la PCV13 contra la NAC asociada con el portador del serotipo de la PCV13 (VT-NAC), debido a que la vacuna conjugada antineumocócica 13-valente (PCV13) está disponible desde 2017, pero solo a través del mercado privado con una baja tasa de aceptación.
La cobertura general de PCV13 en la ciudad de Suzhou fue del 6,5 % para +1 dosis, 6,2 % para +2 dosis y 5,8 % para +3 dosis. La efectividad de la vacuna en la primera visita entre los niños que habían recibido +2 dosis de PCV13 fue 60,9 % para VT-NAC y 17,9 % para NAC clínica. Las reducciones de la tasa de incidencia por 100 000 niños por año de observación para todas las visitas fueron 208 para VT-NAC y 720 para NAC clínica. Se llegó a la conclusión que la vacuna PCV13 fue protectora contra la hospitalización por VT-NAC y NAC clínica y se observó una disminución en la tasa de incidencia en los niños.
Con el objetivo de medir la efectividad de la vacuna PCV13 contra la NAC y la enfermedad neumocócica invasiva, y describir las variables asociadas con neumonía bacteriana y hospitalización, Ruvinsky y otros,11) realizaron un estudio prospectivo de vigilancia poblacional de la incidencia de NAC en niños menores de 5 años en el departamento de Concordia, Argentina. Se incluyeron en el estudio todos los niños menores de 5 años con diagnóstico clínico de NAC, a los que se les realizó una radiografía de tórax y se ingresaron en el hospital de referencia o en atención ambulatoria. Este estudio muestra que la vacunación universal con PCV13 a los 2 y 4 meses, con una dosis de refuerzo a los 12 meses, es eficaz en la prevención de casos de neumonía bacteriana en niños menores de 5 años, en comparación con el período de introducción pre-PCV13. La disminución en la incidencia de neumonia bacteriana fue significativa para todas las edades, independientemente del estado de vacunación.
Estudios retrospectivos
En un estudio realizado por Jiménez y otros,9) el cual tenía por objetivo analizar las tendencias en la incidencia y los resultados de las hospitalizaciones por NAC en niños españoles, 2001-2014 y evaluar el efecto de la cobertura de vacunación antineumocócica en este período.
La tasa de incidencia fue más alta entre los niños menores de 2 años y disminuyó significativamente en 3,67 % por año durante el período de estudio en este grupo de edad. Entre los niños de 2 a 4 años, la incidencia de NAC parece disminuir después del año 2009. Los aislamientos por S. pneumoniae disminuyeron significativamente con el tiempo, pero los aislamientos de virus aumentaron. En niños menores de 2 años y de 2-4 años, el aumento de vacunación antineumocócica se asoció con una disminución en la incidencia de hospitalizaciones por NAC.
En Francia, con el objetivo de analizar si existía relación entre la vacuna PCV13 y la reducción de la NAC en los niños, Noel y otros,10 realizaron un estudio en el que se observa una disminución significativa en la NAC solo para los niños entre 2 y 5 años de edad. La proporción de NAC que requirió hospitalización disminuyó 16 % entre los periodos pre-PCV13 y post-PCV13 temprano.
Gönüllü y otros,12en Turquía, realizaron un estudio observacional con el objetivo de investigar los cambios en la incidencia de NAC y hospitalizaciones relacionadas con la NAC después de la introducción de la PCV13 en niños ≤ 5 años de edad en el Programa Nacional de inmunización de Turquía. Cuando se comparó la incidencia anual media de NAC entre el período de transición de PCV13 (2011/2012) con un período posterior a la PCV13 (2016/2017), se encontró que la incidencia de NAC era 22 % menor. La incidencia de hospitalización relacionada con NAC disminuyó significativamente de 943 a 335/ 100 000 de 2011 a 2017. Además, la incidencia media de hospitalización por NAC disminuyó 35 % entre el período de transición de la PCV13 y el período posterior a la PCV13.
Con el propósito de evaluar el efecto de la incorporación de la vacuna antineumocócica 10-valente (PCV 10) en la incidencia de la enfermedad neumocócica invasora (ENI) y en la NAC en niños hospitalizados menores de 5 años en el área sur de Santiago de Chile, Alvarado y otros,13) realizaron un estudio ecológico entre 2009 y 2015. Al comparar la incidencia de casos de 2010 frente a 2010-2015, la razón de incidencias de ENI se redujo 10 % anual y la de NAC, 8 % en el mismo período.
Implementación de las vacunas
En estudios que se realizaron antes de la introducción de la vacuna antineumocócica, las tasas de hospitalización de niños menores de 2 años eran de 62,2/10 000 en EE. UU. y en Europa la incidencia de NAC en urgencias de niños menores de 5 años llegaba a 33,8/10 000.14,15 Con la implementación de las vacunas, las tasas en la actualidad han disminuido drásticamente. Las tasas de hospitalizaciones anuales en niños menores de 5 años, especialmente en los menores de 2 años, han disminuido. En España se observó una reducción anual de la tasa de ingreso de 3,4 % en los menores de 2 años durante el periodo del 2001 al 2014,9) en Turquía la tasa de hospitalización disminuyó 35 % entre el período de transición de la PCV13 y el período posterior a la PCV13.12 En Francia disminuyó 16 % entre los periodos prePCV13 y pos PCV13.10).No solo se observó disminución en los niños menores de 5 años, sino también en niños de 5 a 15 años. En Japón, con el uso de la vacuna PCV13, la tasa de hospitalizados se redujo en 41 %, en comparación con las tasas en los períodos antes y después de la PCV7.7) La vacuna PCV13 se elabora a partir de los siete polisacáridos capsulares neumocócicos presentes en la vacuna neumocócica de polisacáridos conjugados 7-valente (PCV7), que son 4, 6B, 9V, 14, 18C, 19F y 23F, más seis polisacáridos adicionales (1, 3, 5, 6A, 7F, 19A), todos ellos conjugados con la proteína transportadora CRM197 (Corynebacterium diphtheriae protein 127).16)
La PCV 13 induce una respuesta inmune dependiente de células T y genera de esta manera memoria inmunológica. Las vacunas de polisacáridos conjugados generan respuestas de anticuerpos en las mucosas (IgA) mediante la disminución de la colonización nasofaríngea por los serotipos presentes en la vacuna por reducirse la circulación de neumococos, y producirse una inmunidad de grupo que dificulta la adquisición de nuevos portadores y de futuros enfermos.17
En cuanto a la incidencia de casos de NAC, la revisión describe una marcada disminución, que varía entre 22 % en Turquía (2012-2017)12) y 8 % en Chile, (2010-2015).13) También se observó una significativa disminución en la incidencia en niños menores de 5 años para NAC consolidada con una tasa de incidencia anual de 714,6/100 000 individuos a 283,9/100 000 con la posterior introducción de PCV13; y en el caso de neumonía con derrame pleural, pasó de 132,9/100 000 individuos a 19,4/100 000 posterior al uso de la vacuna ya mencionada.11
En los diversos estudios se encontró que el agente etiológico más frecuente en los niños sigue siendo el S. pneumoniae; sin embargo, existe una disminución de su dominio7,8,9 y el serotipo neumocócico cambió de serotipos PCV13 a serotipos distintos y son los más dominantes el 35B, 15A y 11A/ E.7) En los pacientes que presentaron complicaciones, tales como el derrame pleural, la causa más frecuente es el S. pneumoniae.18 En aquellos pacientes que fallecieron, el agente etiológico cambió, y fueron P. aeruginosa, S. aureus y Legionella los más frecuentes.9
Recordar que S. pneumoniae sigue siendo el agente más tradicional en NAC debido a que posee una cápsula polisacárida. Este polisacárido capsular es el principal factor de virulencia y de patogenicidad del neumococo, debido a que induce la producción de anticuerpos protectores específicos en el huésped, de esta forma evita ser fagocitado por polimorfonucleares neutrófilos y macrófagos, e impide que los anticuerpos y el complemento lleguen a las estructuras internas.16
En cuanto a la efectividad de la vacuna, en la primera visita al hospital entre los niños que habían recibido +2 dosis de PCV13 fue 60,9 % para los niños portadores del serotipo de la PCV13 (VT-CAP) y 17,9 % para niños con NAC clínica.8 También se demostró que el esquema de vacunación universal con PCV13 a los 2 y 4 meses, con una dosis de refuerzo a los 12 meses, es eficaz para la prevención de casos de probable neumonía bacteriana en niños menores de 5 años, en comparación con el periodo de introducción prePCV13.11
En la población pediátrica, según la Organización Mundial de la Salud/Fondo de las Naciones Unidas para la Infancia (OMS/UNICEF), 23 millones de niños se quedaron sin las vacunas básicas administradas a través de los servicios de inmunización sistemática en 2020, 3,7 millones más que en 2019,19 por lo tanto, se requieren mayores estudios de la aplicación de estas vacunas (PCV10, PCV13) en el contexto de la COVID-19 en niños menores de 5 años, debido a la disminución de la cobertura de vacunación por las restricciones de la circulación por la pandemia, además del miedo en acudir a los centros de salud por temor a infectarse de COVID-19.19
Dentro de las limitaciones de esta revisión, no se tomó en cuenta otras bases de datos, ya que solo se utilizaron tres (PubMed, SciELO y Google Scholar). Otro aspecto que contribuye a limitar el estudio es la insuficiente cantidad de investigaciones sobre este tema en población pediátrica menor de 5 años. Así mismo, se sugiere mayores estudios prospectivos analíticos o ensayos clínicos aleatorizados que evalúen esta temática en distintos contextos.
Conclusiones
La vacuna neumocócica conjugada PCV 13 fue eficaz para reducir la incidencia de NAC y la tasa de hospitalización en niños, también se observó una disminución del Streptococcus pneumoniae como agente causal en los últimos años. Por lo que, debido a la eficacia de las vacunas frente al neumococo, la vacunación es una estrategia de salud muy eficaz para reducir esta clase de enfermedades, que son prevenibles por medio de la inmunización y debe considerarse la vacunación incompleta un factor de riesgo prevenible para el desarrollo de la NAC en preescolares.