My SciELO
Services on Demand
Article
Indicators
-
 Cited by SciELO
Cited by SciELO
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Revista Cubana de Medicina Tropical
On-line version ISSN 1561-3054
Rev Cubana Med Trop vol.51 n.3 Ciudad de la Habana July-Dec. 1999
Centro de Investigación-Producción de Vacunas y Sueros. Instituto "Finlay"
Estandarización y evaluación del ensayo vibriocida modificado
Resumen
La prueba vibriocida es un método confiable y bien documentado para determinar la presencia de anticuerpos bactericidas dirigidos contra los antígenos O de Vibrio cholerae 01. Se basa en que al mezclar diluciones de suero con una cantidad constante de bacterias y complemento se produce la lisis celular. La determinación del título se realiza por observación visual. En este trabajo se introdujo una modificación del método reportado, donde al medio de cultivo que se añade para detener la reacción se le adicionó un indicador de pH y glucosa, lo que permitió una lectura más rápida y por cualquier personal que no tenga experiencia en la realización de este ensayo, pues el cambio de color en la placa es evidente.
Descriptores DeCS: ANTICUERPOS BACTERIANOS/sangre; VIBRIO CHOLERAE/inmunología.
Los primeros estudios serológicos en cólera se realizaron en 1906 por Serkowski, y desde entonces los investigadores han realizado diferentes modificaciones del método, hasta 1968 en que Benenson describió una modificación del reportado por Muschel y Treffers en 1956, con el uso de placas de microtitulación en las que se añadió medio de cultivo líquido para detener la reacción dependiente del complemento y proporcionar nutrientes que permitieron crecer a los vibrios sobrevivientes.1
La prueba realizada con mayor frecuencia para la determinación de anticuerpos en infecciones por Vibrio cholerae es el ensayo vibriocida por medio de una microtécnica, ya que los resultados son sencillos de leer y se puede realizar con una mínima cantidad de suero.
Esta técnica ha sido ampliamente usada para medir los niveles de anticuerpos en el suero de pacientes, durante y después del cólera clínico; y en voluntarios, antes y después de la vacunación.2 Su introducción por Benenson ha abierto los horizontes para los estudios epidemiológicos de cólera en áreas endémicas del mundo,3 y constituye una técnica de uso obligado cuando se desea evaluar la eficacia de un preparado vacunal contra el cólera.
En este trabajo se describe una ligera modificación del método reportado por Benenson en 1968, donde usa la capacidad del Vibrio cholerae de utilizar en su metabolismo la glucosa que acidifica el medio y produce un cambio de color que permite una lectura mucho más clara.
Métodos
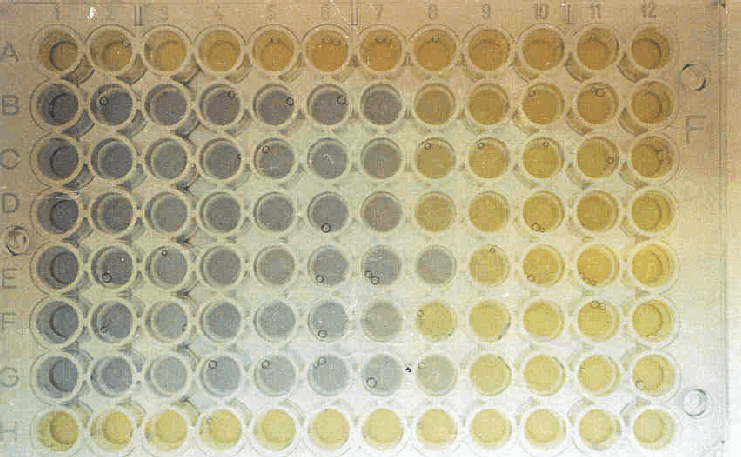
El día anterior a la prueba se sembraron las cepas VC 12 clásico Ogawa y VC 13 clásico Inaba que se mantenían conservadas en congelación a - 70 °C en skim milk a 10 % y glicerol a 20 %, en placas de BHI y se incuban a 37 °C junto con 4 cuñas del mismo medio sin inocular, toda la noche. A la mañana siguiente se pasan colonias aisladas de las placas a las cuñas precalentadas y se incuban 4 h a 37 °C. El crecimiento se recoge con solución salina estéril 0,85 % y la suspensión celular se ajusta en un espectrofotómetro a una densidad óptica (DO) entre 0,9 y 0,95, a una longitud de onda de 550 nm. La suspensión se diluye 1:10 y se mezcla con igual volumen de complemento humano diluido 1:5. Se añaden 25 mL de esta mezcla en una placa de microtitulación estéril en la que antes se habían realizado diluciones de los sueros a probar desde 1:10 hasta 1:20 480 en solución salina. La placa se incuba 1 h a 37 °C y luego se añaden 150 mL por pozo de medio BHI que contiene glucosa y púrpura de bromocresol en solución, ambos a 2 %. Se incuba de nuevo durante 4 h y se procede a la lectura por observación visual. El título se define como la dilución mayor del suero, en la que se observa inhibición completa del crecimiento bacteriano reflejado por la invariabilidad del color del medio de cultivo (fig. 1).
Fig. 1. Títulos de uno de los conejos inmunizados por vía oral
con células vivas.
Prueba de los sueros para detectar actividad bactericida intrínseca del complemento
Se preparó una suspensión bacteriana de la cepa VC 12 y VC 13 a una concentración de 3 x 107 ufc/mL y se incubó a 37 °C por 1 h junto con otro tubo que contenía 500 m L de esta suspensión y 500 m L del suero humano diluido 1:5. Ambas suspensiones se sembraron en placas de agar nutriente, se contó el número de colonias que creció en la placa donde se sembró la mezcla y se comparó con la placa control donde se sembró la suspensión celular. Se seleccionaron los sueros en los que se obtuvo un crecimiento mayor de 80 % con respecto al control.
Estandarización
Para la estandarización de la técnica se escogieron de manera aleatoria 6 muestras de suero provenientes de enfermos de Ecuador con edades entre 18 y 56 años. Se titularon 18 veces, en diferentes días, y se procesaron en paralelo por ambos métodos. Se determinó la exactitud y la reproducibilidad del método modificado en comparación con el original de Benenson (1968). Para lo primero se determinó el coeficiente de correlación y el análisis de regresión de los datos transformados (log) y para lo segundo se compararon las proporciones (X2) de ambos métodos de las determinaciones, no coincidentes con la moda de cada muestra.
Evaluación del ensayo
Una vez estandarizada la técnica se utilizó para verificar la inmunogenicidad de preparados vacunales administrados a conejos. Se determinó el título de anticuerpos vibriocidas a conejos inoculados por vía oral, con 2 dosis de células vivas de la cepa virulenta de V. cholerae C7258 biotipo El Tor serotipo Ogawa y de la cepa 638 atenuada genéticamente obtenida a partir de la primera. Se inocularon 3 conejos por cepa y 3 controles que recibieron sólo tampón fosfato salino (PBS). Como control positivo se utilizó un suero con alto título vibriocida (10240), obtenido en el laboratorio y como control negativo un suero de conejo normal.
Se les extrajo sangre a cada conejo antes de cada dosis y los días 7, 14, 21, 28, 35 y 42, para determinar los niveles de anticuerpos vibriocidas antes y después de cada inmunización.
Resultados
Durante la estandarización se obtuvieron por ambos métodos variaciones entre repeticiones de las muestras de sólo una dilución con respecto a la moda, no resultaron diferentes significativamente las observadas por cada método. Por otra parte, el coeficiente de correlación entre ambos juegos de resultados fue de 0,999 y la pendiente de la recta de regresión de 0,9987.
Entre las muestras de suero de conejo, evaluadas por esta técnica, se encontraron muestras positivas correspondientes a los días 7, 14, 21, 28, 35 y 42 después de la inoculación y negativas, correspondientes al día 0, así como todas las muestras de los conejos usados como controles que no recibieron células. En la figura se muestran gráficamente los títulos de uno de los conejos inmunizados por vía oral con células vivas. En la hilera A se colocó el suero preinmune y en el resto de las hileras, los sueros correspondientes a las siguientes extracciones. La hilera H es un control de suspensión que no contiene suero alguno. En la tabla se muestra el promedio de los títulos de anticuerpos vibriocidas de los 3 conejos inmunizados con las cepas 638 y C7258 respectivamente.
Tabla. Títulos de anticuerpos vibriocidas determinados por el ensayo colorimétrico de conejos inoculados con cepas atenuadas y virulentas de Vibrio cholerae
| Títulos | ||
| Tiempo | Cepa 638 | Cepa C7258 |
| 0 | 0 | 0 |
| 7 | 1280 | 2560 |
| 14 | 1280 | 640 |
| 21 | 1280 | 640 |
| 28 | 1280 | 640 |
| 35 | 1280 | 640 |
| 42 | 1280 | 640 |
Discusión
Los resultados obtenidos permiten señalar que la modificación introducida en este trabajo al método de Benenson (1968) no altera su exactitud y reproducibilidad original, sin embargo, evidencia más claro las diferencias entre negativos y positivos, permite realizar la lectura en menor tiempo y por técnicos menos entrenados, pues al realizarse la lectura por observación visual resulta un poco subjetivo y puede variar entre operadores. En el ensayo tradicional descrito se determina el título por turbidez en el pozo, donde por el pequeño volumen resulta difícil establecer con exactitud la diferencia entre turbidez y transparencia del medio BHI; con la modificación introducida, se produce un cambio de color de púrpura a amarillo que resulta evidente a simple vista.
El ensayo vibriocida que se describe aquí constituye una modificación del reportado originalmente por Benenson en 1968. Cuando se adiciona al medio de cultivo un azúcar bien asimilable por este microorganismo, los vibrios sobrevivientes crecen a expensas de los nutrientes, varía el pH del medio y torna el indicador de púrpura a amarillo, mejora la visualización de la reacción bactericida, lo que simplifica mucho la lectura y da un punto final mucho más claro e inequívoco en la titulación; el título se expresa como la mayor dilución del suero donde no se aprecia cambio de color.
Los títulos vibriocidas en las muestras evaluadas, tal y como se reporta en la literatura, comienzan a elevarse entre los 7 y 10 d, alcanzan un máximo entre los 14 y 21 d.4
Una segunda dosis de células vivas no logra aumentar mucho el título de anticuerpos. Resultados semejantes se han encontrado en estudios en humanos vacunados con células vivas, donde el porcentaje de individuos que seroconvirtieron en una segunda dosis es siempre mucho más bajo que la seroconversión positiva a la primera inmunización. Al comparar la seroconversión de un preparado vacunal con células vivas en áreas endémicas y no endémicas, se ha visto que el porcentaje de seroconversión es inversamente proporcional a los niveles de anticuerpos vibriocidas en sueros previos a la inmunización.5 Esto pudiera deberse a que los anticuerpos circulantes, producto de la primera inmunización, impiden la colonización de los microorganismos que se administran en una segunda dosis. Estudios realizados por Mosley han mostrado que los anticuerpos vibriocidas después de la infección desempeñan un papel importante en la inmunidad y que títulos mayores que 20 están asociados con la protección contra la colonización y la enfermedad.6 Sin embargo, Clemens7 define un nivel elevado cuando los títulos son mayores o iguales a 1 280, en cualquier caso, se puede considerar que el preparado vacunal administrado a los animales logró producir niveles de anticuerpos potencialmente protectores.
Teniendo en cuenta los resultados obtenidos por el método de Benenson, modificado en cuanto a la exactitud, reproducibilidad y la coincidencia del nivel de anticuerpos vibriocidas de los conejos inoculados con lo reportado en la literatura, se recomienda emplearlo en las determinaciones de los títulos vibriocidas de las muestras séricas, tanto para fines de diagnóstico epidemiológico como para la evaluación de la inmunogenicidad de un preparado vacunal contra el cólera.
Summary
The vibriocidal antibody test is a reliable and well-documented method to determine bacterial antibodies to Vibrio cholerae 01 antigens. It consists of mixing serum dilutions and a steady quantity of bacteria and supplement to cause cell lysis. Titer is determined by visual observation. In this paper, we implemented a change in the presented method where a pH and glucose indicator was added to the culture medium used to stop the reaction, which allowed a quicker reading by any person who are not very familiar with the carrying out of this test since the colour change in the plaque is quite evident.
Subject headings: ANTIBODIES, BACTERIAL/blood; VIBRIO CHOLERAE/immunology.
Referencias bibliográficas
- Benenson AS, Saad A, Mosley WH. The vibriocidal antibody response of cholera patients determined by a microtechnique. Bull WHO 1968;38:277-85.
- Ford AW, Seagroatt V, Altermant L, Hayhoe J. The mouse vibriocidal antibody test: a method for monitoring the potency of cholera vaccines. J Biol Standard 1982;10:47-57.
- Gangarosa E, DeWitt W, Feeley J, Adams M. Significance of vibriocidal antibodies with regard to immunity to cholera. J Infect Dis 1970;21:S36-S41.
- Clements ML, Levine MM, Young CR, Black RE. Magnitude, kinetics, and duration of vibriocidal antibody responses in North Americans after ingestion of Vibrio Cholerae. J Infect Dis 1982;145:465-73.
- Su-Arehawaratana P, Preecha S, Taylor D. Safety and Immunogenicity of different immunization regimens of CVD 103 HgR lie oral cholera vaccine in soldiers and civilians in Thailand. J Infect Dis 1992;165:1042-8.
- Mosley WH, Benenson AS, Buno R. 1968. A serological survey for cholera antibodies in rural East Pakistan. Bull WHO 1968;38:327-34.
- Clemens JD, Holmgrem T 1991. Field trial of oral cholera vaccines in Bangladesh: serum vibriocidal and antitoxic antibodies as markers of the risk of cholera. J Infect Dis 1991;163:1235-142.
Recibido: 12 de julio de 1999. Aprobado: 29 de septiembre de 1999.
Lic. Bárbara Cedré Marrero. Calle 190 No. 6917 e/ 69 y 81. La Lisa. Ciudad de La Habana.
1 Licenciada en Microbiología.
2 Licenciado en Bioquímica.
3 Doctor en Ciencias Biológicas.