INTRODUCCIÓN
El género Brucella produce una enfermedad infectocontagiosa conocida como brucelosis, zoonosis trasmitida entre animales, incluyendo al humano. En la actualidad existen diez especies reconocidas de brucelas. Las especies que afectan al hombre y a los animales susceptibles son: Brucella melitensis, B. abortus, B. suis y B. canis.1 La brucelosis tiene una amplia distribución mundial, aparece en países mediterráneos de África y Europa, en el Medio Oriente, Asia Central, la India, América Central y América del Sur.2 En América Latina, los países con mayor prevalencia son Argentina, México y Perú.3
La vía principal de transmisión de la enfermedad es la ingestión de productos lácteos y cárnicos, así como de sus derivados. Los veterinarios, técnicos y obreros vinculados a la manipulación de material biológico en salas de maternidad, ordeño y sacrificio de áreas productivas, así como el personal de laboratorio, se consideran personal con riesgo ocupacional. La brucelosis humana presenta manifestaciones clínicas muy polimorfas y cursa en ocasiones de forma asintomática y crónica, lo que trae consigo las presentaciones focalizadas (complicaciones) en los diferentes sistemas de órganos de la economía humana.4 Históricamente se notifican pocos casos de brucelosis humana en el mundo. En el año 2012 se publica el primer caso de endocarditis infecciosa como complicación de la enfermedad brucelar en Cuba.5 Su diagnóstico se fundamenta en los hallazgos clínicos, epidemiológicos y de laboratorio, en el que este último juega un papel primordial para su confirmación.6
En 2011, se introduce el sistema serológico comercial Febrile Antigen Brucella (FAB, Diesse, Italia)7 para la pesquisa de anticuerpos aglutinantes contra brucelas, en la Red Nacional de Laboratorios de Salud Pública Cubana. Esto permitió el rescate de la vigilancia de laboratorio de la enfermedad a nivel nacional. Sin embargo, esta técnica solo es útil durante la forma aguda de la enfermedad, pues a ella escapan casos crónicos, recidivantes y las reinfecciones. De igual manera, se incorpora en el Laboratorio Nacional de Referencia de Leptospiras y Brucelas (LNRLB), los sistemas ELISA IgM y ELISA IgG (Vircell Microbiologists, España)8 que posibilitan identificar si la muestra pertenece a un caso que cursa por el periodo agudo (IgM) o el de cronicidad (IgG) de la enfermedad.6
En 2015, se recibe en el LNRLB el sistema serológico comercial Brucellacapt® (Vircell Microbiologists, España).8 El sistema Brucellacapt® es una técnica de inmunocaptura-aglutinación para el diagnóstico de la brucelosis, que en un solo paso, de forma simple y cómoda, permite detectar anticuerpos aglutinantes (IgA, IgG e IgM) y no aglutinantes (IgA e IgG) contra Brucellaspp. Este sistema fue presentado en 1997 para el diagnóstico de la brucelosis humana, especialmente en su forma crónica. Además, para el estudio serológico en sueros procedentes de animales, para diferenciar los anticuerpos vacunales de los que se producen en animales enfermos. 9
El sistema Brucellacapt® es un ensayo homólogo a la prueba de Coombs (inmunoglobulina anti-humana). Esta técnica facilita la aglutinación de los anticuerpos aglutinantes y no aglutinantes del suero con la suspensión antigénica de lipopolisacárido (LPS) de B. abortus. Sin embargo, resulta muy compleja y laboriosa.10 Por estas razones, muy pocos laboratorios la realizan de forma habitual. Esta técnica al emplear LPS como antígeno puede dar lugar a reacciones cruzadas en sueros de pacientes infestados con bacterias que presentan LPS, específicamente del epítope O, como son Yersinia enterocolitica 09, Escherichia coli O:157, Salmonella O:30, Stenotrophomonas maltophilia y Vibrio cholerae O:1, entre otras.11
Dada la necesidad de continuar fortaleciendo el diagnóstico serológico de la brucelosis humana en Cuba, en la presente investigación se trazaron como objetivos evaluar y aplicar el sistema serológico comercial Brucellacapt® para la detección de anticuerpos contra Brucella spp.
MÉTODOS
Se realizó una investigación en servicios y sistemas de tipo observacional con un estudio de caso control anidado en el LNRLB, en el período comprendido desde enero de 2015 a junio de 2016.
Muestras clínicas
Grupo I (casos): 50 sueros de pacientes con brucelosis confirmada mediante elementos clínicos, epidemiológicos y presencia de marcadores séricos determinados por ELISA IgM y ELISA IgG (Vircell Microbiologists, España).8
Grupo II (controles): 55 sueros de "individuos sanos" donantes de sangre y 45 sueros de pacientes con otras enfermedades conocidas, miembros del grupo sindrómico, de ellos cinco con dengue, diez con Citomegalovirus (CMV), cinco con virus herpes simple (HVS), tres con Virus Epstein Bar (EBV), seis con hepatitis: cuatro de A (VHA) y dos de E (VHE), ocho con leptospirosis y toxoplasmosis respectivamente. Todos los sueros no tenían anticuerpos contra Brucella spp., mediante los ELISA IgM y ELISA IgG (Vircell Microbiologists, España).8
Grupo III: 695 sueros de casos sospechosos de brucelosis procedentes de zonas con alta focalidad animal y grupos de riesgo, remitidos al LNRLB desde instituciones del Sistema Nacional de Salud de Cuba.
Procedimientos
El sistema Brucellacapt® consta de tiras de pocillos de fondo en U que contienen inmunoglobulinas antihumanas. Tras la adición de los sueros y su dilución se añade el antígeno y se incuba 24 h. En la presente investigación se realizó el procedimiento de ensayo y la lectura e interpretación de los resultados según los criterios del fabricante. Los sueros con títulos desde 40 y hasta 160 se consideraron reactivos a brucelosis, los que mostraron títulos iguales o superiores a 320 fueron positivos con alto valor diagnóstico.8
Se aplicó las técnicas de referencia ELISA IgM y ELISA IgG para la confirmación de la infección en las muestras estudiadas.6,8
Análisis estadístico
Los resultados se tabularon en una base de datos de Excel, diseñada al efecto. Se calculó las frecuencias absolutas y los porcentajes. Además, se calculó mediante Epidat 3.1, los indicadores de desempeño: sensibilidad, especificidad, valor predictivo positivo y negativo, el índice de concordancia o validez, el índice de Youden, así como la razón de verosimilitud positiva y negativa, con un intervalo de confianza (IC) del 95 % y el valor de p ≤ 0,05.
RESULTADOS
El sistema serológico comercial Brucellacapt® demostró la presencia de anticuerpos contra Brucella spp., en el 100 % (50/50) de los sueros del grupo I, de los cuales el 58 % (29/50) resultó reactivo y el 42 % (21/50) positivo.
El 17 % (17/100) de los sueros del grupo II resultó reactivo. De ellos seis correspondientes a donantes de sangre supuestamente sanos, cinco a pacientes con diagnóstico de leptospirosis, tres de toxoplasmosis y uno en cada caso de dengue, CMV y VHA. En estos casos los títulos de anticuerpos detectados fluctuaron entre 40 y 80, los que se consideran bajos.
El sistema Brucellacapt® presentó sensibilidad del 100 %, especificidad del 83 %, índice de validez 88,67 %, valor predictivo positivo y negativo del 74,63 % y 100 %, respectivamente. Por otra parte, el índice de Youden fue de 0,83% y la razón de verosimilitud positiva fue de 5,88 %.
En la tabla se muestran los títulos de anticuerpos detectados por el sistema serológico comercial Brucellacapt® y su confirmación por los sistemas ELISAs de referencia en los sueros del grupo III. El 54,6 % (380/695) presentó títulos de 40 y hasta 160, en tanto en el 16,4 % (114/695) los títulos fueron iguales o superiores a 320.
Tabla Resultados de la aplicación del sistema serológico comercial Brucellacapt® en las muestras de suero del grupo III
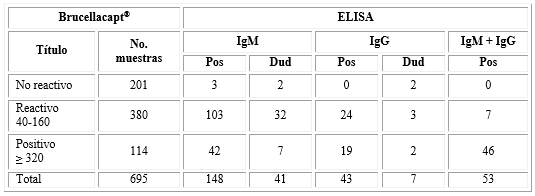
Pos: positivo. Dud: dudoso.
Los sistemas ELISAs confirman 35,1 % (244/695) de las muestras de suero reactivas, positivas y tres no reactivas por el sistema comercial en evaluación. En las muestras reactivas se identificó en el 14,8 %; 3,4 % y 1 % anticuerpos circulantes de la clase IgM, IgG e IgM + IgG, respectivamente. Mientras que en las muestras positivas se identificó IgM en 6 %; IgG en 2,7 % e IgM + IgG en 6,6 %. Se obtuvieron resultados dudosos en el 5,8 % (41/695) para el ELISA IgM y en el 1% (7/695) para el ELISA IgG. Por otra parte, en el 36,4 % (253/695) de las muestras reactivas y positivas por Brucellacapt® no fue posible identificar el isotopo de inmunoglobulina circulante en el paciente.
DISCUSIÓN
En la práctica habitual de los laboratorios de diagnóstico serológico de brucelosis se establecen los sistemas de pesquisa de anticuerpos mediante la implementación de métodos rápidos, sencillos y sensibles como los sistemas de aglutinación. Estos sistemas son de mayor aceptación por mostrar mejores resultados durante la fase aguda de la enfermedad ya que detectan el isotopo IgM, índice de infección aguda y por resultar más económicos. Sin embargo, la detección de IgA e IgG no resulta posible debido al bajo poder aglutinante o no aglutinante de estas moléculas, lo que constituye la limitante fundamental de su uso, al no reconocer el estado de cronicidad, las recidivas ni las reinfecciones por Brucella spp.12,13
La producción de anticuerpos incompletos, de forma no constantes y durante cualquier fase clínica de la enfermedad (aguda, subaguda y crónica), implica la necesidad de contar con sistemas de laboratorio que posibiliten su hallazgo de forma rápida y precisa.14 Es por eso que además del FAB, el ELISA IgM y el ELISA IgG, disponer de Brucellacapt® representa una oportunidad para el diagnóstico y seguimiento de los pacientes cubanos.15
Los indicadores de desempeño alcanzados en esta investigación son aceptables y coinciden con trabajos publicados, los que oscilan entre el 74 y 100% de sensibilidad y entre el 59 % y 98 % de especificidad.16,17
A nivel mundial existen bajos porcentajes de reacciones cruzadas mediante el Brucellacapt® con enfermedades tales como tuberculosis, salmonelosis, yersiniosis y la tularemia.16 En Cuba, no se vigilan serológicamente estas enfermedades, por lo que resulta difícil la comparación con ellas.
Aunque actualmente no se conoce el comportamiento de la brucelosis humana y animal en Cuba, existen notificaciones del Sistema de Información y Vigilancia Epizootiológica en el Instituto de Medicina Veterinaria que establecen el grado de afectación por brucelosis en entidades ganaderas, fundamentalmente en bovinos.18
Por tanto, la detección de títulos bajos de anticuerpos en las muestras de pacientes con otras enfermedades pudo ser consecuencia de una sensibilización tras el contacto con el microorganismo, además de la enfermedad actual. Por otra parte, la literatura consultada plantea que individuos que residen en zonas con alta focalidad, endémicas o que practican la crianza de determinadas especies de animales pueden presentar estos títulos.16
Los sistemas ELISAs para brucelas, pueden detectar inmunoglobulinas específicas con alta sensibilidad y especificidad, en estrecha relación con la naturaleza del antígeno empleado. La aplicación de ellos demuestra la posibilidad de diagnosticar la infección por Brucella spp., incluso en etapas muy tempranas en los que la serología convencional aún no muestra resultados positivos e incluso nunca se hace positiva.19,13,16
La obtención de resultados dudosos mediante los ELISAs, puede estar ocasionada por la incapacidad del sistema inmune del huésped de expresar su respuesta a la infección. En tanto, otros individuos pueden haber recibido antibioticoterapia en una o más ocasiones, lo que afecta la producción de anticuerpos. Ante esta disyuntiva se hace necesario solicitar otra muestra al paciente y repetir el ensayo.8 La no disponibilidad de un sistema ELISA que determine IgA, hizo quizás que no se pudiese identificar este isótopo en las muestras reactivas y positivas por Brucellacapt®.
Resulta difícil seleccionar una herramienta diagnóstica como prueba de oro para la confirmación serológica en la brucelosis. Esto hace necesario la evaluación integral de los resultados de las pruebas de laboratorio disponible (FAB, Brucellacapt®, ELISA IgM y ELISA IgG) junto a la clínica y epidemiología del paciente a la hora de establecer un diagnóstico certero.17,19
Por otra parte, las pruebas moleculares para la detección de ADN de Brucella spp., se desarrollan desde 1990. En 2015 se evaluó e implementó en el LNRLB una PCR sensible, específica y rápida que permite la detección de la proteína inmunogénica de membrana externa de 31 kDa que está presente en todas las especies de Brucella (BCSP 31) (B4B5).20 Esta prueba molecular se emplea en el estudio de casos clínicos seronegativos como herramienta alternativa.
El cultivo y el diagnóstico convencional de Brucella requieren de laboratorios con nivel de contención 3. Esta limitante hace que las herramientas serológicas para la detección de anticuerpos específicos sean indispensables para la detección oportuna de la infección y evitar con esto tanto las complicaciones irreversibles como el deterioro de la calidad de vida de los pacientes afectados. De otra parte, los resultados negativos de estas pruebas no excluyen la infección por Brucella spp., lo que demanda de una evaluación clínica y epidemiológica exhaustiva en cada caso.16
La generalidad de los sistemas serológicos tradicionales comerciales y caseros tienen la limitante de estar constituidos por antígenos genéricos y específicos, presentes en las cepas rugosas de las diferentes especies de brucelas, escapándose en este sentido B. canis (cepa lisa). Por ello, para el diagnóstico de esta especie, en particular, existen sistemas serológicos y moleculares.11
La coincidencia entre los resultados obtenidos por el Brucellacapt® y los sistemas de referencia ELISA IgM y ELISA IgG, demuestran que el primero constituye una herramienta útil para el diagnóstico de la brucelosis tanto aguda como crónica. Estudios internacionales que incluyen un mayor número de sueros indican resultados aun superiores,.15,17,19 La incorporación de este sistema al algoritmo de diagnóstico de la brucelosis humana en Cuba, fortalecerá la vigilancia al permitir la detección de casos que cursan por la fase de cronicidad de la enfermedad, la recaída o la reinfección.














