Introducción
Las primeras técnicas de aféresis fueron manuales, en ellas se obtenía una décima parte del volumen sanguíneo del paciente, la cual era sometida a centrifugación donde para separar el plasma de los elementos celulares. Estos últimos eran reinfundidos al paciente después de ser calentado y diluido en el plasma de los donantes. Las primeras técnicas de centrifugación se realizaron en Suiza en 1877, por el Dr. Carl Gustav Patrik de Laval, y se patentaron en 1881, cuando se diseñó la centrífuga de campana en los Estados Unidos de América.1,2
El término plasmaféresis se publicó por primera vez en el año 1914 por John Jacob Abel y otros, de la Universidad “Johns Hopkins,” Baltimore, EE.UU., quienes utilizaron esta técnica para mejorar los síntomas urémicos en perros a quienes se les había inducido insuficiencia renal mediante nefrectomía bilateral.3,4
Durante la Segunda Guerra Mundial se utilizó para obtener plasma de donantes voluntarios, y fue en la década de 1950 que el Dr. Edwin J. Cohn de la Escuela de Medicina de Harvard diseñó la centrífuga de campana e impulsó el desarrollo de la aféresis, ya que se utilizó como un procedimiento terapéutico para aliviar los síntomas de hiperviscosidad que se presentan en las gammapatías monoclonales, y mantiene su utilidad en el tratamiento del mieloma y de la macroglobulinemia de Waldenström.6,7
En 1960, Schwab y Fahey documentaron el efecto benéfico del intercambio plasmático en el tratamiento de la macroglobulinemia de Waldeström realizado rudimentariamente y de forma manual, donde se documentó que los pacientes con esta enfermedad y los que eran sometidos al procedimiento reducían la viscosidad del suero al reducir los niveles de macroglobulinas.8,9
En 1982, se fundó la American Society for Apheresis (ASFA), cuyo propósito fue no solo investigar la aféresis y sus indicaciones, sino también promover el intercambio de experiencias y opiniones a través de discusiones, presentaciones y publicaciones, así como colaborar y apoyar los estudios cooperativos sobre la aféresis terapéutica mediante estudios de costo-beneficio de los diferentes procedimientos aferéticos.10,11,12
En 1983, se fabricó el primer separador de plasma con membrana de fibra hueca. En 1985, la Asociación Médica Americana, trazó las primeras pautas para definir las indicaciones de plasmaféresis, y las clasificaron en cuatro categorías. A nivel mundial, la experiencia con estas técnicas es relativamente nueva; sin embargo, desde 1990, su aplicación terapéutica, aparte de usarse en enfermedades renales, se extendió a otras afecciones como enfermedades con alteraciones metabólicas, autoinmunes, reumáticas, hematológicas, neurológicas, oftalmológicas, del aparato digestivo, trasplante renal, hepático, de médula ósea, choque séptico y disfunción orgánica.11,12
Para 1993, la ASFA hizo una reevaluación de las categorías establecidas en 1985. En la cuarta edición de la revisión de sus guías se estableció la diferencia entre plasmaféresis y recambio plasmático. La primera consiste en la extracción de la sangre completa en un volumen de hasta 600 mL luego la separación en su componente celular y plasmático (este último es retirado sin la utilización de fluido de reemplazo), mientras que, en el recambio plasmático, el volumen a recambiar es mayor de 600 mL y requiere reposición con fluidos de reemplazo.13
Durante los años 60, se consolidó la técnica de aféresis, con el desarrollo de las membranas separadoras del plasma, base científica de las nuevas membranas de hemofiltración. El mecanismo por el cual la plasmaféresis resulta efectiva, es mediante la depleción rápida de factores específicos asociados a la enfermedad; los cuales incluyen autoanticuerpos patogénicos tipo inmunoglobulinas G y M, complejos inmunes circulantes, crioglobulinas, cadenas ligeras de inmunoglobulinas y lipoproteínas con alto contenido de colesterol.14
La aféresis tiene efecto en la modulación de la respuesta inmune, desbloquea y mejora al sistema reticuloendotelial y la depuración endógena de anticuerpos o complejos inmunes, mediante remoción de mediadores inflamatorios (citoquinas-complemento) y estimulación de clones de linfocitos para mejorar la respuesta citotóxica.15,16,17) A nivel internacional, ASFA y la Asociación Americana de Bancos de Sangre (AABB) actualizan cada tres o cuatro años las guías clínicas para el uso de aféresis terapéutica.18
Este artículo tiene como objetivo analizar los aspectos generales de la aplicación de la técnica de plasmaféresis en los pacientes críticos en disfunción orgánica.
Métodos
Se realizó una revisión de la literatura acerca del tema, publicada en los últimos 10 años en las bases de datos SciELO y Pubmed. Se emplearon los descriptores MeSH (siglas del inglés, medical subject headings) y DeCS (descriptores de ciencias de la salud). Se emplearon las palabras clave: plasmaféresis, disfunción orgánica, paciente crítico y aféresis.
Análisis y síntesis de la información
La lista de indicaciones de la plasmaféresis terapéutica (PFT) se incrementa en las últimas décadas. La ASFA ha establecido una clasificación de las enfermedades tratables mediante esta técnica para su uso en la práctica clínica, con un abordaje basado en la evidencia,22) la cual dividió las recomendaciones en cuatro categorías:
La primera (I), incluye enfermedades en las que la aféresis es aceptada como primera línea de tratamiento, ya sea como primer escalón o en conjunto con otras opciones de tratamiento; por ejemplo en el síndrome Guillain-Barré (GB), como terapia de primera línea, y en miastenia gravi (como primera línea combinada con terapia inmunosupresora e inhibición de la colinesterasa).
En la segunda (II), se incluyen condiciones clínicas en las que la aféresis es aceptada como segunda línea de tratamiento, ya sea como única opción o asociada a otras modalidades de tratamiento; como por ejemplo la encefalomielitis aguda diseminada posterior a dosis altas de esteroides intravenosos.
En la tercera (III), se incluyen aquellas situaciones donde el uso óptimo de la aféresis no se ha establecido aún; por lo que la aplicación de esta terapéutica debe ser individualizada, como en los pacientes con sepsis y falla multiorgánica.
La cuarta (IV), se refiere a situaciones clínicas en las que la evidencia publicada demuestra o sugiere que el uso de aféresis es inefectivo o solo hay casos aislados donde se reporta beneficio con el proceder, como por ejemplo pacientes con artritis reumatoide activa.19
Las evidencias a la hora de valorar la efectividad en los pacientes críticos con una disfunción orgánica establecida ya sea por la evolución de su enfermedad o por complicaciones de la quimioterapia administrada, muestran una mejoría, que pudiera contribuir a incrementar el índice de supervivencia en los servicios de terapia intensiva especializados en el manejo de las enfermedades hematológicas grave.19,20
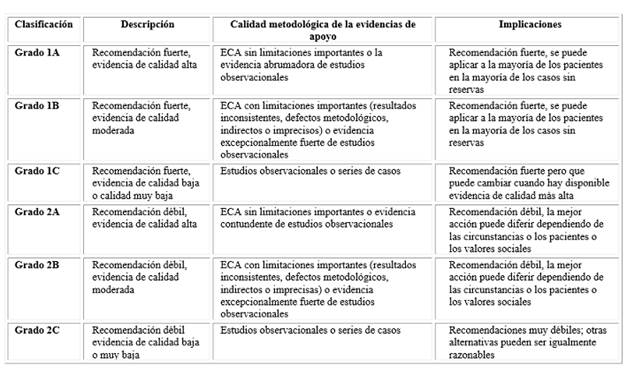
El mecanismo exacto por el que la PFT tiene un efecto terapéutico se desconoce, aunque se postula que el descenso o eliminación en la concentración sustancias tóxicas del plasma tras realizar el procedimiento, induce el efecto terapéutico. Estos elementos perjudiciales, que se eliminan pueden ser anticuerpos, inmunocomplejos, proteínas monoclonales, toxinas, citoquinas-mediadores y otras no conocidas. La PFT se ha empleado en el tratamiento de diversas enfermedades, especialmente en el área de la hematología según evidencias basadas en estudios controlados aleatorios (ECA).20,21) Los grados de recomendación se presentan en la (Tabla).
En los niños, la evidencia es más limitada, y se basa en estudios con pocos pacientes y no multicéntricos. Los protocolos y recomendaciones pediátricas son en su mayoría extrapolados de los estudios de adultos.
En la categoría III se incluye la sepsis grave porque en ella se producen trastornos hemodinámicos, de la coagulación y movimiento de citocinas que justifican el empleo del proceder en determinadas situaciones. Se conoce la eliminación de citocinas implicadas en el proceso séptico con la realización de plasmaféresis; además se piensa que una eliminación amplia de mediadores en esta enfermedad junto con la reposición de proteínas anticoagulantes podría revertir la cadena inflamatoria, la microangiopatías trombótica y restaurar la homeostasis.25
Los primeros estudios observacionales encontraron mejorías importantes de la supervivencia en el 60 - 87 % comparado con controles históricos con supervivencias del 20 - 40 %. Las series de casos sugieren que la PTF debe iniciarse temprano, para ayudar a la estabilización hemodinámica. Sin embargo, los resultados con estudios de mayor calidad de evidencia han sido controvertidos.26,27
En el año 2016, autores de diferentes nacionalidades realizaron un metanálisis que incluyó los cuatro estudios controlados y aleatorizados publicados, con un total de 194 pacientes. Concluyeron que la evidencia era insuficiente para la recomendación de su uso en la disfunción orgánica. En otro estudio, que incluyó todas las técnicas de depuración de la sangre utilizadas en fallos múltiples de órganos, se encontró un descenso de la mortalidad.28,29
En las unidades de cuidados intensivos dedicadas a la atención del paciente crítico se realiza la técnica de PFT cuando los pacientes presentan fallo de tres o más órganos, recuentos plaquetarios por debajo de 100 000 y clínica sugerente de una disfunción múltiple de órganos.30
La PFT es un procedimiento que actualmente tiene diversas indicaciones, en la decisión de su empleo debe considerarse la utilidad de otras terapias existentes, la evaluación activa de la respuesta esperada, costos y riesgos que implica el uso de un procedimiento de aféresis. Así, en pacientes con afecciones graves, en las que algún factor humoral es preponderante, se ha validado el uso de esta terapia.
En las últimas décadas, se ha perfeccionado la técnica de la PFT, lo que sumado al conocimiento de las principales complicaciones ha permitido en la práctica clínica minimizar y prevenir los riesgos que implica su utilización.
Las indicaciones de la PFT, corresponden principalmente a microangiopatías o a enfermedades reumatológicas graves, que no respondieron a terapia inmunomoduladora. En Cuba el escaso uso de la PTF en GB, se explica ya que en el país el tratamiento de GB se prefiere el uso de IgG endovenosa y se reserva para los pacientes que no responden a dicho tratamiento, conducta se basada en la evidencia disponible.
En cuanto al desarrollo de complicaciones, aun cuando estas se describen en un porcentaje considerable de pacientes (65 %), la mayor parte de las veces se trata de hallazgos de laboratorio sin traducción clínica, tales como hipocalcemia leve o trastornos subclínicos de la coagulación. La gravedad, comorbilidades y monitoreo riguroso dan cuenta de lo anterior, por lo cual es razonable promover el control estricto de estos pacientes y tomar medidas para la prevención de las complicaciones, como la suplementación de calcio, para impedir la ocurrencia de hipocalcemias sintomáticas por el uso de citrato en las soluciones de reemplazo utilizadas, además de un monitoreo clínico y de laboratorio que incluya electrolitos plasmáticos, función renal, pruebas de coagulación, hematocrito, evaluación de la volemia, eventuales reacciones transfusionales, etc.
En relación a la ocurrencia de infecciones, ningún trabajo previo ha logrado establecer de manera fehaciente, la utilidad de la plasmaféresis como factor de riesgo para el desarrollo sepsis. Estos pacientes reciben terapia inmunosupresora con alta frecuencia. Existen otros elementos que posiblemente intervengan en eventos infecciosos, como la condición propia del paciente, la adversidad de las terapias utilizadas, tales como ventilación mecánica y dispositivos intravasculares y el uso de terapias inmunosupresoras como corticoides y citotóxicos pero en vista de la evidencia disponible, no es posible establecer causalidad entre ellos y el uso de plasmaféresis.
Otras de las indicaciones donde se prescribe la PFT es en la insuficiencia hepática aguda (IHA) la que puede ocurrir en un hígado normal y se asocia a las complicaciones que presentan los pacientes con enfermedades hematológicas. Otras causas como la administración de fármacos utilizados en el tratamiento con quimioterapia en los pacientes con diagnóstico de enfermedades hematológica también puede producir una disfunción orgánica, la PFT se utiliza como tercera línea de tratamiento con buenos resultados reportados en pacientes con esta complicación.30
Limitaciones de la PTF
La más importante en los pacientes pediátricos es el alto volumen de los filtros diseñados para la realización de la técnica. Además, al presentar este elevado volumen, para evitar su coagulación, se necesitan flujos de sangre elevados. El fabricante considera que nunca se debe utilizar menos de 50 mL/min para el filtro pequeño. Esto obliga a utilizar catéteres que permitan ese flujo (hemofiltración) para su realización. La anticoagulación del filtro solo se puede realizar con heparina, pero al ser sesiones cortas no suele acontecer la coagulación del filtro. Si la sustitución se realiza con albúmina al 5 % hay que controlar la coagulación del paciente, sobre todo el fibrinógeno, que es el factor que más suele perderse.
Si se ha iniciado un tratamiento con sustancias que presentan alta concentración en sangre, aunque estén unidas a proteínas, estas se van a perder. Las inmunoglobulinas son un ejemplo. Debe tenerse en cuenta que parte de las dosis de antibióticos dadas pueden perderse durante la plasmafiltración, es recomendable ajustar el horario para administrarlos al terminar la terapia.
A pesar de las limitaciones en el campo de la especialidad de pediatría consideramos que una técnica que se puede implementar dentro de los protocolos de atención al paciente pediátrico con enfermedades oncohematológicas que se encuentren en disfunción orgánica como una de las pautas importantes del tratamiento.
En síntesis, el uso de plasmaféresis implica riesgos conocidos, que mayormente pueden ser prevenidos con un adecuado monitoreo, lo cual hace menos probable la morbilidad y la mortalidad relacionada al procedimiento. Además, se logra establecer en la experiencia del Instituto de Hematología e inmunología, que existe una asociación entre su uso con pacientes críticos en disfunción orgánica y una disminución del riesgo de muerte medidos por las escalas del sistema de evaluación de fisiología aguda y enfermedad crónica (APACHE, del inglés Acute Physiology And Chronic Health Evaluation) y la escala evaluación secuencial de la falla de órganos SOFA (del inglés Sequential Organ Failure Assessment Score) ambas usadas para estimar el riesgo de muerte en pacientes con disfunción orgánica, medidos durante y con posterioridad al curso del procedimiento. Por todo lo anterior sugerimos que el uso de la plasmaféresis es una herramienta útil y segura en pacientes hospitalizados en unidades de cuidados intensivos dedicados a pacientes críticos en disfunción orgánica si son adecuadamente monitorizados y se manejan oportunamente las alteraciones derivadas del uso de este procedimiento.