Introducción
Los defectos óseos postraumáticos (DOPT) provocan pérdida aguda de tejido óseo y conllevan a patologías como pseudoartrosis atrófica de huesos largos. Alteran el estilo de vida del paciente de manera drástica, e incluso lo incapacitan para sus actividades diarias, debido a secuelas como deformidad angular, rigidez articular, acortamiento disfuncional de la extremidad y dolor intenso.1,2,3,4,5
Las fracturas del húmero son lesiones comunes que representan entre el 5 y el 8 % de los traumas. Generalmente poseen una buena tendencia a consolidar; sin embargo, mantienen una incidencia global de hasta el 15 % en la pseudoartrosis,5 y con los métodos quirúrgicos y conservador, alcanzan de un 3 a un 5 %,4 y de un 145 a un 23 %,4 respectivamente.
La pseudoartrosis de la diáfisis humeral es una de las patologías más complejas de solucionar por los ortopedistas.2,3,4,5 El tratamiento depende de factores como la edad, tipo de pseudoartrosis y el estado general del paciente. Puede ser conservador o quirúrgico. El conservador se aplica en pacientes que no muestran sintomatología importante y para los que requieren el tratamiento quirúrgico reconstructivo, una de las opciones más viables es la técnica de inducción de membrana de Masquelet.3,4,5,6
Esta técnica consta de dos etapas: en la primera se reseca el segmento óseo afectado y se rellena con un espaciador hecho a mano de polimetilmetacrilato (PMMA) cubierto con antibiótico, que actúa como cuerpo extraño e induce la producción de un tejido tipo membrana biológica, rica en factores de crecimiento. La segunda etapa inicia de 4 a 8 semanas de la colocación del PMMA, este se reemplaza por injerto óseo autólogo y se conserva la membrana inducida para nutrirlo.1,2,7,8
El injerto vascularizado del peroné se considera la mejor técnica quirúrgica para el tratamiento de defectos óseos grandes (> 12 cm) en extremidades.1,3,9) Se describe por varios autores como un procedimiento exitoso debido al reducido trauma tisular y morbilidad en el lugar del injerto. El peroné posiblemente es el hueso más apropiado para ser usado en la reconstrucción ósea, por su forma geométrica, resistencia mecánica, longitud y potencial osteogénico.9,10,11
Presentación del caso
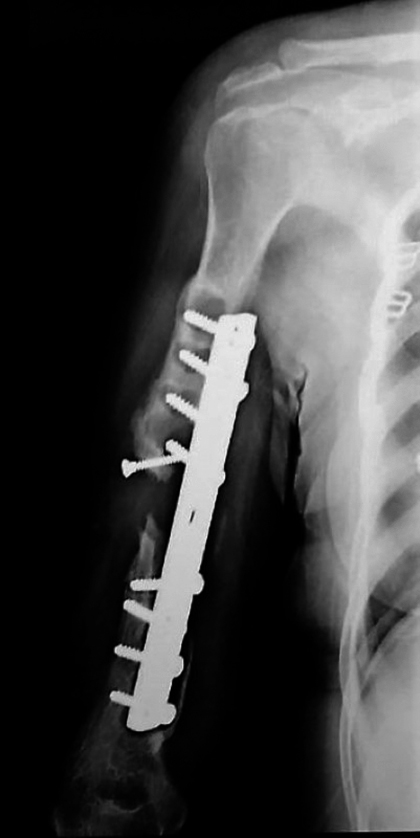
Paciente de 35 años, ama de casa, obesa, sufrió accidente de tránsito hace 4 años y tuvo fractura expuesta de diáfisis humeral derecha. Fue operada por reducción abierta y fijación interna con placa de compresión dinámica (DCP) de 4.5 mm, con abordaje y osteosíntesis anterior. Evolucionó inadecuadamente y debutó con pseudoartrosis atrófica diafasaria (fig. 1).
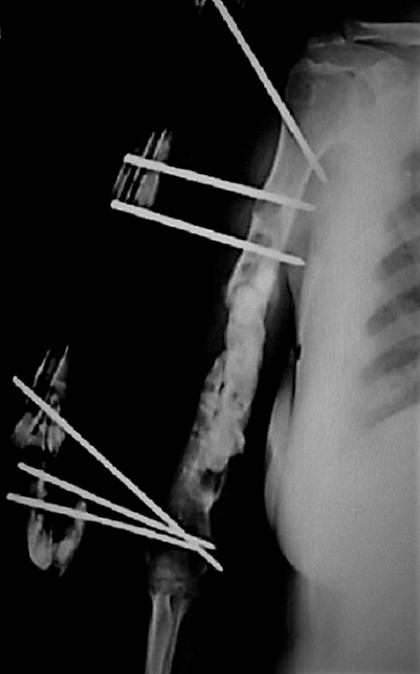
Se realizó la reconstrucción quirúrgica con la técnica bifásica de Masquelet. En la primera fase se llevó a cabo el desbridamiento de partes blandas y óseas, fue retirado el material de osteosíntesis y se hizo osteotomía de resección de fragmentos desvitalizados, verificados con el signo de Paprika, y el defecto resultante fue de 14 cm de longitud. Se obtuvieron muestras para realizar estudios anátomo patológicos: cultivo, Gram sin centrifugar y antibiograma. Ante la sospecha de infección subclínica, se colocó espaciador de cemento óseo PMMA impregnado con gentamicina. Mediante un cierre primario cuidadoso, se aseguró el espaciador y la cobertura ósea. Luego se estabilizó temporalmente con fijador externo uniplanar (fig. 2).
Tras 8 semanas, se cambió el espaciador de PMMA por autoinjerto peroneal no vascularizado de pierna contralateral, se retiró el fijador externo y se aseguró con tornillos y dos placas ortogonales, diseño PHILOS, de 3.5 mm. Se adicionó autoinjerto esponjoso de cresta ilíaca bilateral en los extremos proximal y distal por la presencia de un gran defecto cortical creado por el implante previo.
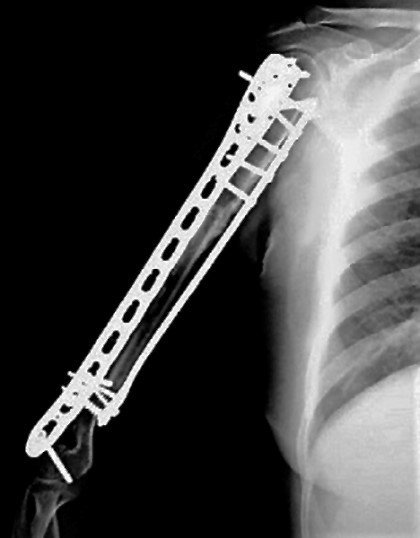
Transcurridos dos años, los resultados funcionales y radiológicos del miembro superior dominante fueron considerados buenos (fig. 3).
Discusión
La reconstrucción de un DOPT de huesos largos es un desafío para el cirujano ortopédico debido a la exigencia de los resultados tanto anatómicos como funcionales.3,4,5,8,10,11,12,13,14,15) Varios autores emplean la técnica de Masquelet en defectos óseos largos postraumáticos por sus beneficios para el paciente.4,10,14,15
La técnica de Masquelet tiene éxito en el tratamiento de DOPT de hasta 25cm; describe la importancia de la formación de la membrana que prolifera por reacción al espaciador de PMMA implantado.16) Esta membrana inducida, tejido pseudosinovial, está compuesta en la parte externa por células fibroblásticas y colágeno tipo I, en su interior por células de tipo epitelial semejante al epitelio sinovial y presenta una vascularización muy rica; además segrega varios factores de crecimiento que incluyen el transformante beta 1 (TGF-β1), el factor de crecimiento de fibroblastos 2 (FGF-2), la proteína morfogenética ósea 2 (BMP-2) y el factor de crecimiento endotelial vascular (VEGF); este último proporciona un ambiente vascularizado que contiene células madres mesenquimales (MSC), osteoprogenitoras, es decir, responsables de la actividad de formación ósea.3,14,17,18,19
La reconstrucción de DOPT con espaciadores de PMMA cada día suscita mayor interés. El uso del peroné estructural no vascularizado es una alternativa para reconstruir huesos en el miembro superior debido a que reduce la cantidad de injerto de hueso ilíaco para rellenar el defecto, pues tiene la longitud adecuada, la forma geométrica necesaria y aporta resistencia mecánica debido a su estructura córtico esponjosa que evita la refractura.5,10,11,14,20 Se empleó el autoinjerto de peroné por su similitud con el canal de torsión del húmero, al ser ambas diáfisis dos prismas triangulares con áreas transversales de diámetros diferentes que encajan entre sí, como un tubo dentro de otro.
En comparación con los injertos de peroné vascularizados, los injertos de peroné no vascularizados pueden necesitar más tiempo para la unión y no deben emplearse cuando no hay una buena cobertura de tejido blando y es difícil el suministro de sangre o la estabilización del injerto.14,21,22,23 La reconstrucción del defecto óseo con un injerto no vascularizado dará como resultado la migración de células desde el área perfundida del área receptora hasta la matriz casi acelular del injerto. Esto está relacionado con el hecho de que los osteoblastos no pueden sobrevivir en un entorno biológico con baja tensión de oxígeno.16
En este caso se tuvo un defecto óseo a cubrir de 14 cm de longitud, por lo que el autoinjerto peroneal no vascularizado necesario debía ser igual o de mayor tamaño. Ello se fundamenta en la opinión de Kashayi-Chowdojirao S y colegas que plantean que un autoinjerto peroneal no vascularizado >6 cm de longitud tiene capacidad relativamente disminuida para la incorporación y curación ósea. No obstante, con el aumento del injerto esponjoso de cresta ilíaca, debido a un defecto cortical creado por el implante previo, aumentará la incorporación ósea y la curación; esto constituye una alternativa al complicado procedimiento de injerto peroneal vascularizado en los países en desarrollo.10
Con respecto a la zona donante del autoinjerto, tanto del peroné como de la cresta ilíaca, se reporta un bajo índice de complicaciones; entre ellas, dolor, inestabilidad del tobillo en adultos y deformidad en valgo en infantes. La disección y preservación de los tejidos y estructuras deben ser meticulosas para reducir las complicaciones del sitio donante.20 Respecto a la obtención del autoinjerto peroneal no vascularizado, deben evitarse los 10 cm proximales y distales para minimizar los riesgos de daño al nervio peroneo y la inestabilidad del tobillo (límite de seguridad de 6 a 8 cm de peroné distal o al menos el cuarto distal del peroné) respectivamente.21,23
En este caso, se obtuvo el autoinjerto peroneal no vascularizado de acuerdo con las recomendaciones de la bibliografía consultada. Clínicamente la paciente solo manifestó dolor leve en las áreas donantes de autoinjertos y no presentó fracturas secundarias durante el posoperatorio. Se deduce que el tipo de osteosíntesis utilizada redujo la probabilidad de complicaciones. La estabilidad de la fijación con placas y tornillos contribuyó al remodelado, previno las fracturas por estrés y aseguró la congruencia de la extremidad.
Se puede afirmar que el injerto con peroné no vascularizado es un procedimiento más simple, menos costoso y más corto que el del injerto vascularizado.14,21,22,23
Conclusiones
La técnica de inducción de membrana de Masquelet con autoinjerto no vascularizado de peroné evidencia ser un tratamiento con menor tasa de complicaciones para los pacientes con defectos óseos postraumáticos segmentarios y de mejor pronóstico debido a que las tasas de consolidación óseas son adecuadas; se valida así la eficacia y la necesidad de reproducir este tipo de cirugías.