My SciELO
Services on Demand
Article
Indicators
-
 Cited by SciELO
Cited by SciELO
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Revista Cubana de Oftalmología
On-line version ISSN 1561-3070
Rev Cubana Oftalmol vol.30 no.1 Ciudad de la Habana Jan.-Mar. 2017
INVESTIGACIÓN
Modificaciones corneales posqueratoplastia penetrante óptica
Corneal changes after penetrating optical keratoplasty
Zaadia Pérez Parra, Carmen Padilla González, Madelyn Jareño Ochoa, Zulema Gómez Castillo, Michel Guerra Almaguer, Marlene Sibila González
Instituto Cubano de Oftalmología "Ramón Pando Ferrer". La Habana, Cuba.
RESUMEN
Objetivo: determinar las modificaciones de la córnea donante en el primer año de la posqueratoplastia.
Métodos: se realizó un estudio descriptivo, longitudinal y prospectivo de serie de casos en 45 pacientes. Para el procesamiento de las variables se utilizó la prueba de Chi cuadrado con corrección de Yates asociada a pruebas de rangos con signos de Wilcoxon y la prueba de probabilidades exactas de Fischer.
Resultados: el diagnóstico más frecuente fue la queratopatía bullosa (35,5 %). La pérdida celular anual fue de 22,8 %; el astigmatismo oblicuo con 61,5 % y la media del cilindro queratométrico de 5,96. En microscopia confocal encontramos ausencia de fibras nerviosas (86,7 %), presencia de queratocitos activados (22,2 %) y haze (11,1 %). Los injertos transparentes correspondieron al 82,2 %. Observamos queratocitos activados en 80 % de córneas no transparentes. El 33,3 % de los leucomas corneales se opacificaron. La complicación más frecuente fue el glaucoma secundario (33,3 %). El 100 % de las úlceras corneales bacterianas evolucionaron a fallo del injerto.
Conclusiones: la córnea posqueratoplastia presenta una pérdida celular endotelial anual de 22,8 %, astigmatismo oblicuo, cilindro queratométrico entre 3-6 dioptrías, presencia de queratocitos activados y haze corneal como factores pronósticos de pérdida de transparencia del injerto. El leucoma corneal posúlcera, la queratopatía bullosa como diagnóstico preoperatorio y la úlcera corneal bacteriana como complicaciones provocan pérdida de transparencia del injerto.
Palabras clave: queratoplastia penetrante; injerto corneal; fallo del trasplante.
ABSTRACT
Objective: to determine the changes in the donor cornea after one year of keratoplasty.
Methods: prospective, longitudinal and descriptive case series study conducted in 45 patients. For variable processing, the study used Yate's corrected Chi-square test associated to Wilcoxon's range test and to Fisher's exact test.
Results: the most common diagnosis was bullous keratopathy (35.5 %). The annual cell loss was 22.8 %; oblique astigmatism with 61.5 % and the mean of the keratometric cylinder was 5.96 %. Using the confocal microscopy, we found lack of nervous fibers (86.7 %), presence of activated keratocytes (22.2 %) and haze (11.1 %). Transparent grafts represented 82.2 %. Activated keratocytes were observed in 80 % of non-transparent corneas. In the study, 33.3 % of corneal leukomas showed opacification. The most common complication was secondary glaucoma (33.3 %). All the bacterial corneal ulcers evolved into failed graft.
Conclusions: after keratoplasty, the cornea showed annual endothelial cell loss of 22.8 %, oblique astigmatism, 3-6 diopter keratometric cylinder, presence of activated keratocytes and corneal haze as prognostic factors of loss of graft transparency. The post-ulcer corneal leukoma, bullous keratopathy as preoperative diagnosis and bacterial corneal ulcer as main complication cause loss of graft transparency.
Key words: penetrating keratoplasty; corneal graft; transplant failure.
INTRODUCCIÓN
Las afecciones de la córnea, tanto congénitas como adquiridas, provocan opacidad que dificulta u obstruye el paso de la luz, o una deformidad en su curvatura, que impide que la imagen se forme correctamente en la retina. La córnea es la única parte del ojo que puede ser trasplantada y la queratoplastia es el principal recurso terapéutico para restaurar la visión en estos casos. Es una de las técnicas quirúrgicas más antiguas de la Oftalmología y constituye la técnica de trasplante de órganos y tejidos más frecuentemente realizada y de mayor éxito en todo el mundo.1
El aumento en las indicaciones de la queratoplastia penetrante se debe, entre otros factores, al aumento de la expectativa de vida, mejor selección del tejido donado, los avances en la conservación de la córnea donante y la evolución de las técnicas e instrumental quirúrgico. El progreso en la inmunología corneal y el desarrollo y uso de fármacos antinflamatorios e inmunosupresores, el conocimiento de la importancia del endotelio corneal, así como el rápido reconocimiento y manejo terapéutico del rechazo corneal, además de las características anatómicas de avascularidad y privilegio inmunológico de la córnea, han mejorado los parámetros tanto en términos de supervivencia del injerto como aquellos funcionales que implican una finalidad refractiva,1-3 aspectos que miden el éxito de la queratoplastia penetrante.
Un resultado anatómico excelente puede no ser satisfactorio si la visión a través de un injerto transparente no resulta buena por la existencia de un astigmatismo elevado o irregular o por afecciones oculares asociadas, por lo que el manejo del paciente posqueratoplastia se ha convertido en uno de los mayores retos para el cirujano de córnea.
El seguimiento del injerto corneal a largo plazo constituye un tema de gran interés para profundizar en el estudio de la cicatrización corneal y en la regeneración de los nervios posqueratoplastia, así como para conocer los factores que influyen en la transparencia del injerto y el diagnóstico precoz del rechazo al trasplante. En el Instituto Cubano de Oftalmología "Ramón Pando Ferrer", a pesar de la introducción y el desarrollo de las técnicas de cirugía de trasplante lamelar selectivo, la queratoplastia penetrante constituye la técnica quirúrgica de trasplante óptico más frecuentemente realizada.
El presente estudio tiene como objetivo determinar las modificaciones de la córnea donante en el primer año de la posqueratoplastia, lo que nos permitirá profundizar nuestros conocimientos sobre los resultados anatómicos y funcionales de los ojos operados de queratoplastia penetrante.
MÉTODOS
Se realizó un estudio descriptivo, longitudinal y prospectivo de serie de casos en 45 pacientes operados de queratoplastia penetrante óptica en el Servicio de Córnea del Instituto Cubano de Oftalmología "Ramón Pando Ferrer" en el período comprendido de enero a diciembre del año 2013. A todos los pacientes se les realizó consulta de seguimiento al primer, tercer, sexto y duodécimo mes. Los datos de identidad personal y los que se refieren a las variables incluidas fueron vertidos en un modelo de recogida de datos. En la córnea donante se estudió la densidad celular endotelial (microscopio endotelial de banco KONAN) inmediatamente después de la conservación del botón corneal, a las 24 horas de conservado, y se tomó el valor más bajo.
En el receptor se evaluaron la edad, el sexo y el diagnóstico preoperatorio. A los 6 y 12 meses de la cirugía se evaluaron la transparencia del injerto corneal, las complicaciones, el cilindro queratométrico y las modificaciones histológicas (Confoscan-4, NIDEK). En aquellos pacientes con córnea transparente se evaluó la densidad celular (microscopio endotelial SP-9000, KONAN) y el patrón topográfico (topógrafo Magellan). Se creó una base de datos utilizando el programa Microsoft Office Excel. Para la variable edad se realizó una estratificación de los datos. Las variables cuantitativas se procesaron por las pruebas Chi cuadrado con la corrección de Yates, asociada a prueba de rangos con signos de Wilcoxon. Se compararon mediciones en Banco de ojo contra el posoperatorio de los 6 y los 12 meses y asociado a la prueba de probabilidades exactas de Fisher, asumiendo comparación entre pacientes con trasplante transparente o no transparente, para lo que se empleó el paquete estadístico EPIDAT y/o SPSS versión 15.0. En todos los análisis se consideró como significativo un valor de p menor o igual a 0,05. Se utilizaron medidas de frecuencia absoluta y relativa, medias e intervalos de confianza presentados en tablas y gráficos. El estudio cumplió con la II Declaración de Helsinki y con la legislación vigente en Cuba, de acuerdo con lo establecido en el Sistema Nacional de Salud y previsto en la Ley No. 41 de Salud Pública. Se solicitó su consentimiento informado a todos los pacientes. Los autores se comprometieron a respetar la confidencialidad de los datos de los pacientes y la fidelidad de los resultados encontrados, los cuales se utilizaron con fines estrictamente científicos y solo serán divulgados en eventos o publicaciones médicas.
RESULTADOS
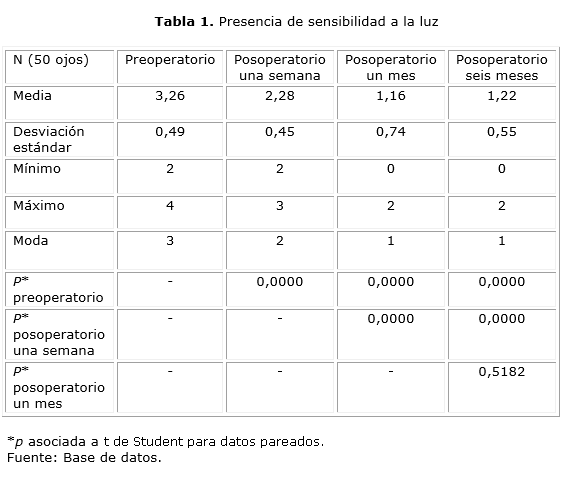
El 33,3 % de los pacientes se encontraban entre 60 y 74 años de edad, seguidos de los mayores de 75 años (26,7 %). Predominó el sexo femenino con el 57,8 %. Los diagnósticos preoperatorios más frecuentes fueron la queratopatía bullosa pseudofáquica (35,5 %), el rechazo inmunológico y el queratocono (22,2 %), como se muestra en la tabla 1.
La densidad celular media de la córnea en Banco de ojos fue de 2 574 cel/mm2. En la evaluación posoperatoria encontramos una densidad celular media a los 6 meses de 2 315 cel/mm2 y a 12 meses fue de 1 999 cel/mm2. El promedio de pérdida celular a los 6 meses fue de 259 cel/mm2 y de 587 cel/mm2 a los 12 meses, lo que corresponde con el 10,1 y el 22,8 % de pérdida celular respectivamente (tabla 2).
A los 12 meses de la queratoplastia encontramos predominio del astigmatismo oblicuo con un 61,5 %, seguido del astigmatismo contra la regla en el 20,5 % y el astigmatismo irregular con 15,4 % (tabla 3). La media del cilindro queratométrico medido por topografía corneal fue de 5,96, con un rango de 1,16 a 11,20 y una desviación estándar de 2,11. El cilindro queratométrico, medido por topografía, correspondió en el 48,7 % de los pacientes al rango entre 3 y 6 dioptrías, seguido de más de 6 dioptrías con 46,2 %.
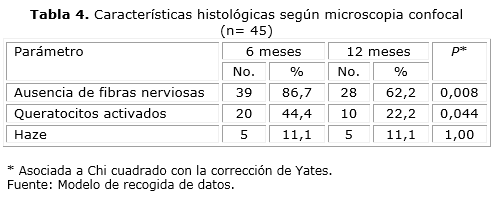
Observamos ausencia de fibras nerviosas en el 86,7 % de los casos a los 6 meses de la cirugía y en el 62,2 % a los 12 meses. En cuanto a la presencia de queratocitos activados, se encontraron en el 44,4 y 22,2 % de los casos a los 6 y 12 meses de la cirugía, respectivamente. La presencia de haze fue observada en el 11,1 % de los casos a los 6 y 12 meses de la cirugía, respectivamente. La ausencia de fibras nerviosas y la presencia de queratocitos activados fueron estadísticamente significativas (tabla 4).
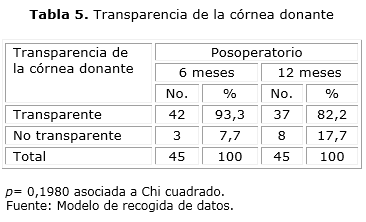
La córnea donante se encontraba transparente a los 6 meses en el 93,3 % de los casos y en el 82,2 % a los 12 meses. Con injerto no transparente encontramos un 7,7 % a los 6 meses y en el 13,3 % a los 12 meses de la cirugía (tabla 5).
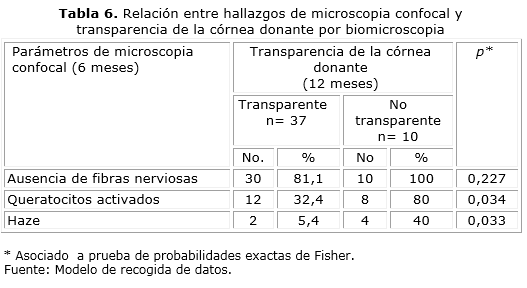
Al relacionar los hallazgos histológicos por microscopia confocal a los 6 meses de la cirugía con el estado de transparencia de la córnea donante a los 12 meses encontramos ausencia de fibras nerviosas en el 100 % de las córneas no transparentes, así como en el 81,1 % de las córneas transparentes. La presencia de queratocitos activados se constató en el 32,4 % de las córneas transparentes y en el 80 % de las córneas no transparentes. El haze se observó en el 40 % de los pacientes con córneas no transparentes y en el 5,4 % en las transparentes (tabla 6). La presencia de queratocitos activados y haze fue estadísticamente significativa.
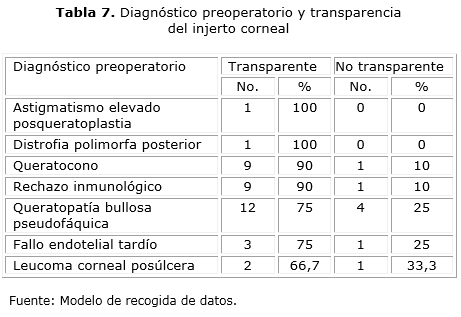
En cuanto al diagnóstico preoperatorio y la transparencia del injerto a los 12 meses, encontramos con injerto transparente el 100 % de los pacientes con distrofia polimorfa posterior descompensada y astigmatismo elevado posqueratoplastia; el 90 % de los pacientes con diagnóstico de queratocono y con injertos con rechazo inmunológico previo y 75 % de los fallos endoteliales tardíos y de las queratopatías bullosas pseudofáquicas, así como el 66,7 % de los leucomas corneales posúlcera. Con injerto no transparente, el 33,3 % de los pacientes presentaban leucoma corneal posúlcera; el 25 % fallo endotelial tardío y queratopatía bullosa pseudofáquica y el 10 % rechazo inmunológico previo y queratocono (tabla 7).
En este estudio, 18 pacientes desarrollaron complicaciones, y en dos casos se observó la presencia de más de una complicación (tabla 8). El glaucoma secundario fue el más frecuente con 33,3 %, seguido de úlcera corneal bacteriana, fallo secundario inmunológico (22,2 %) y defecto epitelial persistente (16,7 %).
Al relacionar la transparencia del injerto con la presencia de complicaciones encontramos que el injerto corneal se mantuvo transparente en presencia de úlcera corneal viral, endoftalmitis aguda posquirúrgica, glaucoma primario de ángulo abierto descompensado (100 %) y glaucoma secundario (83,3 %). El defecto epitelial (66,9 %) y la úlcera corneal bacteriana (100 %) fueron las complicaciones que provocaron pérdida de transparencia del injerto. El rechazo inmunológico se observó en igual cantidad de pacientes con injerto transparente y no transparente (tabla 9).
DISCUSIÓN
En este estudio predominaron los pacientes del sexo femenino y las edades superiores a 64 años de edad. Entre los diagnósticos preoperatorios más frecuentes encontramos la queratopatía bullosa pseudofáquica, seguida por el rechazo inmunológico y el queratocono. López Gallego,2 en Nicaragua, encontró que el grupo de edad más frecuente fue el de 56 a 75 años y predominó el sexo masculino. En el estudio del perfil clínico y quirúrgico de la queratoplastia penetrante, realizado en Perú, se encontró que la media de la edad fue 51,7 ± 20,1 años y las indicaciones más frecuentes fueron la queratopatía bullosa, el queratocono, el rechazo a la queratoplastia y los leucomas corneales.1 Orts Vila y otros4 encontraron que la indicación, en orden de frecuencia, fue el rechazo inmunológico, el queratocono y la queratopatía bullosa. En un estudio cubano,3 las patologías más frecuentes fueron la queratopatía bullosa, el leucoma corneal posúlcera, el queratocono y el rechazo inmunológico.
El mínimo valor de densidad celular endotelial para la córnea donadora debe ser mayor de 1 600 cel/mm2, pero teniendo en cuenta el proceso degenerativo por la edad y el trauma quirúrgico, así como los posibles episodios de rechazo, la densidad celular de la córnea donante debe oscilar entre 2 000 y 2 500 cel/mm2.5
En nuestro estudio, la media de densidad celular endotelial en Banco de ojos fue de 2 574 cel/mm2. El endotelio del injerto corneal penetrante presenta menor densidad celular, mayor pleomorfismo, aumento del tamaño celular y presencia ocasional de nichos acelulares. Durante el primer año tras el trasplante se produce una pérdida celular muy variable entre pacientes. El principal determinante es el número de células del botón corneal prequeratoplastia, influido por el tiempo muerte-enucleación, el posible traumatismo durante la obtención de la córnea y las patologías previas del donante. Una vez realizada la queratoplastia, juegan un papel fundamental los factores propios del huésped, así como las complicaciones postoperatorias.4
La pérdida de células endoteliales ocurre rápidamente durante el primer año posoperatorio, seguido de un período en el cual la densidad celular se restablece y se recupera la hexagonalidad en 5 años. Algunos autores refieren que el restablecimiento se logra a los 2, 3 o 4 años.5
Los resultados de este estudio reflejan una densidad celular media a los 6 meses superior a 2 000 cel/mm2 y a los 12 meses de la cirugía, de 1 999 cel/mm2. El promedio de pérdida celular de 587,3 cel/mm2. La densidad celular endotelial a los 12 meses correspondía a un 22,4 % de pérdida celular.
Bourne y otros6 reportaron en un estudio de cohorte una pérdida de células endoteliales de 7,8 % por año, y concluyeron que 5 a 10 años después de la queratoplastia penetrante, la pérdida anual de células endoteliales era siete veces mayor a lo normal. Orts y otros4 reportan en su estudio una densidad celular de 1 889 cel/mm2 al año de la cirugía, lo que representa una pérdida del 35,26 % (± 21), cifra superior a la encontrada en este estudio.
El astigmatismo posqueratoplastia continúa siendo la causa más importante de la mala calidad visual en los pacientes operados de queratoplastia. El promedio de astigmatismo posqueratoplastia varía entre 4 y 5 dioptrías. Existen numerosos factores que influyen: astigmatismo de la córnea donante, probabilidad de ectasia del donante, corte en la trepanación córnea donante-receptora, diámetro del trépano utilizado, el alineamiento de los bordes de la herida, la técnica de sutura, el grado de tensión y largo de esta (se considera óptimo 1,5 mm de longitud). Los exámenes topográficos en serie después de una queratoplastia penetrante revelan grandes cambios de configuración durante los primeros meses, los cuales permanecen estables hasta la remoción de la sutura. 7 El patrón topográfico más frecuente en nuestro estudio fue el astigmatismo oblicuo y el astigmatismo contra la regla. En los estudios revisados no encontramos referencia a este aspecto. El astigmatismo (menor o igual a 5 dioptrías) se puede corregir con cristales o lentes de contacto. Las opciones para corrección del astigmatismo superior a 5 dioptrías pueden ser la sustitución de puntos de sutura en el meridiano más plano, la remoción selectiva de suturas en el meridiano más curvo y las incisiones relajantes en la cicatriz. Otras opciones son la queratectomía fotorrefractiva, el LASIK y el implante de anillos intraestromales y en algunos casos puede ser necesario el retrasplante corneal.7 Nuestro cilindro queratométrico medio fue de 5,96 y predominó el rango entre 3 y 6 dioptrías, lo que coincide con los resultados de Escalona y otros3 y Quezada Baltodano.1
En la microscopia confocal observamos, en la mayoría de las córneas trasplantadas, pérdida de la continuidad de los nervios corneales, ausencia de fibras nerviosas, y disminución y activación de queratocitos,8,9 resultados que coinciden con los nuestros. Cuando se relacionaron los hallazgos de la microscopia confocal con el estado de transparencia del injerto, encontramos ausencia de fibras nerviosas en todos los casos de córnea no transparente y en la gran mayoría de las córneas transparentes. Sin embargo, la presencia de queratocitos activados y de haze en las córneas no transparentes resultó significativa.
En modelos animales se ha descrito que el aumento de queratocitos activados mantiene relación con la respuesta a la cicatrización y estimula la apoptosis de estas células, lo que condiciona un mal pronóstico para el trasplante8,9, por lo que consideramos que la presencia de queratocitos activados a los 6 meses de la cirugía puede ser un factor pronóstico para el rechazo al trasplante. Por otro lado, el haze se asocia generalmente a la presencia de edema y a cierto grado de fibrosis estromal en respuesta a este primero, por lo que planteamos que en nuestro estudio su presencia responde a fallo endotelial paulatino, que ha llegado a afectar el estroma corneal, y a fibrosis como consecuencia de procesos inflamatorios o infecciosos a este nivel.
En relación con la queratoplastia penetrante, se conoce que la reinervación y la cantidad de los queratocitos juegan un importante papel para mantener la transparencia corneal después del trasplante y un mejor éxito posterior.9 Nuestros resultados coinciden con el estudio de Gómez Castillo y otros,9 que reporta que el 82 % de los pacientes no poseían plexos nerviosos en el primer año de la cirugía. Otros estudios concluyen que la densidad de queratocitos y de fibras nerviosas subbasales después de queratoplastia penetrante es significativamente menor que en córneas normales. No se ha observado regeneración importante de haces de fibras nerviosas, incluso en queratoplastias penetrantes después de 30 años de seguimiento. En pacientes en los que se ha encontrado regeneración del plexo subbasal, la morfología de las fibras nerviosas se encuentra marcadamente alterada, y se observan nervios de aspecto tortuoso y desordenado con reducción del patrón de las ramas y de la longitud del nervio. En injertos opacos se ha encontrado presencia de haze, relacionado con el edema estromal y los queratocitos activados.10
La mayoría de los pacientes presentaban injerto corneal transparente al año de la cirugía, resultado que coincidió con la literatura revisada,1,3 donde se reporta que el éxito de la queratoplastia penetrante está avalado por la supervivencia del injerto y se considera que en esta técnica quirúrgica el pronóstico de supervivencia del injerto es del 90 %. No encontramos relación entre el diagnóstico preoperatorio y la transparencia del injerto corneal a los 12 meses. La pérdida de transparencia del injerto en pacientes con antecedentes de úlcera corneal se justifica por la presencia de vascularización y las complicaciones propias de la inflamación intraocular. Se reporta que la queratopatía bullosa pseudofáquica representa la segunda patología en frecuencia entre los casos de rechazo al trasplante con pérdida de la transparencia del injerto con un 30 %, por lo que considera a esta patología como uno de los factores de riesgo importantes para trasplante de córnea, al igual que la vascularización corneal. Varios autores reportan resultados similares a nuestro estudio en cuanto a la transparencia del injerto;1,3 sin embargo, son muy escasos los estudios comparativos de transparencia del injerto y de diagnóstico preoperatorio.
Las complicaciones posquirúrgicas más frecuentes fueron el glaucoma secundario, la úlcera corneal bacteriana y el fallo secundario inmunológico. El injerto corneal se mantuvo transparente en presencia de la úlcera corneal viral, la endoftalmitis aguda posquirúrgica, el glaucoma primario de ángulo abierto descompensado y el glaucoma secundario. Consideramos necesario resaltar al paciente con diagnóstico de endoftalmitis aguda posqueratoplastia, quien acudió con sintomatología a las 72 horas de la cirugía. Se realizó toma de muestra de humor acuoso y vítreo para cultivo, donde se obtuvo el crecimiento de Estafilococo aureus. Se realizó vitrectomía en las 24 horas iniciales al diagnóstico y se mantuvo transparente el injerto corneal con buena agudeza visual corregida. En el paciente con glaucoma primario descompensado se logró control mediante reajuste del tratamiento médico y a los casos con glaucoma secundario se les controló con tratamiento médico y/o quirúrgico.
El glaucoma posqueratoplastia es una complicación devastadora para el injerto corneal. No solo es difícil su diagnóstico, sino también su manejo, por lo que puede comprometer seriamente la supervivencia del injerto por daño endotelial secundario y daño del nervio óptico, con la consecuente afectación de la función visual. Se plantea una distribución bimodal de la elevación de la presión intraocular tras queratoplastia penetrante, una temprana que ocurre en los primeros días de la cirugía, y otro más tardío después de los tres meses. Se consideran de mayor riesgo las cirugías combinadas. El diagnóstico del glaucoma posqueratoplastia es difícil de realizar por las características de la córnea posqueratoplastia: irregularidad de la superficie corneal, astigmatismo y presencia de edema en estos casos.11
Un paciente desarrolló una úlcera corneal viral sin antecedentes previos a la queratoplastia, que evolucionó satisfactoriamente con tratamiento antiviral. La infección viral herpética puede presentarse semanas o meses después de la queratoplastia, como una pequeña zona irregular, coloreada cerca de la cicatriz y que se extiende al injerto, lo que hace que se confunda erróneamente con un defecto epitelial.12 El defecto epitelial y la úlcera corneal bacteriana provocaron pérdida de transparencia del injerto. El rechazo inmunológico se observó en igual cantidad de pacientes con injerto transparente y no transparente.
Se reporta un 43 % de casos con defecto epitelial persistente, seguidos del 24 % con rechazo al trasplante.2 Otros autores1,3 encontraron en orden de frecuencia la presencia de alteraciones epiteliales, glaucoma, rechazo al injerto y úlcera del injerto. El defecto epitelial se relaciona frecuentemente con un defecto de producción del epitelio a nivel del limbo del receptor, o con las malas condiciones del injerto, que impiden la adherencia del epitelio del receptor a su superficie. Eventualmente se puede reemplazar el epitelio de la córnea donadora por la del huésped. La presencia de un defecto epitelial durante la primera semana posquirúrgica con producción normal de lágrimas es sugestivo de toxicidad medicamentosa tópica, por lo que se sugiere el empleo de medicamentos sin preservo y la indicación de lubricantes corneales.13
La queratitis infecciosa posqueratoplastia es una de las causas más importantes de fracaso del injerto corneal, lo que conlleva la disminución de la visión. Se reporta que la mayoría de las infecciones se producen en el primer año de la cirugía. Las infecciones del injerto se presentan en la unión huésped-injerto, favorecido por factores predisponentes de la córnea receptora tales como la vascularización y los defectos epiteliales. La inmunosupresión localizada en la córnea que provocan las dosis de esteroides tópicos juega un papel importante en la aparición de infiltrado corneal.12
El rechazo inmunológico en nuestro estudio ocupó el tercer lugar entre las complicaciones reportadas. Sin embargo, en la actualidad se considera la primera causa de fracaso de un trasplante de córnea. Más de un 30 % de los trasplantes de córnea tienen al menos un episodio de rechazo y un 5-7 % de todos ellos fracasan por esta causa. 13 Estudios sobre rechazo en queratoplastia penetrante reportan el rechazo endotelial entre 14 y 17 % como la complicación más común en esta cirugía.14,15
Se concluye que la córnea posqueratoplastia presenta una pérdida celular endotelial anual de 22,8 %, astigmatismo oblicuo, cilindro queratométrico entre 3-6 dioptrías, presencia de queratocitos activados y haze corneal como factores pronósticos de pérdida de transparencia del injerto. El leucoma corneal posúlcera, la queratopatía bullosa como diagnóstico preoperatorio y la úlcera corneal bacteriana como complicaciones provocan pérdida de transparencia del injerto. Afortunadamente, muchos de los episodios de rechazo responden adecuadamente al tratamiento, siempre que su diagnóstico sea oportuno.
Conflicto de intereses
Los autores declaran que no existe conflicto de intereses en el presente artículo.
REFERENCIAS BIBLIOGRÁFICAS
1. Quezada Baltodano FP. Perfil clínico quirúrgico de la queratoplastia penetrante en el Instituto Oftalmo Salud. Casuística. Junio 2002 a junio 2005. Perú: Tesis para optar por el título de Especialista en Oftalmología; 2009.
2. López Gallego M. Comportamiento clínico de los casos de queratoplastia penetrante realizados en el Centro Nacional de Oftalmología de enero de 2006 a enero de 2008 (Tesis para optar por título de Especialista de Oftalmología). Universidad Nacional Autónoma de Nicaragua; 2008.
3. Escalona Leyva E, Jareño Ochoa M, López Hernández S, Castillo Pérez AC, Pérez Parra Z, Rodríguez de Paz U. Comportamiento de los trasplantes de córnea en el Instituto Cubano de Oftalmología “Ramón Pando Ferrer” (enero-noviembre de 2006). Rev Cubana Oftalmol. 2009,22(Sup):247-57.
4. Orts Vila P, Calatayud Hernández M, Rodrigo Auría F, Belmonte Martínez J. Biomicroscopia especular en córneas donantes antes de la queratoplastia y tras un año de seguimiento. Microcir Ocul. 2004;12(1):5-8.
5. Covarrubias Espinosa EP, Ozorno Zarate J, Naranjo Tackman R. Factores pronósticos y determinación de pérdida de células endoteliales en queratoplastia penetrante. Rev Mex Oftalmol. 2006;80(3):145-9.
6. Bourne WM. Cellular changes in transplanted human corneas. Cornea. 2001;20(6):560-9.
7. Ang M, Mehta JS, Anshu A, Kiat H, Htoon HM, Tan D. Endothelial cell counts after Descemet’s stripping automated endothelial keratoplasty versus penetrating keratoplasty in Asian eyes. Clin Ophthalmol. 2012;6:537-44.
8. Pacheco del Valle C, Baca Lozano O, Velasco Ramos R. Reinervación corneal y dinámica de queratocitos posterior a queratoplastia penetrante. Reporte de casos. Rev Mex Oftalmol. 2008;82(4):263-6.
9. Gómez Castillo Z, López Hernández S, Castillo Pérez AC, Rodríguez de Paz U, Pérez Parra Z, Escalona Leiva E. Microscopia confocal en operados de queratoplastia perforante. Rev Cubana Oftalmol. 2009 [citado 28 de diciembre de 2016];22(1). Disponible en: http://scielo.sld.cu/scielo.php?script=sci_arttext&pid=S0864-21762009000100006&lng=es
10. Pérez Parra Z, Rodríguez de Paz U, Noriega Martínez JL. Queratoplastia penetrante y lamelar anterior. En: Benítez Merino MC, Capote Cabrera A, Río Torres M, Silva Hernández JR. La Habana: Microscopia confocal de la córnea. Ilustraciones. Editorial Ciencias Médicas; 2013. p. 61-8.
11. Yildirim N, Gursoy H, Sahin A, Ozer A, Colak E. Glaucoma after penetrating keratoplasty: incidence, risk factors and management. J Ophthalmol. 2011: 9512-94.
12. Camarena Hernández J, Graue E, Chirinos P, Navas A, Ramírez A, Vizuet L, et al. Queratitis infecciosas: tendencias microbiológicas y sensibilidad a antibióticos. Primer reporte anual del Grupo de Estudio de Microbiología Ocular del Instituto de Oftalmología "Conde de Valenciana". Rev Mex Oftalmol. 2012;86(4):213-22.
13. Cremona F. Factores predisponentes, diagnóstico y manejo del rechazo del trasplante de córnea. Estonian University of Life Sciences; 2010.
14. Omar N, Bou Chacra CT, Tabbara KF. Outcome of corneal transplantation in a private institution in Saudi Arabia. Clin Ophthalmol. 2013 [citado 10 de noviembre de 2014]; Disponible en: http://dx.doi.org/10.2147/OPTH.S43719
15. Wagoner MD, Gonnah ES, Al-Towerki AE; King Khaled Eye Specialist Hospital Cornea Transplant Study Group. Outcome of primary adult penetrating keratoplasty in a Saudi Arabian population. Cornea. 2009;28(8):882-90.
Recibido: 27 de enero de 2017.
Aprobado: 27 de marzo de 2017.
Zaadia Pérez Parra. Instituto Cubano de Oftalmología "Ramón Pando Ferrer". Ave. 76 No. 3104 entre 31 y 41 Marianao, La Habana, Cuba. Correo electrónico: zaadia.perez@infomed.sld.cu