Introducción
Los implantes cocleares (IC) son el tratamiento estándar cuando existe una hipoacusia sensorineural bilateral (HSNB) severa o profunda sin ganancia funcional con prótesis auditiva. Con los IC estos niños tienen el potencial para desarrollar habilidades auditivas y la posibilidad de adquirir el lenguaje oral.
Los primeros IC en Cuba se realizaron en el año 1997. Sin embargo, no fue hasta el año 2005 que se crea el Programa Cubano de Implantes Cocleares (PCIC) para niños sordos y sordociegos, 1,2 a partir de los progresos tecnológicos en los IC y los resultados en la rehabilitación auditiva en los sujetos implantados en el mundo, no obstante, ciertas condiciones médicas aún representan contraindicaciones, por ejemplo, la ausencia de nervio auditivo. 3,4
El PCIC dirigido en primer lugar a niños con discapacidad múltiple, priorizados los niños con sordoceguera, se inició el 7 de febrero del 2005, ampliándose el número de especialidades del grupo para lograr realizar un trabajo médico asistencial y de investigación más integral en beneficio de los niños. 2
La sordoceguera es una discapacidad única causada por una combinación de deficiencia auditiva y visual. No se trata de la sumatoria de la sordera más la ceguera, sino que es una discapacidad múltiple con características propias, que implica una limitación en los sentidos de la distancia (visión y audición), donde no es necesario tener una pérdida total de los dos sentidos. 5
La sordoceguera en ocasiones también es referida como pérdida sensorial dual (PSD). En la investigación se adopta el término PSD como expresión de pérdida combinada de visión y audición, ya que abarca el amplio espectro de deficiencia de los dos sentidos sensoriales principales, que puede ir desde una pérdida leve de audición y visión hasta la sordoceguera total, 6 que impacta de forma significativa en la calidad de vida de las personas afectadas.
La sordoceguera constituye un grave problema de salud y también social a nivel mundial. Sin embargo, muchas de las consecuencias negativas pueden minimizarse con un diagnóstico e intervención temprana. 7,8 No se trata de una enfermedad, aunque muchas enfermedades y síndromes pueden ser causantes de PSD. En un estudio nacional de la discapacidad realizado en Cuba, 9 entre los años 2001 y 2003, se estudiaron 366 864 personas para una tasa de prevalencia de 3,26 por cada 100 habitantes. Como parte de dicho estudio se identificaron 214 niños con trastornos auditivos y visuales, de los cuales 102 clasificaron como sordociegos. En la actualidad en Cuba ya están identificados más de 3 800 personas con PSD. 10
El trabajo del PCIC ha representado un reto, en tanto no solo se trata de la asimilación tecnológica de los progresos que tienen lugar en la tecnología y la cirugía del IC, sino también, en la asimilación de información sobre la PSD y el difícil trabajo de rehabilitación de estos niños, diferente al que se realiza a niños sordos sin enfermedades asociadas. Vale destacar que en el mundo la experiencia en el tratamiento de niños con PSD con IC es mucho menor que en niños sordos. 11,12,13 Asumir este programa fue un reto para profesionales del PCI, se enfrentó una etapa de adquisición y a la vez de generación de conocimientos, donde el objetivo del trabajo fue describir los resultados del PCIC en el trabajo con niños con PSD.
Métodos
De un total de 248 niños con pérdida auditiva evaluados en el PCIC desde febrero de 2005 a marzo de 2013 que resultaron candidatos a IC, en el estudio retrospectivo, descriptivo quedaron incluidos solo los niños con PSD (n=27). Estos niños fueron evaluados por los especialistas del PCIC en el Hospital Pediátrico Borrás-Marfán de La Habana a través de exámenes clínicos y complementarios de obligatoria realización para definir la idoneidad del niño para recibir un IC. 14
La severidad de la PSD fue evaluada clínicamente por médicos especialistas en Audiología/Otorrinolaringología (ORL) y Oftalmología, apoyada por técnicas de potenciales evocados auditivos de estado estable (PEAee). Mientras que la caracterización de la pérdida visual se hizo según los resultados obtenidos de la evaluación oftalmológica, en especial la gradación de la magnitud del daño visual fue considerada al tener en cuenta la evaluación de la agudeza visual, la visión binocular y la campimetría (esta última realizada solo en los niños que cooperaron al examen). La evaluación se complementó con la valoración de especialistas en Neuropediatría, Genética, Logofoniatría y Psicología. Estos últimos evaluaron el estado de los procesos cognoscitivos y con ello las potencialidades de cada niño para ser rehabilitado, a la vez que se precisó la presencia de enfermedad asociada a la pérdida sensorial.
Análisis estadístico:
Los datos generales y clínico-quirúrgicos de cada niño tomados de las historias clínicas y base de datos del PCIC, así como los resultados de los estudios de imágenes de tomografía computarizada (TC) e imagen de resonancia magnética (IRM) de oídos, fueron llevados a una base de datos para el análisis estadístico. El procesamiento de los datos se realizó con el programa STATISTICA 8. El análisis descriptivo de cada variable fue llevado a cabo, se utilizaron los estadígrafos: frecuencia observada, media, desviación típica y gráficos de dispersión.
Por último, se incluyeron de forma ilustrativa resultados del proyecto de investigación sobre neuroplasticidad que se desarrolla en el marco del trabajo del PCIC evaluada con potencial evocado somatosensorial (PES-N20), donde se realizó un análisis con prueba de permutaciones con el estadígrafo t-Student, para ver la descripción metodológica consultar la publicación de Charroó-Ruíz L et al. 15
Resultados
La Tabla 1 resume las características de la totalidad de niños con PSD que resultaron candidatos a IC (n=27) y en consecuencia fueron sometidos a cirugía para recibir un IC entre febrero de 2005 y marzo de 2013. Se destaca que solo seis de estos niños presentaron una enfermedad asociada. Además, se tuvo en consideración las principales enfermedades y agentes causales de la PSD, con predominio de múltiples factores pre/peri-natales (n=12, 44 %) y el síndrome de Usher (n=7, 26 %), las que de conjunto representan el 70 % de los antecedentes personal en relación con la discapacidad sensorial dual en los niños estudiados. Por el contrario, solo en el 11,1 % no fue posible precisar antecedes personales positivos. Los estudios de imágenes (TC y IRM) se caracterizaron por la no presencia de malformaciones del oído. Mientras que según el momento de ocurrencia de la pérdida sensorial en 24 niños la pérdida auditiva fue pre-locutiva y en tres fue post-locutiva (Tabla 1).
Tabla 1 Características demográficas, clínicas, quirúrgicas y de imagen de los niños con PSD

Fuente: Datos tomados de la base de datos del PCIC y de las historias clínicas.
Todos los niños con PSD presentaron hipoacusia sensorineural bilateral (HSNB) profunda a severa caracterizada en función del grado de severidad de la pérdida auditiva, la cual estuvo dada por restos auditivos a muy altas intensidades de estimulación (90-110 dB) hasta ausencia de respuesta audiométrica en las frecuencias de 0.5, 1, 2 y 4 kHz. A partir de los hallazgos de la evaluación oftalmológica, la muestra estuvo representada por dos niños con ceguera total (7,4 %), mientras que los restantes 25 pacientes tenían un grado de visión, por lo que clasifican como baja visión y muy baja visión. El oído derecho fue el más implantado (77,8 %), con implantación unilateral en el 100 % de los niños con PSD, sin tener lugar la ocurrencia de complicaciones quirúrgicas. Mientras que al analizar la edad de implantación se tiene que el 48 % fue implantado antes de los siete años de edad.
La Figura 1 ilustra los hallazgos característicos de los niños con PSD en la confirmación diagnóstica y caracterización de la HSNB realizada a través de la electroaudiometría obtenida a partir de los registro del PEAee, así como el estudio de imagen realizado a uno de los niños del PCIC, lo cual de conjunto con las evidencias que aportan las restantes evaluaciones realizadas por los miembros del equipo multidisciplinario del PCIC sustentaron que los niños fueran considerados con criterios a IC (Figura 1).

Figura 1 La electroaudiometría obtenida con PEAee y estudio de imagen de oído que se realiza a los niños con PSD en la evaluación para efectuar un IC. Note que solo existe repuesta a la frecuencia de 1000 en ambos oídos a la intensidad de 110 dB. (Imagen de los autores).
Fuente: Datos tomados de la base de datos del PCIC y de las historias clínicas.
La Figura 2 muestra el comportamiento de las intervenciones quirúrgicas para IC. En el año 2005 tuvo lugar el mayor número de cirugías de niños con PSD. Desde entonces cada año se ha continuado detectando e implantado niños con PSD, al encontrarse estos niños distribuidos en todas las provincias del país. De enero 2012 a marzo 2013 no se implantaron niños con PSD (Figura 2).
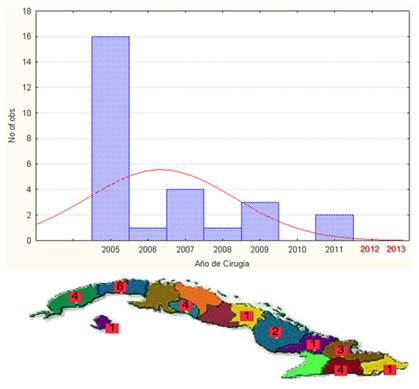
Figura 2 Comportamiento de las intervenciones quirúrgicas para IC por año y distribución por provincia de los niños con PSD implantados en Cuba de Febrero de 2005 a Marzo de 2013.
Fuente: Datos tomados de la base de datos del PCIC y de las historias clínicas.
Por otra parte, en la Figura 3 se ilustran los resultados de la investigación sobre neuroplasticidad (reorganización cortical) a través de los mapas de la distribución topográfica del PES-N20 en niños con PSD. El PES-N20 se localizó con máximos valores de energía en la región centro-parietal del hemisferio contralateral al nervio estimulado al observar los mapas grupales. Nótese que hay una expansión del PES-N20 en los niños con PSD en el hemisferio izquierdo, donde la activación también está presente en región temporal y occipital. La prueba de Permutaciones admitió comparar, a través del estadígrafo t-Student, la distribución topográfica del PES-N20 entre los niños con PSD y el patrón de normalidad (controles) del laboratorio del Hospital Pediátrico Borrás-Marfán. La distribución topográfica de dicha respuesta resultó diferente, estadísticamente significativa, en las derivaciones central, parietal, occipital y temporal (C3, P3, O1, T3) para la respuesta evocada en el hemisferio izquierdo tras la estimulación del nervio mediano derecho, con una probabilidad global de 0,02. Mientras que la respuesta evocada en el hemisferio derecho no fue estadísticamente significativa en ninguno de los sitios de registro (probabilidad global de 0,72) (Figura 3).
Figura 3 Mapas grupales que muestran el comportamiento del PESS-N20 en niños con PSD. En el hemisferio izquierdo existe una expansión, mayor activación, estadísticamente significativa en los sitios de registro C3, P3, T3 y O1, en niños con PSD comparado con la norma.
Fuente: Datos tomados de la base de datos y del proyecto de investigación de neuroplasticidad del PCIC.
Por último, cabe destacar que casi la totalidad de los niños con PSD implantados en el PCIC (26/27) hacen uso del IC de forma regular, al mostrar progresos en la comunicación, reflejado en los resultados escolares y la calidad de vida de los niños y familia, lo cual será objeto de descripción y análisis en futura publicación de nuestro grupo.
Discusión
El trabajo realizado en el PCIC para niños con PSD se destaca por los siguientes aspectos significativos: un gran número de niños con PSD han sido implantados en el marco de trabajo del PCIC, ofrece cobertura a todas las provincias del país, el PCIC integra profesionales de la salud, educación e investigación, con servicios gratuitos, cubiertos por el sistema de salud cubano. Estos últimos apoyan el trabajo médico-asistencial a niño con PSD pero, además, resalta el aporte científico, generación de nuevo conocimiento sobre neuroplasticidad, al describir hallazgos de reorganización cortical en niños con PSD a partir del estudio de PES.
De la variedad de modelos de IC que existen en el mercado, en la primera fase del PCIC (año 2005) se colocaron IC de Advanced Bionics en los niños con PSD y años después (2007) se introdujo también el uso de IC modelos Cochlear. Sin embargo, independientemente del tipo de IC, todos tienen un mismo fundamento: proporcionan sensaciones auditivas al estimular el nervio auditivo.
La información acústica es indispensable para la inserción escolar y social del niño, en especial si la HSNB tiene lugar en los primeros años de vida, antes de concluir el período crítico de máxima capacidad de neuroplasticidad del sistema auditivo central y así lograr el mejor desarrollo lingüístico del niño. 16
La inmensa mayoría de los sujetos con sordoceguera no tienen una pérdida total de ambos sentidos, solo un 10 %. 17 Similar comportamiento fue observado en los 27 pacientes implantados entre febrero de 2005 y marzo de 2013, donde solo dos niños tenían sordoceguera total para un 7,4 %. También, las enfermedades y agentes causales de PSD reportadas en esta muestra son las descritas por otros autores. 5,17,18
Reportes clínicos indican que del 30 % al 40 % de los niños con déficits auditivos tienen una o más enfermedades asociadas a la sordera, donde son descritas más de 200 condiciones diferentes, 19 presentes con mayor frecuentes los trastornos motores, cognitivos, de atención, daño visual y Parálisis Cerebral entre otros. 20,21
Niños con tales condiciones muestran menores beneficios que los niños sordos sin otros problemas de salud, pues necesitan más tiempo y experiencia con el uso del IC para lograr progresos en el lenguaje oral. 22,23,24
Se conoce que la sordoceguera es más grave cuando la pérdida de la visión y la audición ocurre al nacer o durante los primeros años de vida, aspecto que predomina en la muestra de niños con PSD evaluados, donde la pérdida auditiva fue de manera principal pre-locutiva, sin embargo, muchas consecuencias resultantes de tal discapacidad se puede minimizar a través del diagnóstico e intervención temprana. 7,8
Los niños con PSD que han sido implantados en el PCIC desde febrero de 2005 a marzo de 2013 y que reciben rehabilitación muestran progresos (26/27 niños). El único niño que interrumpió la rehabilitación auditiva post-IC fue por falla en la parte interna del IC, donde fue decisión de los padres el no reimplantar a pesar de que el niño mostraba mejoría en la calidad de vida, en lo especial si se considera que se trata de un niño sordociego total desde el nacimiento, que no tenía previo al IC un patrón de comunicación establecido. Antes del fallo de la parte interna del implante el niño ya había iniciado respuestas emocionales positivas con la familia, como resultado de la rehabilitación auditiva intensa recibida, asociada a otras terapias físicas, como la equinoterapia. Especialistas del PCIC estuvieron en contacto con los padres, pero la decisión final de los padres de no reimplantar fue respetada, en cumplimiento del consentimiento informado firmado, donde los padres son los que autorizan o no la realización de cada proceder médico a su niño.
Pocos estudios publicados como el de Wiley S et al. 25 enfocan a los resultados de la percepción de la palabra y la calidad de vida con PSD tras recibir el IC. Ahora, en la muestra queda por concluir el estudio en curso de la evaluación post-IC de los niños en un análisis de los resultados de la rehabilitación y calidad de vida, así como la reorganización cortical pre- versus post-IC, aunque de dicho estudio se brinda un esbozo de los hallazgos obtenidos.
Se plantea que el éxito y los beneficios del IC dependen entre otros factores del momento en el que tienen lugar la pérdida auditiva, la duración, exposición a la comunicación oral y el grado de reorganización cortical que exista. 26,27,28 En la medida en que las áreas cerebrales no dañadas (con entrada sensorial intacta) invadan (o se expandan) hacia las áreas auditivas y el implante resultaría menos útil. 16
Con la disponibilidad de evidencias de neuroplasticidad pre-IC en niños con PSD será posible correlacionarlas con los resultados de la rehabilitación auditiva post-IC. Será posible la evaluación pre- versus post-IC ya que el PES-N20 puede ser realizado después de implantados los niños, no así resonancia magnética, cuyo uso queda rigurosamente controlado una vez colocada la parte interna del IC. 29,30
Las evidencias de neuroplasticidad deben contribuir a disponer de una medida objetiva predictora de los resultados del IC en niños con PSD, aspecto importante, si se toma en consideración que no existen criterios bien establecidos para la selección de niños sordos con enfermedades asociadas tributarios de IC. 15
En general, los artículos publicados sobre IC en sujetos con PSD, en particular los resultados de la evaluación post-IC, son blancos de limitaciones: resultan de muestras pequeñas con resultados heterogéneos. En este sentido, cabe señalar que la muestra de niños con PSD que ha recibido IC en el PCIC entre febrero de 2005 y marzo de 2013 para nada es pequeña si se considera que, por ejemplo, un artículo de revisión realizado por Dammeyer J y Ask Larsen F, 13 describen siete trabajos en sujetos con PSD cuya muestra entre todos los trabajos fue de 19 niños con tal discapacidad.
Conclusiones
Se ha logrado un trabajo sostenido en la evaluación de los niños con PSD, detectados y remitidos al PCIC desde la maternidad o el área de salud en el Programa de Pesquisaje Auditivo de Riesgo y Centros Auditivos Regionales, con lo cual ha sido posible eliminar la lista de espera para recibir un IC, donde se da cobertura a todas las provincias del país. Un aspecto distintivo de este programa es el estudio de neuroplasticidad pre-IC, con lo cual se dispone de un patrón de representación cortical somestésico que será útil para evaluar la reorganización cortical una vez que el lenguaje permita la comunicación a través de la palabra como resultado del aprovechamiento del uso del IC y la rehabilitación.














