Introducción
Entre las técnicas de precipitación se encuentran la inmunodifusión radial simple, la doble inmunodifusión y la inmunoelectroforesis (IEF).1 Esta última, combina la separación electroforética con la doble inmunodifusión por lo que permite primero la separación de las proteínas existentes según su carga y luego su identificación con anticuerpos específicos. La inmunoelectroforesis fue descrita por Grabar y Williams en 1953 y desde entonces ha tenido un amplio uso en la caracterización de muestras biológicas complejas.2,3
Los términos "antisuero" o "suero inmune" se utilizan comúnmente para referirse a un suero que contiene altas concentraciones de anticuerpos contra un antígeno dado, obtenido generalmente mediante un proceso de inmunización en humanos.4,5) Mientras, el término hiperinmune se reserva para sueros inmunes con altos títulos de anticuerpos obtenidos en animales mayores de otra especie.6,7)
En el Departamento de Inmunología del Instituto de Ciencias Básicas y Preclínicas “Victoria de Girón” se obtuvieron antisueros hiperinmunes por inmunizaciones de carneros con suero humano o IgA proveniente de calostro humano. Estos antisueros se consiguieron como parte de las investigaciones realizadas en el departamento para conformar las guías de actividades prácticas de la asignatura Sangre y Sistema Inmune del Plan D.8 Los primeros, deben contener anticuerpos contra las inmunoglobulinas mayores séricas (IgG, IgM e IgA); pero también contra la albúmina (proteína de mayor concentración sérica), así como contra otras proteínas menores, por lo que nos propusimos identificar la respuesta anti IgG, IgM e IgA humanas en el suero hiperinmune antitotal obtenido en carnero y determinar si existe respuesta anti IgM e IgG humanas en el suero anti IgA de calostro humano obtenido en carnero. La realización de este proyecto reporta beneficios sociales y económicos para la impartición de la docencia en pregrado y posgrado en el Departamento de Inmunología. Este suero hiperinmune antihumano puede utilizarse para el diagnóstico de discrasias de células plasmáticas y para su conjugación covalente a enzimas con el fin de emplearlo en técnicas como el ELISA importante para el trabajo de investigación del laboratorio. Por otro lado, esta investigación permitirá la reintroducción de la Inmunoelectroforesis en el trabajo de rutina del Departamento de Inmunología del Instituto de Ciencias Básicas y preclínicas “Victoria de Girón” y contar con Inmunodiagnosticadores económicos.
Los objetivos de esta investigación son identificar IgG, IgM e IgA en suero humano y determinar respuesta anti IgM humana en el antisuero anti IgA de calostro humano obtenido en carnero.
Material y Métodos
Se realizó un estudio observacional, descriptivo y transversal en el Instituto de Ciencias Básicas y Preclínicas “Victoria de Girón” de la Universidad de Ciencias Médicas de La Habana en el período de noviembre de 2017 a junio de 2018.
Muestras
Se trabajó con 1 mL de suero hiperinmune antitotal humano obtenido en carnero que se encontraba almacenado a -20°C en la seroteca del laboratorio. Se utilizó 1 mL de suero antitotal humano obtenido en caballo como suero control, facilitado por el Centro de Inmunoensayos. Se trabajó con muestras de suero de adultos sanos que se encontraban almacenadas en la Seroteca del laboratorio a -20°C de las cuales se conformó un pool a partir de 10 muestras.
Para la realización de la inmunoelectroforesis de suero humano normal se utilizó una placa de vidrio de 8 cm de largo por 6 cm de ancho; se dispensó una capa fina de agar de fijación a 3 % y se secó durante 5 minutos en horno a 80°C. Luego se dispensó agar noble a1,4 %, se perforaron siete pocillos en el centro de la placa y se añadieron en cada uno 5 µL de suero humano normal en dilución de 1:8 y se marcó el frente de migración con bromofenol azul. Se colocó la placa en cubeta de inmunoelectroforesis a la que se añadió previamente solución amortiguadora de Barbital; se conectó a la fuente de poder y se realizó la corrida electroforética durante 1 hora a temperatura de 22 °C, con un voltaje de 240 Volt y un amperaje de 20 mA.
A continuación se perforaron siete canales y se añadió 100 µL del antisuero correspondiente en cada uno y de los anticuerpos monovalentes, respectivamente.
Como control se empleó suero antitotal humano obtenido en caballo en dilución de 1:3; este antisuero es el estándar utilizado en el laboratorio de purificación de proteínas del Centro de Inmunoensayos donde se desarrolla habitualmente la técnica de inmunoelectroforesis como parte del proceso de control de calidad.9,10,11 El primer monoclonal empleado fue un anti IgG humana puro colocado en el tercer canal, que reconoce la IgG del suero al formar un arco grande, extendido hacia el cátodo y de base ancha.12,13,14
En el cuarto canal se enfrentó un monoclonal anti IgM humana puro a la muestra de suero humano sano. Por último, se enfrentó anti IgA humana puro y en dilución de 1:2 y 1:4 a partir del quinto canal y hasta el séptimo, respectivamente.
Para la realización de la inmunoelectroforesis de calostro humano se sigue igual procedimiento técnico que para suero humano. En todos los pocillos se adicionaron 5 µL de calostro humano en diferentes diluciones. Luego de la separación electroforética se adicionaron 100 µL en los primeros tres canales de anti IgA de calostro humano, seguidamente dos canales de anti IgG humana y en los dos últimos canales se adicionó anti IgM humana.
Posteriormente, se colocó la placa en cámara húmeda y se dejó difundir por 24 horas. Se procedió a lavar con agua destilada y solución salina fisiológica a 0,85 %. Luego se sumergió la placa en solución de tinción con azul de Coomassie durante 5 minutos, después se colocó en solución decolorante hasta que los arcos de precipitado se distinguieron con claridad del fondo de la placa, se dejó secar el gel a temperatura ambiente y se registraron los resultados. En esta investigación se tuvieron en consideración todas las normas éticas establecidas para este tipo de estudio.
Esta investigación no se realizó directamente en humanos o animales de experimentación. Se trabajó con muestras biológicas procedentes de la seroteca del Laboratorio del Departamento de Inmunología del ICBP “Victoria de Girón”, donde forman parte del trabajo habitual del personal del mismo. Se encuentran avaladas por consentimiento informado de todos los donantes voluntarios.
Resultados
En la figura 1 se muestra el resultado de la inmunoelectroforesis del suero humano normal teñida con Azul de Coomasie.
En el primer canal se empleó suero antitotal humano obtenido en caballo en dilución de 1:3 como control de la técnica. Este antisuero se enfrentó a la muestra biológica que se había separado previamente de acuerdo con su carga eléctrica. Como resultado se pueden observar los diferentes arcos de precipitado que se corresponden con las clases mayores de inmunoglobulinas (IgG, IgM e IgA) presentes en el suero humano, además de otras proteínas mayores del suero como la albúmina que se muestra en su forma clásica de bote con un desplazamiento hacia el polo positivo por presentar una carga neta negativa mayor que el resto de las proteínas séricas,2,3 pueden visualizarse también otros arcos correspondientes a otras fracciones proteicas.
En el segundo canal se enfrentó la muestra al suero hiperinmune antitotal humano obtenido en carnero. Se empleó en una dilución de 1:4 que fue la mejor dilución donde se observaron los inmunoprecipitados. Se distinguen con claridad los arcos correspondientes a las inmunoglobulinas mayores, los arcos de precipitado correspondientes a la IgG, IgM e IgA son anchos, destaca el arco de la IgG con su forma extendida desde el punto de partida y en dirección al cátodo. También se identifica la albúmina en su clásica forma de bote, está situada más anódicamente y presenta un arco más grande y difuso que el resto de las proteínas.1,3
Para lograr una identificación más completa de los anticuerpos mayores se enfrentó la muestra a diferentes antisueros monovalentes y se comparó con los resultados obtenidos mediante el suero hiperinmune anti total. El primer monoclonal empleado fue un anti IgG humana puro colocado en el tercer canal, que como se observa reconoce la IgG del suero al formar un arco grande, extendido hacia el cátodo y de base ancha,1,2 idéntico al registrado por el policlonal en estudio.
En el cuarto canal se enfrentó un monoclonal anti IgM humana puro a la muestra de suero humano normal; se observa un inmunoprecipitado ancho y difuso en la zona gamma correspondiente a la IgM,3,9,10,15 y coincide también con lo encontrado previamente en el suero hiperinmune.
Por último, se enfrentó anti IgA humana puro y en dilución de 1:2 y 1:4 a partir del quinto canal y hasta el séptimo, respectivamente. Se registró también la aparición de arcos de base ancha, cercanos al punto de partida que se corresponden con IgA,16,17 identificándose de manera similar por el suero hiperinmune antitotal obtenido en carnero.
En la figura 2 se muestra una inmunoelectroforesis de leche materna teñida con azul de Coomasie lo que posibilita el aumento de la sensibilidad física de la técnica.5,12
En todos los pocillos se colocaron 5 µL de leche materna según se muestra en la leyenda. En los primeros tres canales se enfrentó la muestra a nuestro antisuero problema, anti IgA de calostro humano obtenido en carnero. Se observa la presencia de arcos de precipitado correspondientes a la IgA, en su forma clásica de arco de base ancha y difusa cercano al punto de partida que son reconocidos en la muestra en todas las diluciones. Además, se observa un segundo inmunoprecipitado detectado por nuestro antisuero también en todas las diluciones, más difuso que el anterior y un poco más desplazado desde el punto de partida hacia el cátodo.
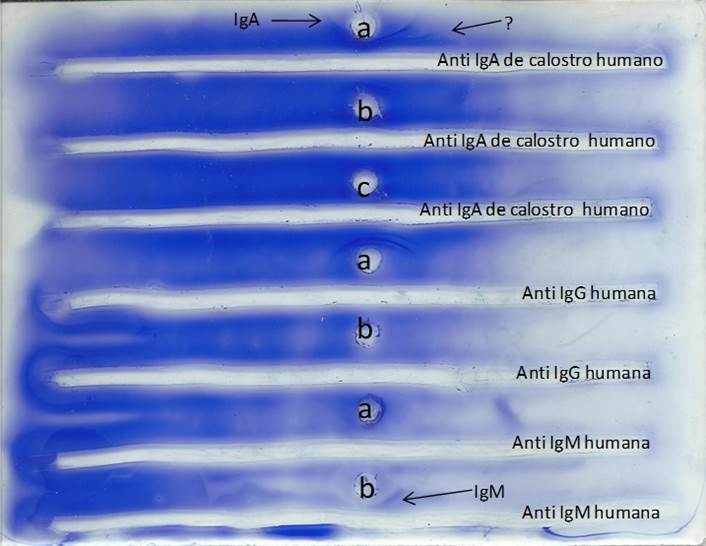
Fig. 2 Inmunoelectroforesis de leche materna. a: leche materna pura. b: leche materna 1:2. c: leche materna 1:4
La muestra de leche materna pura y en dilución de 1:2 se enfrentó a un antisuero monoclonal comercial anti IgG humana, pero en este caso no fue detectada dicha inmunoglobulina, como se puede observar.
En los últimos dos canales fueron colocados 100 µL de un antisuero monoclonal comercial anti IgM humana que se enfrentó a la muestra pura y en dilución de 1:2, en este caso si precipitó en esta última dilución, por lo que se observa un arco de precipitado correspondiente a la IgM muy difuso, ancho situado alrededor del pocillo, características estas que se corresponden con su estructura pentamérica.
Discusión
En la figura 1 se realizó la separación electroforética de 5 µL de suero humano normal en dilución de 1:8, que es la mejor dilución que permite caracterizar los antisueros empleados y se utiliza comúnmente en otros laboratorios del mundo y del país con estos fines.9 Como resultado se pueden observar los diferentes arcos de precipitado que se corresponden con las clases mayores de inmunoglobulinas presentes en el suero humano.2,3 En el segundo canal se enfrentó la muestra al suero hiperinmune antitotal humano obtenido en carnero. Se empleó en una dilución de 1:4 que fue la mejor dilución donde se observaron los inmunoprecipitados a diferencia de la dilución 1:3 que fue la utilizada como control en nuestra técnica, como resultado de experimentos previos con una serie de diluciones diferentes del mismo antisuero. Se observan resultados muy similares a los registrados con el antisuero control: se distinguen con claridad los arcos correspondientes a las inmunoglobulinas mayores, con su migración característica en forma ancha y difusa por lo que los arcos de precipitado correspondientes a la IgG, IgM e IgA son anchos, destacándose el arco de la IgG con su forma extendida desde el punto de partida y en dirección al cátodo.1,3,11 También se identifica la albúmina en su clásica forma de bote, está situada más anódicamente y presenta un arco más grande y difuso que el resto de las proteínas, debido a la disolución del precipitado por exceso de antígeno,3 se pueden identificar además diferentes componentes proteicos con similar comportamiento electroforético con respecto al control.
Para lograr una identificación más completa de los anticuerpos mayores se enfrentó la muestra a diferentes antisueros monovalentes y se comparó con los resultados obtenidos mediante el suero hiperinmune antitotal.
El contenido proteico de la leche materna oscila entre 8, 2 y 9 g por litro, concentración que se reduce con el progreso de la lactancia, máxima durante la etapa de calostro.18,19) Entre estas proteínas se encuentran la caseína, que constituye 40 % de las proteínas totales y en el 60 % restante se encuentra la α-lactoalbúmina (37 %), la lactoferrina (27 %), la lisozima y las inmunoglobulinas, entre otras proteínas de elevado peso molecular.20,21 La IgA representa de 80 a 90 % del total de inmunoglobulinas en la leche recibiendo el neonato 0,3 g/Kg/día de esta proteína.22,23 La IgM es el anticuerpo que le sigue en concentración a la IgA en calostro y leche humana (2,5 mg/mL) seguido de la IgG (0,1 mg/mL).24
Sin embargo, la morfología de este inmunoprecipitado IgM no coincide a simple vista con el encontrado junto al arco de IgA en el antisuero problema, por lo que pudiera tratarse de otra proteína presente en la muestra, que pudiera ser lactoferrina, lactoalbúmina o algún otro componente que se encuentra en altas concentraciones en leche materna y calostro22,24 como se expuso anteriormente y contra la cual pudo haber sido inmunizado el carnero de donde se obtuvo el antisuero. Estos resultados pudieran explicarse ya que al usar IgA total purificada de calostro y no cadenas alfa purificadas el antisuero va a reconocer las cadenas ligeras comunes a todas las clases de inmunoglobulinas.
Como limitante del estudio podemos declarar que la técnica empleada es útil para identificar las clases mayores de inmunoglobulinas en suero, no así para muestras de calostro humano donde se evidencia la necesidad de su adsorción con IgG para eliminar una respuesta contra otras clases de inmunoglobulinas.















