INTRODUCCIÓN
Los mixomas son los tumores primarios más frecuentes del corazón 1-3. Suelen tener una presentación clínica muy variada que depende de su localización y grado de obstrucción mecánica. Habitualmente sus síntomas pueden agruparse en: cardíacos, generales y embólicos 2,3. Años atrás su reconocimiento era excepcional por la escasez de los medios diagnósticos, lo cual era una barrera difícil de sortear desde el punto de vista terapéutico. El desarrollo de la cirugía cardíaca con circulación extracorpórea (CEC) a partir de la década de los sesenta del siglo pasado ha permitido tratar muchos enfermos que han sido curados con la resección quirúrgica, convirtiéndola en la principal arma para su erradicación. Su asociación con otros tipos de tumores ha sido muy poco informada 4-6.
Recientemente hemos operado un paciente con diagnóstico previo de carcinoma de células renales y embolismos cerebrales múltiples. La presencia de lesiones a distancia del tumor primario llevó a plantear la posibilidad de metástasis del mismo tumor como primer diagnóstico; pero el estudio ecocardiográfico identificó una masa intracardíaca, lo que hizo replantear nuevas posibilidades diagnósticas y la remoción quirúrgica para identificar su histología y conducta definitiva.
CASO CLÍNICO
Hombre de 50 años de edad, mestizo, sin antecedentes patológicos de interés, que siete meses antes de ser referido a nuestro centro debutó con cifras elevadas de tensión arterial. En su área de salud fue estudiado y se diagnosticó una tumoración renal izquierda, por lo que se remitió al Hospital Clínico Quirúrgico Gustavo Aldereguía Lima de Cienfuegos, Cuba. Fue llevado al quirófano, se realizó nefrectomía izquierda, y el estudio histológico concluyó que era un adenocarcinoma papilar tubular renal (hipernefroma) en estadio I: tumor mayor de 7 cm que crece hasta la superficie del órgano sin infiltrar la cápsula ni el sistema pielocalicial, con glomeruloesclerosis intercapilar difusa en el parénquima renal no tumoral. El tumor no infiltra la grasa perirrenal.
Fue evaluado por Oncología (sin tratamiento específico por considerarse suficiente el procedimiento quirúrgico) y egresado a los 15 días con seguimiento por Urología. Pasados cinco meses de la cirugía reingresó en el hospital de Cienfuegos por pérdida del conocimiento, de la fuerza muscular y calambres en miembros inferiores. Al examen físico presentaba trastornos del equilibrio y la marcha, vértigos y vómitos. Se realizó una resonancia magnética nuclear que informó: imagen hipodensa de 8 mm en el hemisferio cerebeloso derecho y área poco definida hipodensa sugestiva de infiltración a ese nivel. Con otra imagen en el hemisferio cerebeloso izquierdo, que no varía con el contraste, de aproximadamente 9 mm y que impresiona lesión isquémica no reciente. La posibilidad de metástasis al cerebelo del tumor primario, aunque es una de sus formas menos frecuentes de invasión a otros órganos, era la variante más lógica y fue el primer diagnóstico que se planteó. Se impuso tratamiento sintomático y se comenzó el estudio clínico.
Se realizó un ecocardiograma transtorácico (ETT) en el que se observó una función ventricular conservada y una masa en la aurícula izquierda (AI) de 45 × 32 mm, con oclusión dinámica del tracto de salida del ventrículo izquierdo (Fig. 1). El paciente se trasladó al Cardiocentro Ernesto Guevara de Santa Clara, Villa Clara, Cuba, para concluir el estudio donde se constató que tenía un estado general conservado, presentaba grandes dificultades para la marcha y lenguaje incoherente, así como discreta disnea. La frecuencia cardíaca y las cifras de tensión arterial eran normales, y se auscultaba un soplo diastólico en foco mitral. El resto de la exploración física fue normal. En la analítica sanguínea solo eran destacables una anemia normocítica y normocrómica, así como la elevación de los reactantes de fase aguda. El electrocardiograma y la radiografía póstero-anterior de tórax fueron normales.
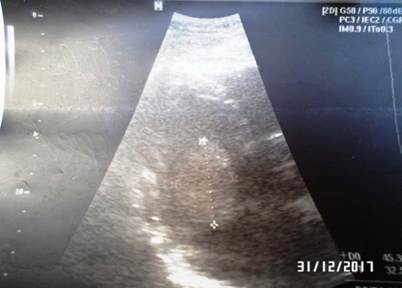
Fig. 1 Ecocardiograma transtorácico realizado en el hospital de la provincia del paciente, donde se observa masa intracardíaca de 45 × 32 mm, que protruye en diástole hacia el ventrículo izquierdo.
El ecocardiograma transesofágico confirmó los hallazgos previamente descritos, con mayor tamaño de la masa en AI (54 × 35 × 22 mm), adherida a la pared auricular y estenosis mitral ligera. La función ventricular izquierda se mantenía conservada. La coronariografía no mostró lesiones significativas, y el ultrasonido abdominal y la tomografía axial computarizada con contraste no mostraron evidencias de recidiva del tumor renal anteriormente resecado, ni adenopatías, ni infiltración de órganos de la cavidad abdominal.
Se discutió el caso con el servicio de cirugía cardiovascular y se decidió llevar de urgencia al quirófano para resecar la masa intracardíaca, ante la posibilidad de un tumor secundario o metastásico del corazón. Se realizó esternotomía media longitudinal, canulación arterial aórtica y venosa bicava, para entrar en derivación cardiopulmonar y, luego del clampeo aórtico y la parada anóxica con cardioplejia hemática isotérmica, se realizó apertura del septum interauricular y el techo de la AI. Se expuso la masa tumoral gelatinosa, friable, de aproximadamente 6-8 cm en la AI, con base de implantación ancha cercana al velo anterior mitral, sin dañar el aparato valvular (Fig. 2A). Se resecó completamente incluyendo su base de implantación (Fig. 2B) y se colocó parche de pericardio autólogo para reparar la pared auricular (Fig. 3). Se comprobó la suficiencia del aparato valvular mitral y se decidió no actuar sobre él. Luego del cierre del techo de AI y SIA se procedió al desclampeo aórtico, cierre del atrio derecho, maniobras de de aireación y salida de la circulación extracorpórea con decanulación progresiva (54 minutos de paro anóxico y 86 minutos de CEC).
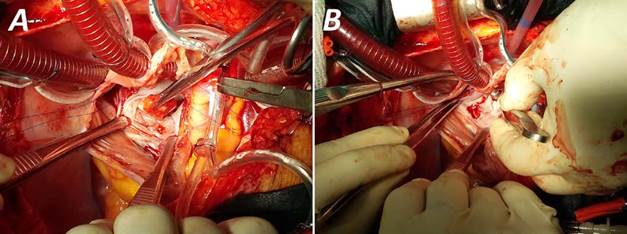
Fig. 2 Exéresis quirúrgica de la masa tumoral. A. Localizada cerca del aparato valvular mitral y fijada para su disección. B. Totalmente resecada de la aurícula izquierda. Se observan los bordes quirúrgicos de la base del tumor.
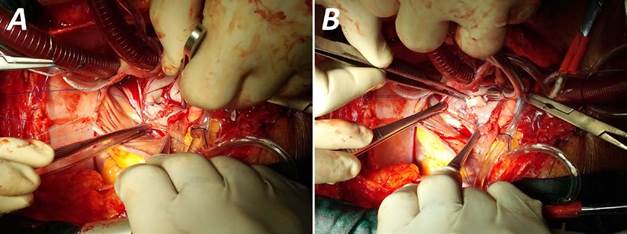
Fig. 3 A. Implante de parche de pericardio autólogo. B. Parche implantado y examen del velo anterior mitral (pinza de disección).
En la Unidad de Cuidados Intensivos el paciente presentó trastornos del ritmo (fibrilación atrial con respuesta ventricular rápida), por lo que necesitó cardioversión eléctrica en 2 ocasiones, fue entubado en las primeras 4 horas del posoperatorio, trasladado a sala convencional en 48 horas y egresado del hospital a los 10 días de la cirugía.
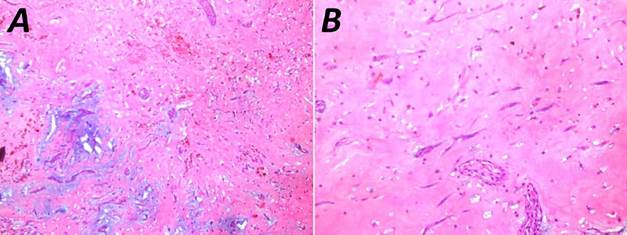
La histología del tumor fue compatible con un mixoma cardíaco (Fig. 4). A los 6 meses del posoperatorio el paciente estaba totalmente recuperado, libre de síntomas y en el ETT de control no hubo evidencias de trombos, derrame, ni masas intracardíacas, las cámaras cardíacas eran de tamaño normal, sin regurgitación mitral, y la fracción de eyección del ventrículo izquierdo de 58,6%.
COMENTARIO
La descripción de neoplasias primarias múltiples data de fines del siglo XIX. Warren y Gates establecieron los criterios anatomoclínicos para su diagnóstico 4. La frecuencia de presentación clínica es de 1,5 a 5,4% de los cánceres y de 5 a 11% en autopsias. En los últimos años se ha observado un aumento de diagnósticos tempranos de segundos tumores 5, debido quizás a su estadio, al mejor seguimiento de los pacientes, a avances en los procedimientos diagnósticos, y a la mejoría en la sobrevida desde el diagnóstico del tumor primario.
El desarrollo de un segundo tumor maligno después del tratamiento del primero con radioterapia o quimioterapia no es infrecuente; sin embargo, otros factores como: la edad, las alteraciones genéticas, el tipo de tumor primario, la exposición a determinadas sustancias o patógenos, la herencia y el estado inmunológico del paciente se han relacionado con el riesgo de presentar tumores múltiples sea de forma sincrónica o secuencial 6. Se entiende por neoplasia sincrónica a la diagnosticada al mismo tiempo que la neoplasia índice, y metacrónica, a aquella que aparece tras el diagnóstico de la primera, según el intervalo entre una y otra, sea menor o mayor a 6 meses, respectivamente. Aunque no existe unanimidad de criterios en ese intervalo de tiempo, algunos autores alegan que en intervalos menores el porcentaje de neoplasias sincrónicas que han pasado desapercibidas, puede ser elevado 7.
El sistema genitourinario está frecuentemente implicado en los casos de neoplasias primarias múltiples. Los órganos urológicos son unos de los sitios de asentamiento de algunos de los tumores primarios en casi una cuarta parte de los casos descritos8, lo que sugiere una susceptibilidad/diana incrementada de este sistema para la enfermedad neoplásica. Es por ello que el seguimiento clínico de este subgrupo de pacientes debe ser estrecho y se deben realizar cribajes de las segundas neoplasias primarias más frecuentes, pues el riesgo de presentar otro tumor independiente después de un tumor urotelial parece estar considerablemente incrementado.
El carcinoma de células renales, hipernefroma o tumor de Grawitz, representa el 90-95% de los tumores malignos renales primarios, afecta más al hombre que la mujer, en relación 2:1 y es más frecuente a partir de los 50 años, aunque en la literatura se han informado casos a cualquier edad9-11. Su tríada urológica clásica de presentación, descrita por Guyon (hematuria, dolor abdominal y tumoración en flanco), rara vez se observa en la práctica. La heterogeneidad de su presentación clínica ha hecho llamarle el «tumor del internista». Es un tumor maligno que metastatiza precozmente, fundamentalmente a ganglios linfáticos, pulmones, glándulas suprarrenales, hígado y huesos12. Puede presentar diseminaciones metastásicas a sitios raros, entre ellos el corazón13, aunque, cuando ocurre, suele ser a la aurícula derecha mediante la vena cava inferior. Aparte de esta vía de diseminación, las metástasis cardíacas del carcinoma renal son raras14,15. Se asocia a trombosis tumoral que puede extenderse a la vena renal, cava inferior y llegar a la aurícula derecha. Existen varios informes de cirugía combinada para exéresis de tumores renales y trombos atriales derechos, donde la mayoría de los autores recomiendan la CEC cuando el trombo se aloja en la aurícula derecha16-18.
Los tumores cardíacos pueden ser asintomáticos u ocasionar una sintomatología clínica diversa y variada, según su localización, movilidad y tipo histológico. Han sido denominados los grandes simuladores1, ya que pueden presentarse casi con cualquier síntoma cardiológico. Ante un tumor cardíaco primario, debe pensarse inicialmente en un tumor benigno, el mixoma, ya que es éste el más frecuente y supone más de la mitad de los casos15. El mixoma es una masa de crecimiento endocavitario que se presenta en el 75% de los casos en la aurícula izquierda, el 20% en la aurícula derecha y el resto en ventrículos y, ocasinalmente, en válvulas. Suele afectar a pacientes de mediana edad, aunque hay un amplio intervalo (11-82 años) y un predominio por el sexo femenino. Su presentación clínica dependerá de la localización, tamaño y tendencia a embolizar, si bien el 20% de ellos están asintomáticos en el momento del diagnóstico.
De forma clásica, se describen síntomas sistémicos, como: fiebre, petequias, artralgias o letargia. La exploración física puede revelar la existencia de un soplo obstructivo mitral y, raramente, el signo auscultatorio del tumor «plop», en casos en los que el mixoma ocupe todo el plano valvular mitral. La forma clínica de presentación es disnea o embolización sistémica (no metástasis), en general a sistema nervioso central (carta de presentación de nuestro caso), arterias coronarias, aorta, riñón, bazo o extremidades. En raras ocasiones pueden asociarse a mixomas mamarios o cutáneos, neoplasias testiculares, hiperactividad ovárica, pigmentación o schwannomas, que forman el síndrome de Carney2,3.
La ecocardiografía es el método de diagnóstico por excelencia, la sensibilidad del ETT para diagnosticar el mixoma es de aproximadamente el 95%, pudiendo llegar hasta cerca del 100% con su modalidad transesofágica19; y la cirugía ofrece altas tasas de curación con bajas morbilidad y mortalidad asociadas, por lo que se debe ofrecer de urgencia, en casos seleccionados, para evitar las complicaciones embólicas.
La asociación de mixoma cardíaco con hipernefroma es muy poco frecuente, con muy escasos informes en la literatura20 y en las series que describen los tumores primarios múltiples. Se trata de dos enfermedades clínicas complejas de diagnosticar por la variedad de presentaciones clínicas, no tan infrecuentes como se pensaba hasta hace poco, y que el desarrollo de las técnicas de imagen y procedimientos quirúrgicos las han revolucionado completamente; lo que permite incorporarlas en las listas de enfermedades neoplásicas tratables y con altas tasas de curación al descubrirlas en fases tempranas.
CONCLUSIONES
El aumento de la frecuencia de aparición de segundos tumores debe tenerse en cuenta en el diagnóstico y seguimiento de los pacientes con enfermedad oncológica, con énfasis en los tumores del aparato genitourinario. Los pacientes deben llevar seguimiento estrecho con las técnicas de imágenes de alta sensibilidad. La resección quirúrgica es la única forma terapéutica efectiva para pacientes con mixoma cardíaco, y se debe ofrecer de urgencia, en casos seleccionados, en los centros con equipamiento y personal entrenado en cirugía cardíaca.