My SciELO
Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Centro Azúcar
Print version ISSN 0253-5777On-line version ISSN 2223-4861
cen. az. vol.45 no.4 Santa Clara Oct.-Dec. 2018
ARTICULO
Caracterización de los residuos agrícolas de sorgo para su uso como material biosorbente de colorantes
Characterization of sorgh agricultural waste for use as coloring material biosorbent
María Hertha Broche Galindo1*, Iván Leandro Rodríguez Rico1, Yoandi Coca Rives2 y Mónica Calero de Hoces3
1 Departamento de Ingeniería Química, Facultad de Química y Farmacia. Universidad Central "Marta Abreu" de Las Villas, Carretera a Camajuani km 5 ½, Santa Clara, Villa Clara, Cuba.
2 Empresa Láctea Río Zaza. Carretera a Zaza del Medio km 2, Sancti Spíritus, Cuba.
3 Departamento de ingeniería Química, Universidad de Granada, 18071, Granada, España.
*Autor para la correspondencia: MarÃa H. Broche, Email: mariah@uclv.edu.cu
RESUMEN
En este trabajo se presentan los resultados obtenidos en la caracterización de los residuos agrícolas de sorgo (RAS) con el objetivo de valorarlo como biosorbente, para la remoción de contaminantes presentes en disoluciones acuosas. El material se recolecta de los productores y se trata mediante lavado, secado y reducción de tamaño. La caracterización consistió en el estudio sobre sus propiedades fisicoquímicas, térmicas y estructurales La determinación del punto de carga cero, los sitios ácidos y básicos, el tamaño de partícula y la composición elemental para la cuantificación de % C, % H, % N, y %S. Las propiedades térmicas por análisis termogravimétrico y las estructurales por espectroscopia de infrarrojo con transformada de Fourier (FTIR). Se encontró que 7,5 es el punto de carga cero; y que 0,750 meq/g y 0,525 meq/g son los valores para sitios ácidos y básicos respectivamente y que predomina tamaño de partícula de 0,342 mm y para los que están entre 0,63 y 0,83 mm. La composición elemental refleja que está constituido fundamentalmente de carbono y oxígeno, el análisis infrarrojo permite conocer que tiene una naturaleza altamente compleja por la cantidad de grupos funcionales superficiales presentes. En el análisis termogravimétrico se identifican cuatro zonas térmicas fundamentales asociadas a las pérdidas de masa por deshidratación, la pirólisis de hemicelulosa y celulosa, de la celulosa y de la lignina y del H+ residual. Los resultados obtenidos permiten identificar a este residuo agrícola, de bajo costo, como un posible material biosorbente para colorantes.
Palabras clave: biosorción; lignocelulósicos; residuo de sorgo.
ABSTRACT
This paper presents an agricultural residues of sorghum (RAS) characterization with the objective of its evaluation as biosorbent of contaminants present in aqueous solutions. The material is collected from the producers and treated by washing, drying and sizing. For characterization its physicochemical, thermal and structural properties were studied. Thermal properties were determined by thermogravimetric analysis and structural properties by Fourier Transform Infrared Spectroscopy (FTIR). It was found that 7.5 is the zero loading point; and that 0.750 meq/g and 0.525 meq/g are the values for acid and basic sites respectively and that particle sizes of 0.342 mm and those between 0.63 and 0.83 mm predominate. The elemental composition reflects that it is mainly carbon and oxygen. Infrared analysis shows that it is highly complex in nature due to the number of surface functional groups present. Thermogravimetric analysis identifies four fundamental thermal zones associated with losses of mass through dehydration, pyrolysis of hemicellulose and cellulose, cellulose and lignin, and residual H+. The results obtained allow the identification of this low cost agricultural waste as a possible biosorbent material for dyes.
Key words: biosorption; lignocellulosics; sorghum residue.
INTRODUCCIÓN
El agua, es necesaria en los sectores domésticos, industriales y agrícolas, e indispensable para el desarrollo de los mismos. Sin embargo, la escasez y contaminación se han incrementado en los últimos años, asociado al crecimiento de la población y al vertido de contaminantes.
Los residuales procedentes de sectores dedicados a la producción de textiles, cosméticos, papel, plásticos, productos farmacéuticos, alimentos, entre otras, tienen concentraciones significativas de colorantes. Los colorantes son moléculas orgánicas recalcitrantes, resistentes a la digestión aeróbica, y son estables a la luz, calor y agentes oxidantes por consiguiente difíciles de tratar. Su eliminación se ha convertido en uno de los principales problemas para las industrias debido al impacto, visual, aumento de carga orgánica y toxicidad (Ramos, 2010).
Variedad de métodos se han aplicado para el tratamiento de aguas residuales, con procesos que pueden ser químicos y físicos entre los que se encuentran la adsorción, floculación, coagulación, sedimentación, precipitación y métodos electroquímicos, la mayoría con alto costo (Doğan, 2008); o biológicos, pero, su aplicación se ve restringida porque requieren una mayor área superficial y están sujetos a mayor sensibilidad por variaciones diurnas, toxicidad de ciertos químicos y menor flexibilidad en diseño y operación.
Se ha venido enfocando los estudios en los biosorbentes que son de bajo costo, como los materiales agrícolas derivados de recursos naturales, residuos vegetales o subproductos industriales, compuestos en su mayoría a base de celulosa y pueden ser utilizados sin ningún pretratamiento térmico o químico (Demirbas, 2008; Yagud et al., 2014; Wasti y Awan, 2016; Hasan et al., 2015).
Son materiales lignocelulósicos, generados en cantidades considerables en países agrícolas alrededor del mundo. Entre estos residuos o productos secundarios se incluyen entre otros el bagazo de la caña de azúcar, cáscara de arroz, cáscara de maní; celulosa, tallo de banano, pulpa de remolacha, corteza de cacao, tuza de maíz, cáscara de naranja, hueso de aceituna, hojas de caucho y fibra de coco (Calderón, 2015; Vargas, 2009).
El proceso de biosorción, se caracteriza preferentemente por la retención de las sustancias, en la superficie del biosorbente. La retención puede darse mediante la interacción de la sustancia a grupos funcionales que se encuentran en la superficie como carboxilos, hidroxilos, fosfatos, también ocurren procesos de difusión, por eso la importancia de la caracterización química para conocer la afinidad particular de un determinado adsorbente por un adsorbato específico. En todos los casos, los procesos de sorción dependen de la naturaleza de la sustancia a eliminar, de la estructura y características del sorbente, del proceso previo al que se ha sometido y de las condiciones experimentales, por ese motivo muchos investigadores han buscado las propiedades de adsorción de los adsorbentes no convencionales (Uddin et al., 2009). Por consiguiente, el uso de biomasa no viva, se ha convertido en el principal tema de investigación para los científicos, siendo estas de fácil acceso, bajo costo y con gran capacidad de adsorción. Además, sus propiedades físicas y químicas pueden ser modificadas, incrementando los sitios activos de sorción (Tejada-Tovar et al., 2015).
Romina (2011) compara la capacidad de adsorción del bagazo de Agave salviana con sorgo y avena, concluyendo que si bien la capacidad de adsorción de azul de metileno en sorgo y avena fue mayor, para bagazo de Agave salmiana fue de 61,23 mg g-1, lo que indica un valor interesante en comparación con otros biosorbentes propuestos por diferentes autores. Algunos de los materiales estudiados, la capacidad de adsorción y el autor son: alga marina (Caulerpa racemosa), 5,23 mg g-1, Cengiz y Cavas (2008); polvo de hoja de nim, 8,76mg g-1, (Bhattacharya et al., 2005); cáscara de naranja, 13,9 mg g-1,(Annadurai et al., 2002); cáscarade trigo, 21,5 mg g-1, (Bulut y Aydin, 2006).
En el presente trabajo se realiza la caracterización de RAS con el objetivo de evaluar su uso como material biosorbente de colorantes. Se elige este residuo por el incremento de su cultivo dado el interés del Ministerio de Agricultura para generalizar la siembra de este cereal, por los diversos usos de los granos y el forraje, con la finalidad de desarrollar alternativas productivas que contribuyan a garantizar la seguridad alimentaria (González, 2016). En zonas de India, África y China, constituye más del 70% del total de calorías y suministra gran parte de las proteínas de la dieta (Mestre, 2007).
MATERIALES Y MÉTODOS
El biosorbente empleado, RAS, fue cultivado por un productor del municipio de Encrucijada perteneciente a la provincia de Villa Clara, el mismo fue recolectado días posteriores a la cosecha y preparado antes de su utilización. Este cultivo tiene gran importancia a escala mundial, pues está comprobado que puede sustituir cereales como el trigo y el maíz en la mayoría de los usos de estos, tanto en la alimentación humana como en la producción de forraje o grano para la ceba de animales, y también en la industria. A su vez posee alto potencial de producción de granos y buenas perspectivas de contribución al desarrollo de la agricultura. La planta presenta un sistema radical profuso que le brinda una estructura de soporte muy desarrollada, lo que permite acumular gran cantidad de reservas; además le confiere una mayor capacidad de penetración y mejor persistencia en climas secos, donde la escasez de agua se mantiene por períodos prolongados; su tallo es grueso, con espinas que nacen por pares, y la altura puede oscilar de 1 a 3 m. Los nudos presentan abundantes pilosidades. Las hojas son alternas, aserradas, lanceoladas, anchas y ásperas en su margen; estas tienen la propiedad de quitinización durante los períodos secos, lo que retarda el proceso de desecación (Pérez, 2010). La célula vegetal está formada fundamentalmente por la celulosa, hemicelulosa y lignina (González, 2004).
2.1. Preparación.
Se lavan con abundante agua y se secan en una estufa (Binder) a una temperatura de 50 °C por un tiempo de 6 h. Posteriormente se realiza la reducción de tamaño empleando un molino (MF10 basic). Para lograr la separación por tamaño de partículas se emplea un tamiz (Marui) con tamices de diámetros de 2,4 mm; 2 mm; 1 mm; 0,84 mm; 0,63 mm; 0,40 mm; 0,355 mm; 0,342 mm y fondo.
1.2. Determinación del punto de carga cero y sitios ácidos y básicos.
Para la determinación del punto de carga cero, se pesan diferentes masas de RAS desde 0,01 g a 1,00 g (10 muestras). Se colocan en Erlenmeyer de 50 mL y se le agregan 20,0 mL de NaCl a 0,1 M. Los frascos se tapan y se agitan manteniendo la temperatura a 30 ºC durante 48 h para que se equilibren las cargas(Noh y Schwarz, 1988) Pasadas las 48 h, se mide el pH de cada una de las muestras con el pH-metro (Hanna pH 213).
Los sitios ácidos y básicos en la superficie del biosorbente se determinan por el método de Boehm, que consiste en pesar 1,0 g de biosorbente, por duplicado; una cantidad se utiliza para determinar sitios ácidos y otra para sitios básicos. La primera cantidad de biomasa de sorgo se coloca en un Erlenmeyer con 50,0 mL de hidróxido de sodio, NaOH, 0,1 N, y la segunda cantidad se coloca en un recipiente con 50,0 mL de ácido clorhídrico, HCl, 0,1 N (Boehm, 2001). Las soluciones se tapan, se dejan a temperatura constante de 30 °C, durante 5 días y se agitan en la zaranda (Sartorius). Pasados los 5 días se toman muestras de 10,0 mL de las soluciones y cada una se titula con la disolución estándar de hidróxido de sodio o ácido clorhídrico según sea el caso, midiendo durante la titulación el pH de la disolución con un pH-metro (Hanna pH 213).
Mediante la ecuación 1 se calcula la concentración (meq/g) para los sitios ácidos y los sitios básicos.
2.3. Composición elemental de los RAS.
El análisis de la composición elemental del biosorbente se realiza utilizando un analizador elemental (Fisons Instruments EA- 1108 CHNS-), que permite realizar la determinación simultánea del porcentaje de carbono, hidrógeno, nitrógeno y azufre en 15 minutos, mediante el siguiente procedimiento:
1) Se pesan 2 mg de muestra y se envuelven en una lámina de estaño.
2) Se quema la muestra en la lámina de estaño a 1000 ºC (el estaño al oxidarse hace subir la temperatura a 1800 ºC).
3) Los productos de esta reacción se pasan a través de óxido de wolframio para oxidar el 100 % de la muestra.
4) Se hacen circular los gases a través de finos alambres de cobre para obtener N2, CO2, H2O y SO2.
5) Los gases resultantes se introducen en una columna de cromatografía para separarlos generando una señal en un detector de conductividad térmica (TCD) que luego se procesa en un computador personal (PC).
2.4. Análisis infrarrojo.
Se realiza un análisis infrarrojo (IR) con un espectrofotómetro de IR por Transformada de Fourier (FTIR), marca Perkin-Elmer, (Spectrum 65), para determinar los principales grupos funcionales que están presentes en el RAS. Procedimiento:
1) Se pesan 2 mg de residuo seco y se muelen hasta un tamaño inferior a 0,250 mm.
2) El sólido molido se dispone en el compartimento para la muestra del espectrofotómetro y se presiona con el accesorio de diamante.
3) A continuación se realiza el barrido para obtener el espectro de IR en el rango de 4000 - 400 cm-1 con una resolución de 2 cm-1.
2.5. Análisis termogravimétrico.
El análisis termogravimétrico fue realizado en un equipo (TA Instruments SDT Q600), empleando crisoles de alúmina de 90 μL, a una velocidad de calentamiento de 10°C min-1, en un intervalo de 30 a 1000°C, con un flujo a 100 mL min-1 de gas nitrógeno pureza 5,0.
RESULTADOS Y DISCUSIÓN
3.1. Preparación del material.
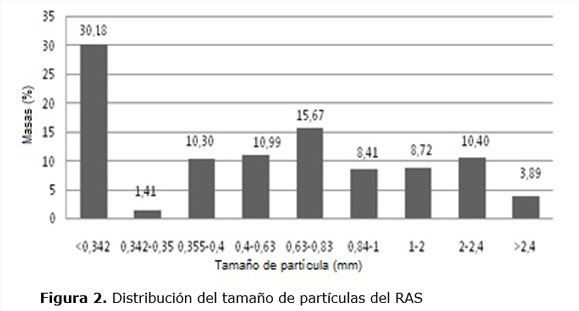
En las Figuras 1 y 2 aparecen imágenes del material después de lavado y secado, molido y la distribución del tamaño de partículas. Los resultados de la distribución del tamaño de partícula permite observar que no es uniforme en cuanto cantidades por tamaño, predomina con 30,18 % para los valores menores que 0,342 mm y con 15,67 % para los valores entre 0,63 y 0,83 mm. El tamaño de partícula del biosorbente normalmente no afecta la capacidad de sorción, pero en algunos casos se ha observado que esta capacidad aumenta al reducir el tamaño de la partícula, ya que el área de los poros puede ser más accesible y el área de contacto es mayor (Rosas, 2012; Ramos, 2010).
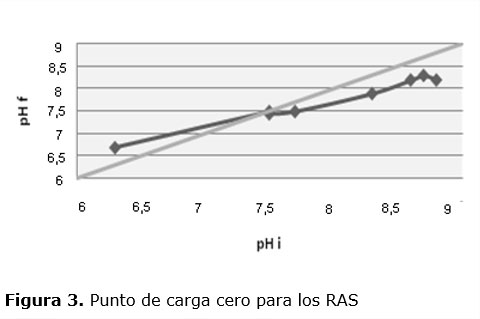
3.2. Determinación del punto de carga cero y sitios ácidos y básicos. El punto de carga cero, se muestra en la Figura 3, corresponde al punto donde la curva de pH final en función del pH inicial se corta con la diagonal; a valores de pH superiores al punto de carga cero, en la superficie del biosorbente hay mayor concentración de grupos funcionales disociados con carga negativa y por debajo, predominan en la superficie del biosorbente grupos funcionales disociados con carga positiva; el valor es de 7,5. Amaringo y Homasa, (2013) citan a otros autores que han determinado el punto de carga cero de diferentes minerales que se han usado para la remoción de contaminantes en aguas, confirmando su importancia en lo referente al tratamiento adecuado de efluentes líquidos, pero declara que ha sido poco explorada en los residuos agroindustriales; en su estudio para la cascarilla de arroz es 5,40, para la corteza de coco es 4,61. En otras publicaciones también se exponen resultados (Ramos, 2010) para borra de café obtiene 3,47; (Romina, 2011) para el bagazo de Agave y aserrín de haya 3,5 y 5,2; (Martín, 2008) para el hueso de aceituna, alpeorujo y ramón 4,38, 4,37 y 4,53; (Bermejo, 2016) para el bagazo de caña y cáscara de cacao 6,08 y 7.
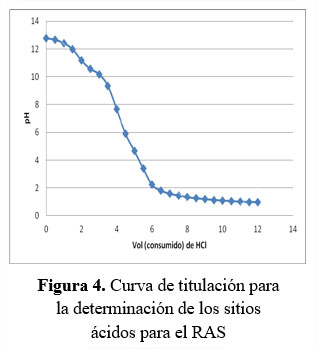
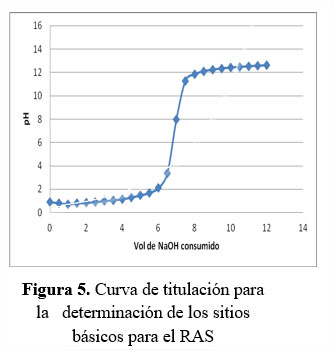
Las curvas de titulación para la determinación de los sitios ácidos y básicos se muestran en la figuras 4 y 5.
Aplicando la ecuación 1 se obtiene que los valores para los sitios ácidos, es de 0,750 meq/g y sitios básicos, es de 0,525 meq/g. Se puede observar que la concentración de grupos funcionales disociados con carácter ácido predomina con respecto a los sitios básicos; que un biosorbente sea totalmente ácido o básico depende de la concentración de estos grupos y de la fuerza de los mismos (Menéndez, 1995). Jiménez y Jacobo (2015) así como Bermejo, (2016) reportan respectivamente los sitios ácidos - básicos para paja de sorgo y pluma de pollo en 4,57 -0,3 y 4,75 – 0,8 el primero, y para bagazo de caña y la cáscara de cacao en 5, 00 - 2,35 y 0,60 - 0,51 el segundo.
3.3. Composición elemental.
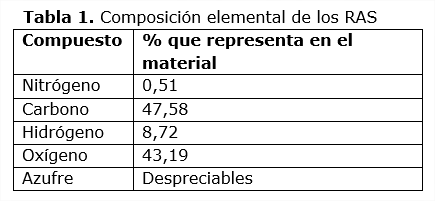
Los resultados obtenidos en el análisis de la composición elemental del biosorbente se muestran en la tabla 1, con el contenido de nitrógeno, carbono, hidrógeno, oxígeno y azufre; es significativo el alto contenido de carbono y oxígeno, las cantidades de hidrógeno y nitrógeno son pequeñas, y despreciables el contenido de azufre. Pinzón-Bedoya y Cardona, (2008) realizan comparación para otros residuos agrícolas, que se han estudiado en el sur de España, con la cáscara de naranja, en todos los casos los valores del análisis elemental es similar al de los RAS.
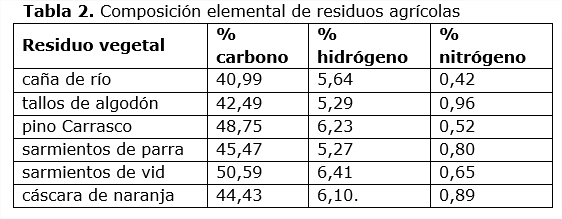
Se indican en la tabla 2 para algunos de esos residuos vegetales, la composición en los por cientos que corresponden a carbono, hidrógeno y nitrógeno para cada uno.
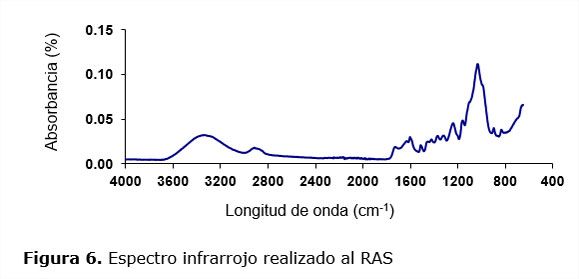
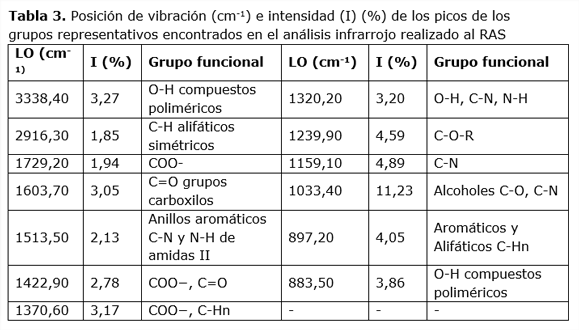
3.4. Análisis infrarrojo.
El análisis infrarrojo permite mostrar en la figura 6 y en la tabla 3 las longitudes de ondas (LO) que corresponden a los diferentes grupos funcionales, por tener cada enlace químico tiene una banda de absorción, se identifica a cuál corresponde considerando la posición, ancho e intensidad de absorción de los mismos utilizando las tablas de correlación. Un enlace puede tener varios modos vibracionales, dependiendo del tipo de movimiento de los átomos, las bandas de absorción para un enlace son únicas en cuanto a su longitud de onda y a su forma (Dionisio, 2012).
En el IR se destacan bandas de interés, ubicadas entre 3200 a 3600 cm-1, se deben normalmente a varias vibraciones por estiramientos O-H asociadas a alcoholes y carboxílicos; entre 2800 y 2900 cm-1 atribuibles a ácidos carboxílicos y carbonilicos; las bandas de diferentes intensidades que se observan de 1239 a 1729 cm-1, pueden pertenecer al estiramiento de ácidos, aldehídos, cetona, amidas, esteres; la que corresponde a 1603 cm-1, es característica del estiramiento asimétrico del doble enlace del carboxilo; las bandas en la región 1033 a 1159 cm-1 pueden pertenecer a la presencia de modos de estiramiento de los grupos nitrilos y las bandas de diferentes intensidades cercanas a 1033cm-1 y a 883cm-1 son asignadas al estiramiento de polisacáridos (tensiones C-O) o a uniones de componentes polisacáridos.
3.5. Análisis termogravimétrico.
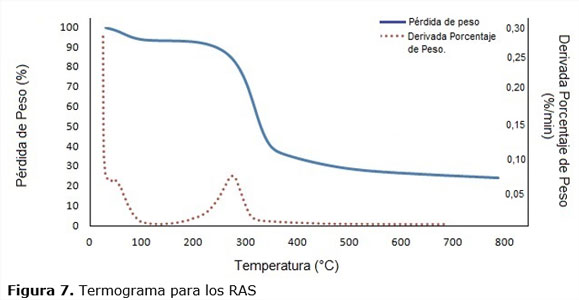
El análisis termogravimétrico permite medir la cantidad y la velocidad de cambio de la masa de un material como función de la temperatura o tiempo en una atmósfera controlada, dichas medidas son utilizadas principalmente para determinar la composición de un material y para predecir su estabilidad térmica a temperaturas hasta de 1000°C (Quintero et al., 2013). En la figura 7 se muestra la curva de degradación térmica correspondientes a los experimentos dinámicos, se diferencian cuatro zonas térmicas fundamentales. A temperatura inferior a 200 °C, ocurre una pérdida de masa de alrededor de 8 %, se atribuye al proceso de deshidratación que corresponde a ese rango de temperatura. En el intervalo entre 200 a 380 ºC, tiene lugar una pérdida de aproximadamente el 56 %, para la pirólisis de hemicelulosa y celulosa, con un pico en 292,04 ºC. La tercera zona a temperaturas superiores a los 380 °C, también ocurre pirólisis de la celulosa y de la lignina, en un % próximo al 8 y a temperaturas superiores a 560 ºC, se aprecia una de pérdida de peso más constante, la cual está asociada a la pérdida del H+ residual. El contenido de celulosa, hemicelulosa y lignina en materiales semejantes a los empleados para su estudio lo expone (Rosas, 2012), considera que la celulosa puede conferir estabilidad a los residuos, no obstante, la lignina, la hemicelulosa y las proteínas generalmente presentan un mayor contenido de sitios ácidos, los cuales son indispensables para la remoción de especies catiónicas durante la adsorción por intercambió iónico. El estudio para borra de café, semillas de algodón y hojas de caqui realizado por (Blasco, 2018) tiene resultados semejantes.
CONCLUSIONES
1. La evaluación del punto de carga cero con valor de 7,5 indica en términos generales un comportamiento básico. Sugiere que puede ser adecuado para la remoción de contaminantes de naturaleza aniónica a valores inferiores y de naturaleza catiónica a valores superiores.
2. El estudio de la química superficial muestra la distribución de sitios ácidos y básicos, que corresponde a 0,750 meq/g y 0,525 meq/g respectivamente.
3. Los porcientos de C y O2, obtenidos en el análisis elemental, son de 47,48 y 43, 19 % respectivamente, están en correspondencia con los resultados del análisis infrarrojo; que muestra que los grupos determinantes son del tipo hidroxilo, carbonilo, estructuras de simples enlaces carbono-carbono, y ésteres y éteres.
4. El estudio termogravimétrico realizado a los RAS presenta cuatro zonas de pérdidas de masas, la primera de agua de alrededor de 8 %, seguida de la pirólisis de hemicelulosa y celulosa de aproximadamente el 56 %, en la tercera pirólisis de la celulosa y de la lignina cercano al 8% y una de pérdida de peso más constante del H+ residual.
REFERENCIAS
Amaringo, F., Hormasa, A., Determinación del punto de carga cero y punto isoeléctrico de dos residuos agrícolas y su aplicación en la remoción de colorantes., Revista de investigación agraria y ambiental, Vol. 4, No. 2, 2013, pp. 27-36.
Bermejo, D., Remoción de plomo y cadmio presente en aguas residuales mineras mediante biosorción en columnas con bagazo de caña y cáscara de cacao., Tesis presentada en opción al Título de Ingeniero Ambiental, Universidad de Cuenca, Ecuador, 2016.
Blasco, C., Evaluación de los recursos agrícolas para su valorización energética en calderas Spouted Bed Reactors., Trabajo de fin de grado en Ingeniería Química, Universidad de Valencia, España, 2018.
Boehm, H.P., Surface oxides on carbon and their analysis: a critical assessment., Carbon., Vol. 40, No. 2002, 2001, pp. 145- 149.
Calderón, J.E., Caracterización eléctrica de materiales adsorbentes, cerámicos y carbonosos., Tesis presentada en opción al Grado Científico de Doctor en Ingeniería Mecánica, Energética y de los Materiales, Universidad de Extremadura, España, 2015.
Demirbas, A., Heavy metal adsorption onto agro-based waste materials: A review., Journal of Hazardous Materials, Vol. 157, No. 2, 2008, pp. 220–229.
Dionisio, E., Aprovechamiento de residuos vegetales para la eliminación de cobre presente en medios acuosos mediante biosorción., Tesis presentada en opción al Grado Científico de Doctor en Ingeniería Química, Universidad de Granada, España, 2012.
Doğan, M.A., Alkan, H., Biosorption of Methylene Blue from Aqueous Solutions by Hazelnut Shells: Equilibrium, Parameters and Isotherms., Water Air Soil Pollut, Vol. 192, No. 1-4, 2008, pp. 141–153.
González, R., Científicos villaclareños reafirman potencialidades del sorgo., Periódico Vanguardia, Villa Clara, 12 de junio 2016, pp. 1-2.
González, M., Degradabilidad ruminal de ensilados de fracción vegetativa, hojas y tallos de maíz (grano y silaje) y de sorgo (con y sin taninos)., Tesis presentada en opción al título de Licenciada en Producción Animal, Instituto Nacional de Tecnología Agropecuaria, Argentina, 2004.
Hasan, S., Fuat, G., Yunus, O., Conversion of grape industrial processing waste to activated carbon sorbent and its performance in cationic and anionic dyes adsorption., Journal of Cleaned Production, Vol. 93, No. 15, 2015, pp. 84-93.
Jiménez, L., Jacobo, A., Estudio de las propiedades fisicoquímicas de bioadsorbentes para la remoción de cromo VI en agua., Jóvenes en la Ciencia, Vol. 2, No. 2, 2015, pp. 229-234.
Martín, M., Caracterización y aplicación de biomasa residual a la eliminación de metales pesados., Tesis presentada en opción al Grado Científico de Doctor en Ingeniería Química, Universidad de Granada, España, 2008.
Menéndez, J., On the difference between the isoelectric point and the point of zero charge of carbons., Carbon, Vol. 33, No. 11, 1995, pp. 1655-1659.
Mestre, Y.,Usos del sorgo granífero en la alimentación humana y otros., Publicación miscelánea No. 108, Estación experimental agropecuaria Rafaela, Argentina, 2007, pp. 9-19.
Noh, S.J., Schwarz, A.J., Estimation of the Point Zero Charge of Simple Oxides by Mass Titration., Journal of Colloid and Interface Science, Vol. 130, No. 1, 1988, pp. 157-164.
Pérez, A., Caracterización y potencialidades del grano de sorgo (Sorghum bicolor L. Moench)., Pastos y Forrajes, Vol. 33, No. 1, 2010, pp. 1-29.
Pinzón-Bedoya, M.L., Cardona, A., Caracterización de la cáscara de naranja para su uso como material bioadsorbente., Bistua, Vol. 6, No. 1, 2008, pp. 1-23.
Quintero, V.D., Lucas, J.C., Álzate, E. A., Determinación de las propiedades térmicas y composicionales de la harina y almidón de chachafruto., Ingenium, Vol. 14, No. 28, 2013, pp. 16-32.
Ramos, J., Estudio del proceso de biosorción de colorantes sobre borra (chuncho) de café., Tesis presentada en opción al Grado Científico de Máster en Ciencias-Química, Universidad Nacional de Colombia, Colombia, 2010.
Romina, C., Remoción de azul de metileno en agua empleando bagazo de agave salmiana como biosorbente., Tesis presentada en opción al Grado Científico de Máster en Ciencias Ambientales, Universidad Autónoma de San Luis Potosí, México, 2011.
Rosas, J.M., Aplicación de residuos agrícolas para el tratamiento de agua contaminada con colorantes., Tesis presentada en opción al Grado Científico de Máster en Ciencias con orientación a Procesos Sustentables,Universidad Autónoma de Nuevo León, México, 2012.
Ruth, V., Celiaquía: alternativas para una dieta libre de gluten., El Salvador Ciencia & Tecnología, Vol. 17, No. 23, 2012, pp. 13-17.
Uddin, T., Islam, A., Mahmud, S., Rukanuzzaman, M., Adsorptive removal of methylene blue by tea waste., Journal of Hazardous Materials, Vol. 164, No. 1, 2009, pp. 53–60.
Vargas, M., Evaluación del proceso de biosorción con cáscaras de naranja para la eliminación del colorante comercial Lanasol Navy CE en aguas residuales de la industria textil., Ingeniería, Vol. 13, No. 3, 2009, pp. 39-43.
Wasti, A., Awan, M., Adsorption of textile dye onto modified immobilized activated alumina., Journal of the association of Arab Universities or Basic and applied Sciences, Vol. 20, 2016, pp. 26-31.
Yagud, M.T., Sen T.K., Afrose, S., Ang, H., Dye and its removal from aqueous solution by adsorption: a review. Advances, Colloid and Interface Science, Vol. 209, No. 1, 2014, pp. 172-184.
Recibido: Enero 31, 2018
Revisado: Abril 3, 2018
Aceptado: Junio 14, 2018