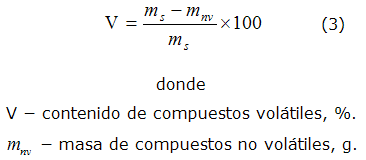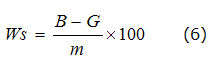Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Química
versión On-line ISSN 2224-5421
Rev Cub Quim vol.29 no.1 Santiago de Cuba ene.-abr. 2017
ARTICULOS
Características fisicoquímicas del carbón activado de conchas de coco modificado con HNO3
Physiochemical Characteristic of Activated Carbon of Coconut Shell Modified with HNO3
MSc. Mónica Hernández-RodríguezI; Dr. Alexis Otero-CalvisI; Dr. José Falcón-HernándezII, Dr. Yan YpermanIII
IInstituto Superior Minero Metalúrgico "Antonio Núñez Jiménez", Holguín, Cuba, mhernandezr@ismm.edu.cu
IIUniversidad de Oriente, Santiago de Cuba, Cuba
IIIUniversidad de Hasselt, Bélgica
RESUMEN
En la investigación se estudió el efecto de la modificación química con soluciones diluidas de ácido nítrico, en las características fisicoquímicas del carbón activado de conchas de coco. Los cambios en la química superficial del material adsorbente fueron evaluados mediante varios métodos de análisis químicos: Titulación de Boehm, Titulación de pH y Análisis Próximo según las normas ASTM. El proceso de modificación incrementó los grupos superficiales ácidos oxigenados de forma proporcional a la concentración de la solución oxidante, provocando una disminución del pH, el pH en el punto de carga cero, el contenido de cenizas y los compuestos solubles en agua y en ácido. La reducción del pH en el punto de carga cero y el aumento de la humedad resultaron aspectos positivos para la posible utilización del material adsorbente en la remoción de cationes presentes en soluciones acuosas.
Palabras clave: carbón activado, modificación química, química superficial.
ABSTRACT
In these search the effect of the chemical modification with diluted solutions of nitricacid, in the physiochemical characteristics of the activated carbon of coconut shell was studied. The changes in the superficial chemistry of adsorbent materials were evaluated by several methods of chemical analysis, as Bohem Tritation, pH Tritation and Proxime Analysis according to the ASTM norms. The modification process increased the acid superficial oxygenated groups in a proportional way to the concentration of acid nitric solution, causing a decrease of the superficial area, the pH, the pH in the point zero charge, the ash content and the soluble compounds in water and acid. The decrease of pH in the point zero charge and the increment of moisture content, is positive for its employment in the removal of cations present in aqueous solutions.
Keywords: activated carbon, chemical modification, superficial chemistry.
INTRODUCCIÓN
El término adsorción se emplea para describir la existencia de una elevada concentración de cualquier sustancia en la superficie de un líquido o sólido [1].
Esta concentración superficial suele ser bastante mayor que la concentración promedio en el sólido o en el líquido, debido al estado de desbalance de fuerzas moleculares o al estado de insaturación. Como resultado las superficies sólidas y líquidas tienden a completar sus fuerzas atrayendo y reteniendo en sus superficies gases o sustancias disueltas con las cuales estén en contacto. La sustancia así adsorbida en la superficie se denomina fase adsorbida o adsorbato, mientras que la sustancia en la cual está fijada se conoce como adsorbente [1].
El carbón activado es un adsorbente muy versátil, porque el tamaño y distribución de sus poros en la estructura carbonosa le confieren posibilidades de utilización en la purificación en fase gaseosa y líquida [2, 3].
La capacidad de remoción del carbón activado está influenciada por la superficie activa, debido a su elevado y variado grado de porosidad; sin embargo, un aspecto influyente en el proceso de adsorción lo constituye la química superficial del material adsorbente. Varios investigadores [4-8] establecen que la capacidad de remoción de los adsorbentes no está determinada solamente por sus características texturales, sino que los grupos químicos existentes en la superficie ejercen un papel distintivo, producto a las interacciones específicas con el adsorbato.
La superficie de los carbones puede encontrarse combinada, en mayor o menor proporción, con otros átomos o grupos de átomos distintos al carbono (heteroátomos), entre los que figuran los grupos carboxílicos, lactonas, fenólicos y carbonilos como principales grupos de carácter ácido y los grupos básicos algunos autores lo atribuyen a los grupos pirona, cromeno y electrones p deslocalizados en las capas del grafeno [3, 9].
Todos los carbones presentan, en principio, un carácter hidrófobo, que puede ser disminuido por la adición de ciertos grupos superficiales, lo que puede conseguirse por oxidación con algún tipo de agente oxidante que crea grupos oxigenados, dando lugar a la adsorción de moléculas de agua, que a su vez adsorberán nuevas moléculas por formación de puentes de hidrógeno; de esta forma se incrementa el carácter hidrófilo, que resulta beneficioso para la adsorción de compuestos inorgánicos en fase acuosa [3].
Por ello el presente estudio evalúa cómo influye la modificación del carbón activado de conchas de coco producido en Baracoa, con soluciones diluidas de ácido nítrico, en sus características fisicoquímicas y en la formación de grupos superficiales ácidos oxigenados, que permita su posterior empleo en la adsorción de cationes presentes en soluciones acuosas.
MATERIALES Y MÉTODOS
Modificación química del carbón activado de conchas de coco
Entre la amplia variedad de reactivos químicos utilizados para potenciar la formación de grupos superficiales ácidos (H2SO4, H3PO4, H2O2, HNO3, O3, CH3COOH), fue escogido el ácido nítrico (HNO3) por su mejor desempeño en la formación de grupos oxigenados en comparación con los otros agentes oxidantes comúnmente empleados [8, 9]. Se decidió evaluar su actuación utilizando concentraciones diluidas, en el rango de 0,1 - 1 mol/L y para el punto medio de 0,55 mol/L, pues los procedimientos de oxidación con HNO3 provocan una disminución del área superficial del carbón, producto a la erosión de las paredes de los microporos, pudiendo afectar su capacidad de adsorción [7].
Los tratamientos se desarrollaron durante 2 horas a 200 °C, temperatura donde se considera que las fuerzas convectivas ayudaran a la agitación y mezclado entre el material adsorbente y la solución de HNO3. Luego los carbones fueron lavados con abundante agua destilada para remover cualquier exceso de ácido existente en el mismo y posteriormente secados a 110 °C durante 6 horas en una estufa de calefacción eléctrica. Las codificaciones de los adsorbentes obtenidos según la concentración de la solución empleada se relacionan en la tabla 1.
TABLA 1. CODIFICACIÓN DE LOS CARBONES ACTIVADOS
| Tratamiento | Codificación |
| Carbón activado granular | CAG |
| CAG tratado con soluciones de HNO3 de 0,1 mol/L | CAG1 |
| CAG tratado con soluciones de HNO3 de 0,55 mol/L | CAG2 |
| CAG tratado con soluciones de HNO3 de 1 mol/L | CAG3 |
Contenido de grupos ácidos superficiales
Los grupos funcionales ácidos existentes en la superficie del carbón fueron determinados por la titulación de Boehm [8, 10] mediante la adición de 0,5 g de carbón en diferentes beakers conteniendo 50 mL de soluciones de hidrógenocarbonato de sodio (NaHCO3), carbonato de sodio (Na2CO3) e hidróxido de sodio (NaOH) de 0,05 mol/L. Luego de 24 horas en agitación se filtró y se valoró 10 mL de filtrado de las soluciones con ácido clorhídrico (HCl) de 0,05 mol/L. Fue asumido que el NaOH neutraliza los grupos carboxílicos, lactonas y fenólicos, el Na2CO3 los carboxílicos y las lactonas, mientras que el NaHCO3 solamente reacciona con los carboxílicos.
Los grupos superficiales ácidos por gramo de adsorbente se determinaron mediante la ecuación 1:
Análisis Próximo
El contenido de humedad, compuestos volátiles, cenizas y carbono fijo fue determinado de acuerdo a las normas ASTM.
Procedimiento para determinar la humedad [11]
- En un crisol tarado pesar 1 g de cada muestra.
- Llevar a una mufla precalentada a 145 – 150 °C.
- Secar aproximadamente alrededor de 3 horas.
- Sacar y llevar a un desecador hasta enfriarse.
- Pesar a temperatura ambiente. Repetir el procedimiento hasta que el peso de la muestra sea constante.
El contenido de humedad en base seca se determina a partir de la ecuación 2:
Procedimiento para determinar el contenido de materia volátil [12]
- En un crisol tarado poner 1 g de cada muestra seca.
- Llevar tapado a una mufla a 950 °C por 7 minutos.
- Sacar y llevar rápidamente a un desecador hasta enfriarse.
- Pesar el crisol tapado a temperatura ambiente (el peso corresponde a los compuestos no volátiles).
El contenido de materia volátil se determina según la ecuación 3:
Procedimiento para evaluar el contenido de cenizas [13]
- Pesar en un crisol tarado 0,1 g de cada muestra seca.
- Llevar la mufla a 650 °C de 3 a 16 horas (se considera que la incineración es completa cuando el peso sea constante).
- Sacar y llevar rápidamente a un desecador hasta enfriarse.
- Pesar a temperatura ambiente.
El contenido de cenizas y carbono fijo se determina a partir de las ecuaciones 4 y 5:
Determinación del pH
Los grupos químicos activos de la superficie de los carbones activados pueden alterar el pH de los líquidos en el cual es añadido. Para la determinación del pH es necesario pulverizar el carbón activado granular sin secar.
Procedimiento [14]
- Pesar 4 g de carbón en un beaker de 250 mL, añadir 100 mL de agua destilada libre de dióxido de carbono (CO2), cubrir con una tapa de vidrio y hervir por 5 minutos.
- Insertar un termómetro y poner en reposo la solución para permitir que las partículas se asienten. Verter el líquido sobrenadante antes que la temperatura descienda los 60 °C.
- Enfriar la porción decantada a temperatura ambiente y medir el pH con un valor decimal.
La determinación del pH se realizó empleando un pH-metro Nahita, modelo 903.
Determinación del pH en el punto de carga cero (pHZCO)
La determinación del pHZCO fue realizada mediante el procedimiento de titulación de pH. Para ello se prepararon soluciones de NaCl de 0,01 mol/L a diferentes valores de pH (entre 3 y 12 unidades), luego 0,15 g del adsorbente fue añadido a 50 mL de cada solución y puesto en agitación por 48 horas, pasado este tiempo se midió el pH final de la solución. El pHZCO se determinó gráficamente como el punto en el cual la variación de pH contra pH inicial cruza la línea en la cual su valor es cero [8].
Contenido de compuestos solubles en agua y en ácido
El contenido de compuestos solubles en agua y en ácido brinda una estimación de la pureza de los carbones activados en relación a las sustancias extractables en estos medios, para ello se emplea carbón activado granular pulverizado (granulometría menor de 0,1 mm) y se secado a 150 °C.
Procedimiento [15, 16]
- Pesar 10 g de carbón pulverizado y seco, transferirlo a un balón, agregar 100 mL de agua, 10 mL de ácido clorhídrico concentrado (solamente para el caso de los compuestos solubles en ácido), mezclar y conectar el frasco al condensador. Hervir en reflujo durante una hora.
- Enjuagar el frasco con un poco de agua y filtrar la mezcla lo más caliente posible en un erlenmeyer para filtración.
- Enjuagar el frasco con tres porciones de 25 mL de agua y agregar el enjuague al erlenmeyer para filtración. Luego refrescar el filtrado a temperatura ambiente, transferirlo cuantitativamente a un frasco volumétrico de 250 mL y enrasar.
- Pesar un platillo seco y limpio con una precisión de 0,1 mg.
- Pipetear 50 mL de extracto de agua en el platillo y evaporar a sequedad durante 3 horas.
- Pesar el platillo después de refrescarlo en un desecador durante 15 minutos y repetir el secado con un intervalo de una hora hasta alcanzar un peso constante con una precisión de 0,2 mg.
Los contenidos de compuestos solubles en agua y en ácido se evalúan según las ecuaciones 6 y 7:
RESULTADOS Y DISCUSIÓN
Resultados del contenido de grupos ácidos superficiales
En la tabla 2 se relaciona el contenido de grupos ácidos conformados por grupos carboxílicos, lactonas y fenólicos, determinados mediante la titulación de Boehm. Como se observa, los grupos superficiales de carácter ácido se incrementan en correspondencia con el aumento de la concentración de la solución oxidante desde un valor inicial de 0,05 mmol/g alcanzado para el material adsorbente sin modificar hasta valores entre 1,150 y 1,575 mmol/g.
En todos los casos estos grupos se incrementan entre 23 y 32 veces sobre el valor inicial. También es notable un mayor incremento de los grupos carboxílicos, seguidos de los fenólicos y las lactonas excepto para el CAG 3, en el cual el orden es el siguiente: carboxílicos, lactonas y fenólicos.
Para el carbón activado sin modificar (CAG) fue imposible por esta vía determinar el contenido de cada grupo independiente, debido a que los consumos de la solución ácida del agente valorante en cada uno de los casos fueron similares a los de la solución básica empleada.
TABLA 2. CONTENIDO DE GRUPOS ÁCIDOS SUPERFICIALES
| Carbón | Carboxílicos (mmol/g) | Lactonas (mmol/g) | Fenólicos (mmol/g) | Totales (mmol/g) |
| CAG | - | - | - | 0,050 |
| CAG1 | 0,850 | 0,043 | 0,257 | 1,150 |
| CAG2 | 1,250 | 0,019 | 0,281 | 1,550 |
| CAG3 | 0,900 | 0,381 | 0,294 | 1,575 |
Resultados del Análisis Próximo
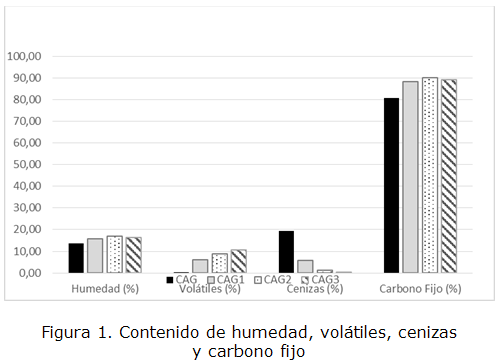
En la figura 1 se observan los resultados del análisis próximo, realizados a cada material adsorbente.
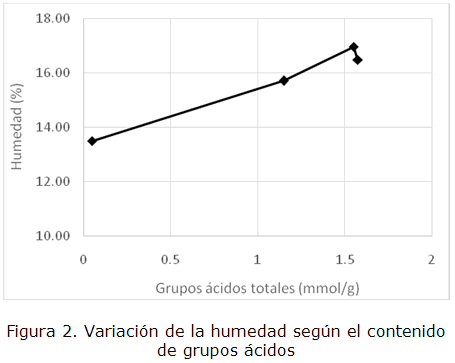
Se evidencia un aumento de la humedad de los carbones activados al ser tratados con las soluciones de ácido nítrico, alcanzándose el máximo valor (16,96 %) para el CAG2. Estos resultados se deben al incremento de los grupos oxigenados en la superficie de los materiales adsorbentes con carga parcial negativa, que atraen a los átomos de hidrógeno que conforman las moléculas de agua que se encuentran a su alrededor, aumentando el carácter hidrófilo (figura 2), aspecto positivo para el empleo de los carbones activados en la adsorción de especies químicas presentes en soluciones acuosas.
Paralelamente al incremento de la humedad también se produce un aumento de los compuestos volátiles (desde 0,01 % hasta 10,54 %) y del carbono fijo, aunque en este caso ocurre una inflexión lográndose el máximo valor para el CAG2.
El contenido de cenizas del adsorbente (característica no deseada en el material), varía desde un valor máximo de 19,24 % para el carbón activado sin modificar (CAG) y un mínimo de 0,44 % cuando se emplea la mayor concentración de ácido nítrico en el tratamiento, correspondiente con el adsorbente CAG3. La disminución de este índice se debe, fundamentalmente, al proceso de lavado para la eliminación del exceso de agente oxidante en el material.
Resultado del pH de los carbones activados
La variación del pH del carbón activado de conchas de coco con respecto al cambio en el contenido de grupos ácidos se observa en la figura 3. La muestra sin modificar (CAG) posee un carácter básico con un pH de 10 unidades, mientras que para los carbones CAG1, CAG2 y CAG3 el pH obtenido es de 7,9, 5,2 y 5,1 unidades respectivamente. El incremento de los grupos superficiales ácidos producto a la modificación química del material adsorbente originó una disminución del pH de los carbones activados.
Resultados del pH en el punto de carga cero (pH ZCO)
En la tabla 3 se relacionan los valores de pH alcanzados para cada tipo de carbón activado, luego de estar en contacto durante 48 horas con soluciones de cloruro de sodio de 0,1 mol/L a diferentes valores de pH inicial.
TABLA 3. VARIACIÓN DEL PH DE LAS SOLUCIONES
| Solución | pH inicial | pH final | |||
| CAG | CAG1 | CAG2 | CAG3 | ||
| 1 | 3,3 | 5,0 | 3,7 | 2,7 | 2,6 |
| 2 | 6,3 | 6,6 | 6,1 | 4,3 | 4,4 |
| 3 | 9,9 | 7,9 | 7,8 | 6,7 | 6,9 |
| 4 | 11,0 | 8,4 | 8,1 | 7,5 | 7,8 |
| 5 | 11,2 | 8,6 | 8,3 | 7,7 | 8,0 |
A partir de la variación de pH contra pH inicial (figura 4 y 5) se obtuvieron los valores de pH en el cual la carga neta en la superficie del carbón es cero (pHZCO), siendo estos de 6,8, 5,7, 2,2 y 1,9 unidades para el CAG, CAG1, CAG2 y el CAG3 respectivamente. En todos los casos se obtuvieron los modelos de regresión (tabla 4), que permitió la determinación exacta de pHZCO de los carbones, en el caso del CAG2 y CAG3 la determinación del pHzco se realizó mediante la extrapolación de las líneas de tendencias obtenidas.
El incremento de grupos ácidos superficiales en la matriz de los adsorbentes provocó un descenso del pH en el punto de carga cero. Estos resultados coinciden con los obtenidos en el caso de la determinación del pH de los carbones activados y brindan la posibilidad de que en soluciones acuosas donde el pH de la solución sea mayor que el pHZCO, la superficie de los adsorbentes quede cargada negativamente, ejerciendo atracciones electrostáticas sobrecationes presentes en la solución.
TABLA 4. MODELOS DE REGRESIÓN PARA DETERMINAR EL PHZCO
| Tipo de carbón | Modelo de regresión | Coeficiente de regresión (R2) |
| CAG | ΔpH = -0,012 1 pHinicial2 - 0,385 3 pHinicial + 3,129 8 | 0,997 7 |
| CAG1 | ΔpH = 0,019 7 pHinicial2 - 0,655 pHinicial + 1,346 6 | 0,999 8 |
| CAG2 | ΔpH = -0,043 9 pHinicial2 + 0,206 1 pHinicial + 0,209 8 | 0,998 4 |
| CAG3 | ΔpH = 0,018 pHinicial2 - 0,582 3 pHinicial + 1,032 4 | 0,999 5 |
Resultados del contenido de solubles en agua y en ácido
El contenido de solubles en agua y en ácido de los diferentes carbones activados se evidencia en la tabla 5. El valor mínimo en ambos casos se alcanza para el carbón tratado con la mayor concentración de ácido nítrico (CAG3) siendo de 0,04 % y 0,05 % para el contenido de solubles en agua y en ácido, respectivamente.
La oxidación del material adsorbente provoca una disminución de los extractables en ambos medios, aspecto positivo para su empleo en la adsorción de especies químicas en soluciones acuosas, pues asegurará un menor contenido de los compuestos solubles en la solución, luego de ocurrir los procesos de separación sólido-líquido.
TABLA 5.CONTENIDO DE COMPUESTOS SOLUBLES EN AGUA Y EN ÁCIDO
| Adsorbente | Solubles en agua (%) | Solubles en ácido (%) |
| CAG | 0,167 | 0,230 |
| CAG1 | 0,083 | 0,110 |
| CAG2 | 0,089 | 0,100 |
| CAG3 | 0,040 | 0,050 |
CONCLUSIONES
La modificación química del carbón activado de conchas de coco con soluciones diluidas de ácido nítrico originó un incremento de los grupos ácidos (carboxílicos, lactonas y fenoles) existentes en la superficie del material adsorbente y de la humedad. También causó una disminución del pH, el pH en el punto de carga cero, las cenizas y el contenido de compuestos solubles en agua y en ácido de acuerdo con el incremento de la concentración de la solución oxidante. El aumento de la humedad relacionado con el carácter hidrófilo y la disminución del pH en el punto de carga ceroes positivo para su posterior empleo en la adsorción de cationes presentes en soluciones acuosas.
REFERENCIAS BIBLIOGRÁFICAS
1. PETER, A., PAULA, J. Elements of Physical Chemistry. Fifth Edition. New York: W. H. Freeman and Company New York, 2009. 578 p. ISBN-13: 978–1–4292–1813–9
2. RODRÍGUEZ, E. P., GIRALDO, L., MORENO-PIRAJÁN, J. C. "Modificación de la química superficial de carbones activados. Efecto de la oxidación con soluciones de HNO3 y H2O2 sobre la remoción de cadmio (II) en solución acuosa." Afinidad, LXXI, 2014, vol. 565, p 49-56.
3. SMISEK, M., CERNY S. Activated Carbon Manufacture, Properties and Applications. New York: Elsevier Publishing Company, 1970, 479 p., ISBN -10: 0444407731
4. AHMADPOUR, A., et al. "Rapid removal of cobalt ion from aqueous solutions by almond green hull". Journal of Hazardous Materials, 2009, vol. 166, p 925–930.
5. HUANG, C-C., LI, H-S., CHEN, C-H. "Effect of surfaceacidic oxides of activated carbon onadsorption of ammonia". Journal of Hazardous Materials, 2008, vol. 159, p 523-527.
6. LU, C. LIU, C. "Removal of nickel (II) from aqueous solution by carbon nanotubes". Journal of Chemical Technology and Biotechnology, 2006, vol. 81 p 1932–1940.
7. RODRÍGUEZ, E. P., GIRALDO, L., MORENO, J. "Oxidación de la superficie de carbón activado mediante HNO 3 y H 2 O 2: efecto sobre la remoción de níquel (II) en solución acuosa". Revista Colombiana de Química, 2011, vol. 40, p 349 – 364.
8. SHIM, J.-W., PARK, S.-J., RYU, S-K. "Effect of modification with HNO 3 and NaOH on metal adsorption by pitch-based activated carbon fibers". Carbon, 2001, vol. 39 p 1635–1642.
9. RODRÍGUEZ, E. P. Modificación y Caracterización Calorimétrica de Carbón Activado Granular, para la Remoción de Cd (II) y Ni (II) en Adsorción Simple y Competitiva. Tesis en Opción al título de Magister en Química. Universidad Nacional de Colombia, Bogotá, 2011.
10. BOEHM, H. "Someaspects of thesurfacechemistry of carbon blacks and othercarbons". Carbon, 1994, vol. 32 p 759-769.
11. ASTM 2867–09. Standard Test Methods for Moisture in Activated Carbon. ASTM International, West Conshohocken, PA, 2014.
12. ASTM 5832 –98. Standard Test Methods for Volatile Matter Content of Activated Carbon Samples. ASTM International, West Conshohocken, PA, 2014.
13. ASTM 2866– 94 . Standard Test Methods for total Ash Content of Activated Carbon. ASTM International, West Conshohocken, PA, 1999.
14. ASTM 3838 – 80. Método de Prueba Estándar para pH del Carbón Activado. ASTM International, West Conshohocken, PA, 1999.
15. ASTM D-5029. Standard Test Methods for Determining Water Soluble Compunds. Carbon. ASTM International, 2011.
16. D6385 - 99. Standard Test Method for Determining Acid Extractable Content in Activated Carbon by Ashing. Carbon. ASTM International, 2011.
Recibido: 25/05/2016
Aceptado: 15/09/2016
MSc. Mónica Hernández-Rodríguez, Instituto Superior Minero Metalúrgico "Antonio Núñez Jiménez", Holguín, Cuba, mhernandezr@ismm.edu.cu