My SciELO
Services on Demand
Article
Indicators
-
 Cited by SciELO
Cited by SciELO
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Tecnología Química
On-line version ISSN 2224-6185
RTQ vol.36 no.3 Santiago de Cuba Sept.-Dec. 2016
ARTICULO ORIGINAL
Estudio de la transformación del Aceite de Soya usado en ésteres etílicos de ácidos grasos
Etudy of the Transformation of the Oil of Used Soya in Fatty Acid Ethyl Ester
Ing. Anabel Sarracent-López, MSc. José Gandón-Hernández
Facultad de Ingeniería Química, ISPJAE, La Habana, Cuba
Resumen
La reutilización de los aceites vegetales en la elaboración de alimentos trae efectos nocivos para la salud y por otro lado se necesita de un complejo tratamiento para poder descartarlos sin que afecten al medio ambiente. Transformarlo en ésteres metílicos o etílicos de ácidos graso y glicerina, mediante la transesterificación con el alcohol correspondiente, puede constituir un procedimiento adecuado para su tratamiento. Se investigó con aceite de soya residual, proveniente de una empresa productora de alimentos fritos. Es conocido que con etanol el proceso de transformación presenta dificultades que no aparecen con el metanol, pero al mismo tiempo no trae los inconvenientes de este último, en cuanto a toxicidad y adquisición, ya que por tratarse de un derivado de la industria azucarera nacional, no constituye una materia prima de importación. Se experimentó con etanol de 80 %, 85 % y 90% de pureza y se trabajó a 35 ºC y 50 ºC. Los rendimientos finales de ésteres etílicos, resultan bajos si se comparan con los obtenidos para los procesos similares con metanol, siendo 85 % el mayor valor obtenido bajo las condiciones establecidas para el proceso. Se realizó la evaluación de los costos para producir 1L de ésteres etílicos a nivel de laboratorio, siendo los gastos de 0,56 pesos/L.
Palabras clave: aceite vegetal usado, transesterificación, etanol, ésteres etílicos.
Abstract
The reuse of vegetable oils in food processing brings harmful health effects and on the other hand needs a complex treatment to discard without affecting the environment. Transformed into methyl or ethyl esters of fatty acids and glycerin by transesterification with the corresponding alcohol, can be a suitable method for treatment. It was investigated residual soybean oil from a producer of fried foods and ethanol. It is known that with this spirit the transformation process presents difficulties not listed with methanol, but at the same time does not bring the drawbacks of the latter, for toxicity and acquisition, and that since it is a derivative of the domestic sugar industry does not constitute a raw material import. We experimented with ethanol 80 %, 85 % and 90 % purity and worked 35 ºC and 50 ºC. Final yields of ethyl esters, are low compared with those obtained for similar processes with methanol, 85 % being the highest yield obtained under the conditions of the process. An assessment of costs was conducted to produce 1L of ethyl esters in the laboratory, the expenses of 0,56 pesos/L.
Keywords: used vegetable oil, transesterification, ethanol, ethyl esters.
INTRODUCCION
Se conoce que en la actualidad, los alimentos fritos gozan de una popularidad cada vez mayor y son aceptados por personas de todas las edades, pero no se tiene conciencia de que el aceite no debe ser reutilizado en la elaboración de alimentos, debido principalmente a que una vez que es sometido a temperaturas elevadas, el mismo genera dioxinas, un agente cancerígeno muy agresivo, y uno de los químicos que tienen la dudosa fama de pertenecer a la docena sucia de contaminantes orgánicos. Por otro lado constituye un residual extremadamente riesgoso que se desecha sin contar con ningún tratamiento previo que cumpla con las normas de vertimientos, esto trae consigo la contaminación del agua, además su infiltración hacia los suelos causa graves deterioros en los mismos, con su consecuente repercusión en las fuentes subterráneas de agua y los cultivos [1, 2,3].
Por las características de este residual, no puede tratarse por los métodos tradicionales, de ahí que una vía ventajosa, desde el punto de vista energético es transformar estos aceites en ésteres metílicos o etílicos y glicerina, mediante la transesterificación con alcoholes como el metanol y el etanol, aunque la mayoría de las tecnologías reportadas se basan en el uso del alcohol metílico [4, 5].
Estos ésteres poseen características similares a las del combustible Diesel, por lo que pueden ser utilizados a modo de biocombustibles, fundamentalmente en forma de mezclas con el combustible fósil y la glicerina resultante tiene un sin número de aplicaciones, tanto cruda como refinada.
Las principales variables que influyen en el rendimiento, conversión y cinética de la reacción de transesterificación son la calidad de la materia prima, tipo y concentración de catalizador, tipo y concentración de alcohol, relación molar alcohol:aceite y las condiciones de reacción como temperatura, presión y agitación [6, 7]. A continuación se enfatiza en algunas de ellas. Por la estequiometria de la reacción se utiliza una relación molar alcohol: aceite de 3:1, pero como esta reacción de transesterificación es reversible se recomienda utilizar una relación mayor, alimentando un exceso de alcohol para favorecer la reacción directa. Según Abreu [4] y Abularach [5] con el empleo de etanol las condiciones más adecuadas de relación molar alcohol:aceite vegetal usado son de 3,6:1 a 9:1. Por otro lado George Anastopoulos y otros [8] investigaron que la relación molar alcohol: aceite más apropiada se encuentra en el intervalo de 6:1 a 12:1. Aunque estas relaciones son las que mejor se ajustan con la utilización de este alcohol, se debe tener en cuenta que un valor alto de la misma afecta la separación de glicerina, debido al incremento de la solubilidad de esta con el etanol [9, 10].
Durante la reacción generalmente se forma una emulsión, en la metanólosis esta emulsión desciende rápidamente formándose una capa rica en glicerol quedándose en la parte superior otra zona rica en ésteres metílicos. En cambio en la etanólisis esta emulsión no es estable y complica mucho la separación y purificación de los ésteres etílicos [10, 11].
Los catalizadores que se suelen utilizar a escala comercial son los homogéneos básicos ya que actúan mucho más rápido y además permiten operar en condiciones moderadas de 25°C a 35°C y a presión atmosférica [11,12,13].
Leung y Guo [14], analizaron el efecto de tres catalizadores básicos en la transesterificación de aceite usado de cocina, el cual se encuentra representado en la figura 1.
Fig.1 Efecto de tres catalizadores básicos en la reacciónde transesterificación.
Se observa que se obtienen altos porcentajes de ésteres contenidos en el producto con el empleo de los tres catalizadores a medida que aumenta su concentración, sin embargo, se puede apreciar que los mejores resultados fueron con el hidróxido de sodio [13,14,15].
La concentración del catalizador es un factor determinante para llevar a cabo la reacción puesto que una cantidad elevada del mismo limita el rendimiento, lo que se debe a que la viscosidad del medio aumenta, dificultando el contacto entre los componentes, mientras que una cantidad mínima no permite neutralizar parte de los ácidos grasos libres presentes en el aceite usado lo cual también influye directamente en el rendimiento [4,8,10]. Es por ello que Abreu [4] recomienda una relación de catalizador: aceite de 0,2 % a 0,8 % en peso de NaOH con respecto al aceite usado, no muy lejano a este intervalo se encuentra el sugerido por George Anastopoulos [8] siendo de 0,25 % a 1,5 %.
Es objetivo de este trabajo al abordar el tema de la elaboración de biocombustibles, utilizar etanol en el proceso de transformación de aceites usados en ésteres, puesto que, aunque se considere que los mejores resultados se obtienen con metanol, el etanol al margen de las dificultades operacionales con su uso, no traería los inconvenientes que tiene el metanol en cuanto a toxicidad y procedencia. Además por tratarse de un derivado de la industria azucarera nacional, no constituiría una materia prima de importación.
Este proceso de transformación de aceites usados de origen alimentario en ésteres, constituye una propuesta factible para contrarrestar la utilización indiscriminada del aceite en las frituras, además es una variante atractiva no solo para el tratamiento de un residual muy peligroso, sino que además aborda el tema de la obtención de biocombustibles que pueden sustituir a los combustibles fósiles, petróleo y sus derivados, puesto que están presentando señales de agotamiento y se estima que a mediano plazo ya no será posible cubrir la demanda mundial. Esta situación, sumada a la contaminación ambiental y al calentamiento global, provocados en gran medida por el uso de este tipo de combustibles, es un reto de enormes proporciones, pero también una oportunidad de realizar investigaciones referentes al uso de biocombustibles, como una alternativa más para la implementación de energías renovables.
En el entorno cubano proyectos de este tipo resultan atrayentes principalmente para los polos turísticos, las grandes instalaciones dedicadas a la elaboración de alimentos y los asentamientos poblacionales con infraestructura de servicios.
MATERIALES Y METODOS
Preparación y caracterización del aceite
Para la obtención de ésteres etílicos a escala de laboratorio, inicialmente se realizó un pre tratamiento del aceite vegetal usado proveniente de una empresa de elaboración de alimentos, la cual tiene una planta de productos conformados en la que se pre-fríen productos empanados y sin empanar, por lo que fue necesario realizar una operación de filtración para eliminar los sólidos suspendidos en el mismo y posteriormente su secado para eliminar el agua captada durante el proceso de fritura [5]. A continuación se realizó la caracterización del mismo para conocer la calidad de la materia prima que se utilizó en la investigación, las propiedades determinadas experimentalmente fueron: viscosidad cinemática, densidad, acidez e índice de acidez.
Método de transesterificación
Se empleó como método la transesterificación vía catálisis alcalina, puesto que resulta un proceso relativamente simple. Además que permite el empleo de relaciones molares alcohol: aceite bajas [7, 15].
Material reactivo
En la reacción se utilizó como catalizador el NaOH en forma de perlas con un 95 % de pureza, donde la cantidad necesaria para neutralizar los ácidos grasos libres presentes en el aceite se determinó mediante un proceso de valoración, y alcohol etílico por las ventajas antes mencionadas con respecto al metanol.
Diseño de experimentos
Para los experimentos se fijaron las siguientes variables: 250 rpm, 20 minutos como tiempo de reacción, relación molar alcohol: aceite de 3:1 y un valor de concentración de 0,41g de NaOH correspondiente a 50mL de aceite usado determinada por el proceso de valoración, para la selección de estos valores se tuvieron en cuenta las experiencias obtenidas en los trabajos anteriores así como la premisa de que el proceso se realizara en condiciones poco exigentes, en cuanto al consumo de energía y utilización de reactivos [13, 16].
Para la temperatura se establecieron dos niveles 35ºC y 50ºC tomando como referencia la temperatura ambiente promedio en Cuba y los 78 ºC correspondientes a la temperatura de ebullición del alcohol.Además los valores escogidos se encuentran en el intervalo reportado por diferentes autores [10, 15].
Se trabajó con tres niveles de pureza del alcohol etílico, 80 %, 85 % y 90 %; ya que aunque el mismo debe comercializarse con una pureza entre el 95 % y el 96 %, por diversas razones no siempre se cumple con este parámetro de calidad. Además la posibilidad de trabajar a concentraciones más bajas, permite utilizar alcoholes rechazados de otras producciones.
Luego de conocer los niveles de las variables para este estudio los cuales se muestran en la tabla 1, se seleccionó un diseño factorial del tipo 2k·3m con k=1 y m=1, y dos réplicas para cada corrida experimental, lo que significa un total de 18 corridas experimentales.
| Variables | Símbolo del parámetro | Niveles | |||
| Temperatura (°C) | X1 | 35 | |||
| 50 | |||||
| Concentración de etanol (%) | X2 | 80 | |||
| 85 | |||||
| 90 | |||||
En todos los experimentos se utilizaron 50mL de aceite y 10mL de etanol, volúmenes referentes a una relación aproximada alcohol: aceite de 3:1.
Descripción de los experimentos
Determinación de la concentración de catalizador necesario
Cuando el aceite es nuevo, es decir sin previo uso, se necesitan de forma generalizada 3,5g de NaOH por litro de aceite para catalizar la reacción de transesterificación [17]. Pero cuando el aceite es usado se requiere una concentración mayor de NaOH para neutralizar los ácidos grasos libres que se forman durante el proceso de fritura, que pueden afectar o impedir la transesterificación. Esta concentración se determinó partir de una valoración.
Se prepararon las soluciones de etanol para las diferentes concentraciones partiendo de etanol reactivo de 99,5 % [18].
Determinación de la cantidad de etanol
Para la conocer el volumen de etanol en exceso para 50 mL de aceite a partir de la relación molar fijada, fue preciso la determinación de las masas molares de ambos reactivos mediante las ecuaciones 2 y 3 para conocer la cantidad molar estequiométrica de la reacción de transesterificación.

La masa molar del aceite de soya usado se determinó mediante la siguiente ecuación [19, 20].

Conociendo las cantidades de los reactivos se procedió a llevar a cabo la reacción de transesterificación básica bajo las condiciones experimentales establecidas en el diseño. Los ésteres etílicos obtenidos luego de su purificación fueron caracterizados al igual que el aceite residual para conocer las propiedades de los mismos.
RESULTADOS Y DISCUSION
En la tabla 2 aparecen los resultados de las mediciones de la viscosidad cinemática para el aceite de soya usado después de ser utilizado en un severo proceso de fritura. La viscosidad cinemática, se midió con un viscosímetro capilar automático, según el método estándar: ASTM D 445, D 7279, ISO 3104.
Tabla 2
Viscosidad cinemática a 40 ºC del aceite usado
| Muestra | Viscosidad cinemática (mm2/s) |
| 1 | 36,2 |
| 2 | 36,8 |
| 3 | 36,5 |
| Media | 36,5 |
| Desviación estándar | 0,300 |
Como era de esperar, se incrementa el valor de esta propiedad en el aceite usado con respecto al aceite de soya nuevo, el cual presenta una viscosidad según la bibliografía de aproximadamente 32,40 mm2/s [20]. Este aumento es debido a las transformaciones que trae aparejadas el proceso de fritura, causadas fundamentalmente por la polimerización, donde los radicales libres que se unen entre sí y con los ácidos grasos insaturados forman compuestos de mayor tamaño y masa molar (polímeros) que incrementan la viscosidad del aceite, provocan la formación de espuma y una capa de consistencia plástica en la superficie y en el propio recipiente, la cual es muy difícil de eliminar [2,3,22].
La determinación de la densidad aparente se realizó en el laboratorio con un picnómetro tipo B de 25 mL. En la tabla 3 aparecen los resultados de las mediciones de la densidad aparente a 15 ºC para el aceite de soya usado.
Tabla 3
Densidad del aceite usado
| Muestra | Densidad (kg/m3) |
| 1 | 918,23 |
| 2 | 918,01 |
| 3 | 918,15 |
| Media | 918,13 |
| Desviación estándar | 0,111 36 |
De acuerdo a los resultados mostrados en la tabla 3 y su comparación con los valores de densidad para el aceite de soya sin usar (917 kg/m3 – 924 kg/m3) se pudo apreciar que la densidad del aceite residual de frituras se encuentra dentro del intervalo establecido. Esto demuestra que el aceite presentó un adecuado almacenamiento, es decir que no se encontró expuesto de forma excesiva a la atmósfera debido a que se mantuvo en recipientes herméticamente cerrados antes de ser utilizado en los experimentos, lo que trajo consigo que su rancidez, propiedad relacionada con la densidad, no se afectó considerablemente [23].
Con respecto al índice de acidez y la acidez se determinaron según NC-ISO 660:2001 para aceites y grasas de origen animal y vegetal mediante las siguientes expresiones:
Acidez expresada en ácido oleico

Para determinar este volumen se tiene como principio disolver la muestra en una mezcla de disolventes y valorar mediante una solución etanólica de hidróxido de potasio.
c : concentración exacta, en moles por litro, de la solución de hidróxido de potasio utilizada,mol/L.
M: masa molecular del ácido en que se expresa el resultado (ácido oleico=282), g/mol-equivalente de ácido oleico.
P: masa en gramos (g) de la muestra utilizada.
Ambas propiedades presentan una estrecha relación entre sí, puesto que ambas se encuentran en correspondencia con la cantidad de ácidos grasos libres presentes en el aceite luego de los procesos de fritura.
A continuación en las tablas 4 y 5 se muestran los resultados de la determinación del índice de acidez y la acidez.
Tabla 4
Índice de acidez del aceite usado
| Muestra | Índice de acidez |
| 1 | 5,70 |
| 2 | 5,51 |
| 3 | 5,89 |
| Media | 5,7 |
| Desviación estándar | 0,190 0 |
Tabla 5
Acidez del aceite usado
| Muestra | Acidez (% ácido oleico) |
| 1 | 2,88 |
| 2 | 2,77 |
| 3 | 2,96 |
| Media | 2,81 |
| Desviación estándar | 0,055 7 |
Para el índice de acidez se obtuvieron valores superiores a los reportados en la bibliografía para el aceite de soya sin usar, siendo el límite establecido en las normas para el índice de acidez de 0,6 mg KOH/g de aceite y un nivel de ácidos grasos libres menor de un 0,2 % [7]. Este incremento es consecuencia de la presencia de agua proveniente del producto frito, que junto a las elevadas temperaturas de la fritura, favorecen la reacción de hidrólisis de los triglicéridos aumentando la cantidad ácidos grasos libres [7].
Después de la reacción de transesterificación se evidenció la separación de dos fases, como se muestra en la figura 2.
Fig. 2 Separación de las fases de ésteres etílicos y glicerina
Conocer las cantidades de ésteres etílicos producidos y el rendimiento del proceso o lo que es lo mismo la relación volumétrica del producto con respecto a las materias primas, resulta de gran importancia, pues constituye un indicador de la eficiencia con que ocurre la reacción.
En la tabla 6 se muestran los valores de los rendimientos obtenidos a partir del diseño de experimento planteado.
Tabla 6
Rendimientos obtenidos en la fase de ésteres etílicos
| Corrida | X1(°C) | X2(%) | Volumen de ésteres etílicos | Rendimiento con respecto al aceite (%)* |
| 1 | 35 | 90 | 41,83(0,288 7) | 84 (0,577 35) |
| 2 | 50 | 90 | 42,67(0,577 4) | 85 (1,154 70) |
| 3 | 35 | 85 | 41,33(0,577 4) | 83 (1,154 70) |
| 4 | 50 | 85 | 42,00(0,866 0) | 84 (1,732 05) |
| 5 | 35 | 80 | 40,33(0,577 4) | 81 (1,154 70) |
| 6 | 50 | 80 | 41,00(0,866 0) | 82 (1,732 05) |
*Los valores reportados corresponden a los promedios y entre paréntesis aparecen las desviaciones típicas
Esta tabla indica la influencia de la temperatura y la concentración de etanol sobre el rendimiento de la reacción. El rendimiento se encuentra en un intervalo de 81 % hasta 85 %.
Estos rendimientos que se muestran en la tabla 6 son los que se obtuvieron luego de los procesos de lavado y secado, usados en la producción de biocombustibles, ya que la fase de los ésteres etílicos, luego de la reacción de transesterificación contienen fundamentalmente alcohol, triglicéridos sin reaccionar, glicerina, jabón y algo de agua; de ahí la importancia de realizar estas etapas en las cuales se eliminan dichas impurezas.
Los rendimientos obtenidos resultaron bajos para las condiciones de operación establecidas, lo que era de esperar puesto que la separación de fases es más complicada en la producción de ésteres etílicos que metílicos. Esto es debido al alto nivel de ácidos grasos libres presentes en la materia prima, así como la humedad, los cuales son factores altamente perjudiciales para el rendimiento en la transesterificación [7, 23].
Aunque con una temperatura de 50 °C se obtuvieron valores mayores de rendimientos, es posible obtener rendimientos superiores al 80% en la conversión, con cualquier temperatura por encima de la ambiental y menor que la temperatura de ebullición del alcohol, afectándose el factor tiempo para alcanzar dichos rendimientos [19].
A partir de procesar los datos experimentales y realizar el análisis estadístico en Statgraphics Centurion 16,2 se obtuvieron los siguientes resultados donde en la tabla 7 se muestra el análisis de varianza y en la tabla 8 los estadígrafos.
Tabla 7
Análisis de varianza para Rendimiento
| Fuente | Suma de Cuadrados | Gl | Cuadrado Medio | Razón-F | Valor-P |
| A:Temperatura | 4,805 | 1 | 4,805 | 43,44 | 0,000 0 |
| B:% Etanol | 28,520 8 | 1 | 28,520 8 | 257,85 | 0,000 0 |
| Error total | 1,659 17 | 15 | 0,110 611 | ||
| Total (corr.) | 34,985 | 17 |
| R-cuadrada = 95,26 % |
| R-cuadrada (ajustada por g.l.) = 94,63 % |
| Error estándar del est. = 0,33258 |
| Error absoluto medio = 0,26574 |
| Estadístico Durbin-Watson = 2,2996 (P=0,7540) |
| Autocorrelación residual de Lag 1 = -0,19471 |
Fig. 3 Diagrama de Pareto estandarizado para el rendimiento de la reacción.
La tabla 7 recoge el análisis de varianza con respecto al rendimiento. Con este análisis se evidencia que la temperatura y la concentración de etanol tienen un efecto estadísticamente significativo sobre el rendimiento puesto que el valor-P es menor que 0,05 con un nivel de confianza del 95,0%. Lo cual también se corrobora con el Diagrama de Pareto que se muestra en la figura 3, donde se puede apreciar que la concentración de etanol y la temperatura tienen un efecto positivo sobre el rendimiento.
En la tabla 8 se aprecia que el estadígrafo R-cuadrado refleja que el modelo obtenido describe el 99,83% de la variabilidad del rendimiento de la reacción. El estadístico de Durbin-Watson (DW) examina los residuos para determinar si hay alguna correlación significativa basada en el orden en que se presentan los datos experimentales. Como el valor-P es mayor que 0,05, no hay indicación de una autocorrelación serial en los residuos con un nivel de confianza del 95 %. Lo cual se puede evidenciar en la figura 4 que se muestra a continuación, donde se puede observar que no existe tendencia en los residuos lo cual comprueba lo anteriormente dicho.
Fig. 4 Gráfico de residuos para rendimiento.
Ver figura 5.
Fig. 5 Tendencia del comportamiento del rendimiento de la reacción con el cambio de variables estudiadas.
Es posible valorar en la figura 4 que a medida que aumenta la temperatura se evidencia un aumento del rendimiento, lo que era de esperar pues con el aumento de la temperatura se favorece la reacción directa hacia los productos lo que trae consigo el incremento del rendimiento.
Con respecto a la concentración de etanol se evidencia que a medida que aumenta la concentración de etanol, el aumento del rendimiento de la reacción volumétrico es representativo. Es sabido que difícilmente la reacción de transesterificación consigue ser completa y esto se dificulta aún más cuando se utiliza etanol, no obstante cuando se trabaja a mayores concentraciones de este alcohol, disminuye el % de agua, lo que contribuye a que no se favorezca el proceso de saponificación [10, 8], por lo que se infiere que la conversión de triglicéridos en ésteres etílicos será mayor durante la reacción, disminuyendo así la cantidad de compuestos intermedios como son monoglicéridos, diglicéridos y triglicérido, lo que se tradujo en un mayor volumen de producto y por ende en mayores rendimientos. En la tabla 9 se muestran los coeficientes del modelo ajustado.
Tabla 9
Coeficientes de regresión para Rendimiento
| Coeficiente | Estimado |
| constante | 54,21 |
| X1 | 0,069 |
| X2 | 0,308 |
La ecuación (5) es la del modelo ajustado, en donde los valores de las variables están especificadas en sus unidades originales, es decir que no se encuentran codificadas.

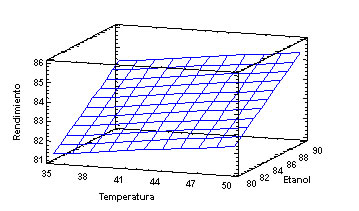
Fig. 6 Superficie de respuesta para el rendimiento.
En la figura 6 se muestra la superficie respuesta para el rendimiento con respecto a las dos variables dependientes estudiadas.
La mejor combinación de los niveles de los factores que se obtuvo a partir del análisis estadístico, con la cual se alcanzó el mayor valor de rendimiento fue a una concentración de etanol al 90% y una temperatura de 50°C.
A continuación se muestran los resultados de las mediciones de las propiedades de los ésteres etílicos que se obtuvieron a una temperatura de 50 °C, aplicando las mismas técnicas que se utilizaron para el aceite usado.
En la tabla 10 se muestran los resultados de las mediciones de la viscosidad cinemática a 40 °C para la fase de los ésteres etílicos, para los tres niveles de concentración.
Tabla 10
Viscosidad cinemática de los ésteres etílicos
| Muestra | Concentración de alcohol (%) | Viscosidad cinemática (mm2/s) |
| 1 | 90 | 25,93 (0,885) |
| 2 | 85 | 28,56 (0,036) |
| 3 | 80 | 29,58 (0,150) |
Con el análisis de las viscosidades obtenidas para cada concentración se evidenció que de forma general se obtuvieron valores elevados de esta propiedad comparados con el reportado por la norma ASTM D 445, lo que era de esperar puesto que uno de los inconvenientes de los ésteres etílicos comparados con los metílicos, lo constituye su viscosidad que resulta significativamente mayor en el caso de los primeros [5].
Otro aspecto importante es que la glicerina que se encuentra en el aceite vinculada a los ácidos grasos para formar los triglicéridos es miscible en etanol, lo que trae consigo que la misma se mantenga en la solución provocando que la reacción revierta hacia los reactivos y parte de estos triglicéridos no reaccionen para formar diglicéridos, monoglicéridos y por último la fase glicerina que se obtiene luego de las tres reacciones que ocurren en la transesterificación alcalina [11, 13], sino que van a encontrarse en la fase de ésteres etílicos de ácidos grasos, lo que trae consigo el aumento de la viscosidad en esta fase.
Además de lo antes mencionado es válido agregar que otro factor que influye en esta propiedad, es que aunque el aceite usado es sometido a un proceso de secado, no se garantiza la eliminación de toda el agua presente en el mismo, por lo que esta va a interferir en la reacción de transesterificación con elevados niveles de jabones, ácidos grasos libres y triglicéridos en el producto final, elementos que como ya se ha mencionado elevan la viscosidad del producto obtenido [7, 9].
Por otro lado se evidenció también que a medida que disminuyó la concentración del alcohol, la viscosidad presentó un incremento debido a que en la fase de ésteres etílicos fue quedando una mayor cantidad de triglicéridos, monoglicéridos y diglicéridos sin reaccionar, obteniéndose los mejores resultados para las muestras de 90% de concentración de alcohol.
A continuación en la tabla 11 se muestran las mediciones de la densidad de los ésteres etílicos.
Tabla 11
Densidad a 15 °C de los ésteres etílicos
| Muestra | Concentración de alcohol (%) | Densidad (kg/m3) |
| 1 | 90 | 882,28 (0,2939) |
| 2 | 85 | 886,18 (0,3215) |
| 3 | 80 | 892,86 (0,4513) |
Se observó que los valores de densidad de los ésteres etílicos son menores que la del aceite, esto es debido a que producto de la transesterificación las moléculas de los ésteres son más cortas [9].
Esta propiedad tanto para los ésteres etílicos como para los metílicos presenta valores similares, dentro de los límites de especificación según la norma ASTM D-1298 de 875 kg/m3a 900 kg/m3.
Analizando los valores de densidades obtenidos en la tabla 11 para cada concentración de etanol utilizada, se evidenció que con la disminución de la pureza aumentó la densidad del producto obtenido, esto ocurrió precisamente porque aumentó el contenido de ácidos grasos sin reaccionar los cuales presentan una mayor densidad que los propios ésteres.
En las tabla 12 y 13 se muestran los valores de las mediciones del índice de acidez y de la acidez para los tres niveles de concentración.
Tabla 12
Índice de acidez de los ésteres etílicos
| Muestra | Concentración de alcohol (%) | Índice de acidez |
| 1 | 90 | 2,3 (0,055 1) |
| 2 | 85 | 2,75 (0,050 0) |
| 3 | 80 | 2,98(0,045 1) |
Los valores obtenidos para el índice de acidez a pesar de que no se encontraron entre las especificaciones establecidas para los biocombustibles de 0,8 mg KOH/g de aceite, según la norma ASTM D 664 o por AOCS Oficial method Da 14-48 [15], fueron menores que los del aceite usado de partida. Esto es debido a como se ha explicado en las propiedades anteriores, luego del proceso de transesterificación quedan ácidos grasos sin reaccionar en el producto lo cual determina el comportamiento de esta propiedad.
A continuación en la tabla 13 se muestran los valores de la acidez de los ésteres etílicos obtenidos.
Tabla 13
Acidez de los ésteres etílicos
| Muestra | Concentración de alcohol (%) | Acidez (% ácido oleico) |
| 1 | 90 | 1,16 (0,055 1) |
| 2 | 85 | 1,40 (0,050 0) |
| 3 | 80 | 1,50 (0,045 1) |
Con respecto a la acidez de los ésteres etílicos, los valores obtenidos disminuyeron con respecto a la del aceite de partida luego del proceso de transesterificación, no obstante aún fueron superiores al 1%, lo que corrobora que se tiene presencia de ácidos grasos libres, por lo que sería recomendable realizar un pre tratamiento mediante la esterificación del aceite usado con el objetivo de disminuir la cantidad de ácidos grasos y así obtener un producto con menor acidez [10,19].
Las desviaciones estándar de todas las mediciones y experimentos realizados presentaron valores adecuados puesto que sus valores se encontraron entrev-2 y 2, por lo que la metodología empleada es reproducible y confiable.
ANALISIS ECONOMICO
Costo de producción a nivel de laboratorio
Para la determinación del costo de producción se partió de conocer el costo de las materias primas, materiales de producción y facilidades auxiliares, así como las cantidades a utilizar durante el proceso para transformar 1L de aceite usado.
A continuación se muestran los costos asociados para la transformación de 1L de aceite usado a nivel de laboratorio. Ver tabla 14.
Tabla 14
Costos de producción a nivel de laboratorio
| Costos directos | Costo (pesos/L) * |
| Materias primas | 0,161 |
| Materiales de producción | 0, 213 9 |
| Facilidades auxiliares | 0, 085 5 |
| Costo total | 0,46 |
*Costo para transformar 1L de aceite.
Con vistas a determinar los costos para producir 1L de ésteres etílicos fue necesario estimar la cantidad de aceite usado a transformar.
Se puede analizar que bajo las condiciones experimentales establecidas para el proceso de transesterificación y conociendo que el volumen de aceite a transformar en cada corrida fue de 50 mL, los resultados obtenidos con respecto a los volúmenes de ésteres etílicos luego de la etapa de purificación presentaron una ligera variación (ver tabla 5), por lo que se consideró determinar la media de estos valores para conocer de forma aproximada cuantos ésteres etílicos se obtienen al transformar 50 mL de aceite, arrojando un valor de 42 mL para una desviación típica de 0,8211.
Se obtuvo un costo aproximado de 0,56 pesos/L y como se puede apreciar la producción de ésteres etílicos se considera rentable, aunque es recomendable que con este valor no se especule puesto que se calculó a nivel de laboratorio, este análisis puede modificarse para una escala superior.
CONCLUSIONES
1. Con la transformación del aceite usado en biocombustible, se tiene una alternativa tentadora para eliminarlo como residual peligroso en la elaboración de alimentos.
2. Los rendimientos obtenidos, a pesar de ser bajos, demuestran que con etanol de no alta pureza se logró transesterificar el aceite usado en ésteres etílicos y glicerina.
3. Las propiedades que presentan los ésteres etílicos no cumplen con las principales especificaciones establecidas para los biocombustibles según la Norma, no obstante se logra el objetivo fundamental que persigue el proceso de transesterificación pues las propiedades del producto disminuyen con respecto a las propiedades del aceite usado de partida.
4. Con la variación de la temperatura y la concentración a los niveles fijados, se obtuvieron rendimientos con valores similares.
5. La mejor condición experimental, con la cual se alcanzó el mayor valor de rendimiento fue a una concentración de etanol al 90% y una temperatura de 50°C.
6. Se debe seguir investigando este procedimiento para optimizarlo con vistas a mejorar el rendimiento.
BIBLIOGRAFIA
1. GHIDURUS, Mihaela, TURTOI, Mira, BOSKOU, George, NICULITA, Petru, STAN, Visilica. "Nutritional and health aspects related to frying", Romanian Biotechnological Letters, 2010, vol 15, núm. 6, pp. 123-128. Romania.
2. HURTADO SUATERNA, Adriana Cecilia. "La fritura de los alimentos: el aceite de fritura". Perspectivas en nutrición humana, 2009, vol 11, núm. 1, pp. 39-53. Colombia.
3. SALAS VÁZQUEZ, R., "Peligros a controlar en la fritura de alimentos". Colombia.
4. ABREU, L., ALVAREZ, M., RUIZ, S., CARDENAS, M. "Obtención de biodiesel a partir de aceites vegetales usados". ION, 2006, vol 19, núm. 1, pp. 39-42. Colombia.
5. ABULARACH ASBUN, Elias, AMURRIO DERPIC, David. "Obtención de biodiesel a partir de aceite desechado de frituras". Acta Nova, 2010, vol 4, núm. 4, pp. 514-533. Bolivia.
6. BENJUMEA H., Pedro, AGUDELOS S.,John , JAIME CANO,Gabriel. "Estudio experimental de las variables que afectan la reaccion de transesterificacion del aceite crudo de palma para la produccion de biodiesel". Scientia Et Technica, 2004, vol X, núm. 24, pp. 169-174. Colombia.
7. CHHETRI, Arjun B., WATTS CHRIS, K., RAFIQUL ISLAM, M. "Waste Cooking Oil as an Alternate Feedstock for Biodiesel Production". Energies, 2008, núm. 1, p. 3-18. Canadá .
8. ANASTOPOULOS, George, ZANNIKOU, Ypatia, STOURNAS, Stamoulis, KALLIGEROS, Stamatis. "Transesterification of Vegetable Oils with Ethanol and Characterization of the Key Fuel Properties of Ethyl Esters". Energies, 2009, núm. 2, pp. 362-376. Greece.
9. MARTÍNEZ MACHUCA, Fiderman, MELLIZO CERÓN, Jhon Eric, ROJAS HOYOS, Jaime Andrés. "Optimización de condiciones de operación en la transesterificación de aceites de higuerilla y palma con etanol e hidróxido de sodio". Bistua, 2010, vol 8, núm. 1, pp. 315-335. Colombia.
10. ROJAS GONZÁLEZ, Andrés Felipe, GALLEGO GIRÓN, Erika, TORRES CASTAÑEDA, Harlen Gerardo. "Variables de operación en el proceso de transesterificaión de aceites vegetales: una revisión-catálisis química". Ingeniería e Investigación, 2009, vol 29, núm. 3, pp. 17-22. Colombia.
11. GARCÍA CAMÚS, J.M., GARCÍA LABORDA, J.A., "Informe de vigilancia tecnológica. Biocarburantes líquidos: biodiésel y bioetanol". España. pp. 5-119.
12. GARCÍA DÍAZ, Marulin. "Estudio del aprovechamiento del aceite comestible usado". 2013, La Habana, Cuba.
13. VICENTE, Gemma, MARTÍNEZ, Mercedes, ARACIL José. "Integrated biodiesel production: a comparison of different homogeneous catalysts systems". Bioresource Technology, 2003, vol 92, pp. 297-305. Madrid, España.
14. LEUNG D.Y.C., Y.G. "Transesterification of neat and used frying oil: Optimization for biodiesel production". 2006, China.
15. TOROSSI BAUDINO, Favio Daniel. "Reacciones en contexto: la transesterificación en la producción de biodiesel a partir de aceites de fritura usados". An. Quím., 2006, vol 103, núm. 3, pp. 43-49. Argentina.
16. GARCÍA DÍAZ, M., MAQUEIRA TAMAYO,Y. "Estudio de la obtención de biodiesel a partir de aceite comestible usado". Tecnología Química, 2013, vol 33, núm. 2, pp. 134-138. Colombia.
17. PLATA CHAVEZ V., et-al, "Estudio de la transesterificación del aceite de palma con etanol en un sistema de reactores de flujo continuo para la producción de biodiesel". 2008. Colombia.
18. MONDINO, D.P. "Preparación de soluciones". 2012. México.
19. CIFUENTES GUERRERO, Manuel Francisco. "Obtención de biodiesel a partir de aceite usado de cocina por transesterificación en dos estapas, con dos tipos de alcoholes". 2010. Colombia.
20. AZIAN MORAD, Noor, MUSTAFA KAMAL, A.A, YEW, T.W. "Liquid Specific Heat Capacity Estimation for Fatty Acids,Triacylglycerols, and Vegetable Oils .Based on Their Fatty Acid Composition". JAOCS, 2000, vol 77, núm. 9, pp. 1001-1005. Malaysia.
21. AVILA GÓMEZ, Adrian E., "Desarrollo de la cinética química de la reacción de transesterificación de la oleina de palma". 2006.Colombia.
22. RESTREPO HERRERA, Juan Alberto."Caracterizacion y aprovechamiento del aceite residual de frituras para la obtencion de un combustible". 2008. Colombia.
23. HAMELINCK, Carlo, SCHOBER, Sigurd. "Fatty acid ethyl esters. Final report for Lot 3a of the Bioscopes project". 2007.
Recibido: Mayo 2016
Aprobado: Septiembre 2016
Ing. Anabel Sarracent-López. Facultad de Ingeniería Química, ISPJAE, La Habana, Cuba