My SciELO
Services on Demand
Article
Indicators
-
 Cited by SciELO
Cited by SciELO
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Revista de Salud Animal
Print version ISSN 0253-570X
Rev Salud Anim. vol.31 no.3 La Habana Sept.-Dec. 2009
Comunicación corta
EVALUACIÓN DE LA CARTA DE COLORES FAMACHA© EN LA DETECCIÓN DE ANEMIA EN CABRAS EN SILVOPASTOREO. ESTUDIOS PRELIMINARES
EVALUATION OF FAMACHA© COLOR CHART IN THE DETECTION OF ANEMIA IN GOATS UNDER SILVOPASTORAL SYSTEM CONDITIONS. PRELIMINARY STUDIES
Noelvys Aróstica*, J. Arece*, Y. López*, J.G. Rodríguez Diego**
*Estación Experimental de Pastos y Forrajes "Indio Hatuey" Central España Republicana. CP 44280. Matanzas. Cuba. Correo electrónico: noelvys.arostica@indio.atenas.inf.cu. Teléf: 377482. FAX: 377307; **Centro Nacional de Sanidad Agropecuaria (CENSA), Apartado 10, San José de las Lajas, La Habana, Cuba
RESUMEN
Con el objetivo de evaluar la factibilidad del empleo de la carta de colores FAMACHA© en la detección de anemia en cabras mestizas, se muestrearon 70 animales mantenidos en un área de pastoreo (Dichrostachys cinerea- Acacia farnesiana - complejo Dichantium spp., Brotriochloa spp) alrededor de 9 horas diarias. Por dos meses se determinó el color de la mucosa ocular (CMO) según la escala de la carta de colores FAMACHA© y se extrajeron muestras de sangre y heces a cada animal. Se determinó volumen celular aglomerado (VCA), el conteo fecal de huevos (CFH) de estrongílidos y las especies presentes por coprocultivos. El coeficiente de correlación (Spearman) entre el VCA y los valores del color de la mucosa fue de -0,58 para un nivel de significación p<0,01. Para los valores 4 y 5 de la carta FAMACHA© y hematocrito = 19% como indicador de anemia, se obtuvo una sensibilidad y una especificidad de 91% y 62,4% respectivamente. El valor de predicción de un caso negativo fue de un 91,3% mientras que el valor de predicción de un caso positivo fue de 45,7%. Por otro lado los animales con categoría 4 y 5 fueron los que mayor conteo fecal de huevos presentaron aunque no mostraron diferencias significativas. Los resultados indican que la metodología FAMACHA© puede ser una herramienta en la detección de anemia en cabras en nuestras condiciones.
Palabras clave: FAMACHA©; cabras; anemia; haemonchosis; silvopastoreo
ABSTRACT
With the objective to evaluate the feasibility of the use of FAMACHA© color card in the detection of anemia, 70 goats were used. These animals were grazed in a silvopastoral system around 9 hours daily (Dichrostachys cinerea- complex Dichantium spp., Brotriochloa spp.). During 2 month, the colour of the ocular mucosa was determined (CMO) according to the scale of FAMACHA© color card. Besides, faecal and blood samples were extracted from each animals to determine the faecal strongyle egg count, genera by coprocultures and packed cell volume (PCV) through centrifugation. The correlation coefficient (Spearman) between the VCA and the values FAMACHA© card was -0, 58. Sensitivity and specificity for 4 and 5 FAMACHA© card values and PCV =19% as indicator of anemia were 91% and 62.4%, respectively. The predictive value of a negative case was of 91.3%, whereas the predictive value of a positive case value was 45, 7%. On the other hand, the animals with category 4 and 5 showed the highest faecal egg count, but no differences among groups were detected. The results indicate that the FAMACHA methodology© can be a useful tool in the detection of anemia in goats under our condition.
Key words: FAMACHA©; goats; anemia; haemonchosis; silvopastoral system
La resistencia antihelmíntica (RA) de los nematodos gastrointestinales en los últimos años se ha ido incrementando notablemente en los pequeños rumiantes (1), especialmente en los trópicos húmedos, lugar donde los estadios de vida libre de nemátodos como Haemonchus contortus y Trichostrongylus colubriformis encuentran las condiciones para su desarrollo durante todo el año (2).
Por su carácter hematófago Haemonchus spp. constituye uno de los principales enemigos de las producciones de pequeños rumiantes, en especial de las cabras, señalándose una disminución de la producción de hasta un 50% (1).
Sobre la base del concepto de Control Integrado de Parásitos se ha enfrentado la situación de la (RA) de estos nematodos, que incluye varios componentes entre los que se encuentran: el manejo del pastoreo (pastoreo mixto, rotación de potreros, descanso de potreros), control biológico, selección de animales resistentes (3), utilización de vacunas y plantas medicinales y la desparasitación selectiva de los animales en función de la coloración de la mucosa ocular (FAMACHA©) (2, 4).
La metodología FAMACHA© fue creada en Sudáfrica y se basa en el tratamiento selectivo de los animales en función de la coloración de la mucosa de la conjuntiva ocular para el control del Haemonchus spp (4). Inicialmente fue evaluada en ovinos aunque puede ser aplicada a todos los rebaños donde la haemonchosis constituya uno de los principales problemas, lo que permite extrapolarla a diferentes condiciones; en cabras ha sido evaluada con excelentes resultados (1).
Se ha implementado con éxito en varios países localizados en las regiones tropicales y subtropicales del orbe, cabe destacar a nivel latinoamericano la incursión que han realizado en este método países como Brasil, Argentina Uruguay y México (5).
En estudios previos en Cuba se demostró la aplicabilidad de la metodología en la detección de anemia por haemonchosis en ovinos (6), sin embargo, se desconoce su aplicación en la especie caprina, por lo que el objetivo del presente trabajo fue evaluar la factibilidad de detectar cabras anémicas con el uso de la metodología FAMACHA© en un sistema silvopastoril.
El experimento se realizó en un rebaño caprino de un productor privado del municipio Martí en la provincia de Matanzas, durante los meses de enero y febrero (período poco lluvioso) del 2008. Para ello se muestrearon 70 cabras mestizas mantenidas en un sistema de vegetación arbustiva espontánea de D. cinerea- Acacia fernisiana (90% del área) y complejo pitilla-jiribilla (Dichantium spp.-Brotriochloa spp.) como pasto base, en un área de 58,3ha.
Con frecuencia mensual se determinó el color de la mucosa ocular (CMO) de los animales y se clasificó según las categorías de la carta de colores FAMACHA© en la cual el valor mínimo (A) se corresponde con la mucosa ocular de rojo intenso y el máximo (E) con un color pálido. Se extrajo sangre por punción de la vena yugular de los animales para la determinación del hematocrito o volumen celular aglomerado (VCA) (7); además se extrajeron heces directamente del recto de cada animal a las que se les realizó el conteo fecal de huevos (CFH) de estrongílidos gastrointestinales mediante la técnica de McMaster modificada (8). Luego se realizaron coprocultivos por pool de heces y se identificaron las larvas según sus características morfológicas (9). Se realizó un análisis de correlación (Spearman) entre el CMO y el VCA y el CFH. Además se determinó la sensibilidad y especificidad de la carta en la detección de animales anémicos así como el valor predictivo de un animal anémico y de un animal sano; para la clasificación de animales anémicos se consideró todo aquel con VCA = 19% (10). Se realizó un análisis de varianza de clasificación simple entre el VCA y el CFH. Por la variabilidad de los datos del CFH y para lograr una aproximación a la distribución normal se transformaron a través de su logaritmo (log CFH +1). Se empleó el paquete estadístico SPSS: versión 15 para Windows.
En el grupo de cabras muestreadas se pudo constatar el predominio de Haemonchus spp como estrongílido de mayor importancia coincidiendo con los resultados de Pérez y Rodríguez-Diego (11); La O et al.; Aguirre y otros (12, 13) y representó el 86, 6% del total de larvas encontradas. Además se encontró Trichostrongylus spp (6,6%) y Strongyloides spp. (6,6%).
En la Figura 1 (A) se muestran los valores del volumen celular aglomerado en función de la clasificación de la carta de colores y se aprecia que en la medida que aumentan los valores de la carta de colores, lo cual se corresponde con mucosas más pálidas, disminuye el VCA. Existen además imbricaciones de los valores del VCA en cada categoría. Esta relación ofrece un coeficiente de correlación inverso de -0,58 (p<0,01), superior al reportado por Kaplan et al. (1) de 0,30 en cabras en los Estados Unidos de América (EUA). En la Figura 1 (B) se ve reflejado en los animales como a medida que aumentan los valores de la carta de colores, va siendo menor su condición corporal.

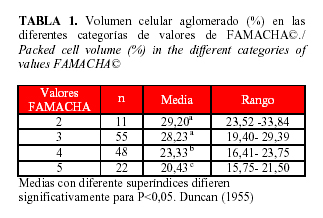
En la Tabla 1 se aprecian los valores de cada categoría FAMACHA© así como sus rangos. Se pudo constatar que entre las categorías 2 y 3 no existieron diferencias significativas (p<0,05), sin embargo, si se contrastan con los valores 4 y 5 de la carta. Estos resultados coinciden con los obtenidos por Arece (6) en ovinos en la provincia de Matanzas.
Como podemos apreciar en la Tabla 2 la sensibilidad y especificidad de la prueba a partir de que se consideró anémico todo el animal con VCA =19% fue de un 91% y 62,4% respectivamente. Los resultados de sensibilidad son superiores a los encontrados por varios autores (1, 2, 6, 14, 15), quienes reportaron valores de 57,6; 75; 79- 85%; 30,1 y 19,1% respectivamente aunque los obtenidos por Arece (6) fue en la especie ovina; en el caso de la especificidad solo fue superior a la demostrada por Vatta et al. (14). La sensibilidad posee mayor importancia que la especificidad pues tratar animales falsos positivos implicaría gastos innecesarios, sin embargo, dejar de tratar animales afectados podría causar la muerte. El valor predictivo de animales positivos (45,7%) es similar a los obtenidos por Burke et al. (15), mayor que los obtenidos por Kaplan et al. (1) y menor que los propuestos por Mahieu (2) y Arece (6), este último en ovinos en la provincia de Matanzas. En el caso del valor predictivo negativo (91,3%), varios autores plantean resultados similares (1, 15); Arece (6) y Kaplan et al. (1) publicaron resultados superiores a los obtenidos en el trabajo y Burke (15) y Mahieu (2) obtuvieron resultados inferiores.
Según la clasificación propuesta por Hansen y Perry (16), las medias de los conteos de huevos en cada uno de los grupos FAMACHA© fue moderada (200-800 hpg) y no mostró diferencias significativas (P<0,05). Estos resultados nos permiten trazarnos algunas hipótesis que dan respuesta a dicho comportamiento: 1) los bajos conteos fecales de huevos estuvieron influenciados por la suplementación a base concentrados a que fueron sometidos los animales durante el muestreo (920g/animal/día); Chartier et al. (17) y Hoste et al. (18) demostraron la influencia del plano nutricional en el comportamiento de los nemátodos gastrointestinales en cabras; 2) Los arbustos predominantes (D. cinerea-Acacia spp.) en el sistema modifican la dinámica de los nemátodos gastrointestinales con la presencia de polifenoles (taninos condensados) en sus estructuras y favorecen el ramoneo de los animales, lo que disminuye la posibilidad de infestación mediante el consumo directo de larvas en el pasto; 3) La baja carga de animales disminuye la intensidad de pastoreo y la probabilidad de consumo de larvas en pasto en estadios infestivos.
Los resultados indican que es posible utilizar la carta de colores FAMACHA© en la detección de anemia en cabras en un sistema de silvopastoreo de vegetación espontánea de D. cinerea- Acacia spp.
REFERENCIAS
1. Kaplan RJ, Burke M, Terrill TH, Miller JE, Getz WR, Mobini S et al. Validation of the FAMACHA© eye colour chart for detecting clinical anaemia in sheep and goats on farms in the southern United States. Vet Parasitol. 2004;123(1-2):105-120.
2. Mahieu M, Arquet R, Kandassamy T, Mandonnet N, Hoste H. Evaluation of targeted drenching using Famacha© method in Creole goat: Reduction of anthelmintic use, and effects on kid production and pasture contamination. Vet. Parasitol. 2007; 146(1-2):135-147.
3. Camps D, Martínez RD, Torres G, Romero E, Becerril CM., García J. Differences in gastrointestinal parasites between two goats genotypes in the dry tropic of Mexico. Memorial First North American Parasitology Congress 2007; Mérida. México.
4. Van Wyk J, Vatta A. Sustainable approaches for managing Haemonchosis in sheep and goats, final report of FAO. Technical cooperation project Nº TCP/SAF/882 (A) 2001; (en línea) Consultado 3 jul. 2007. Disponible en: http://cnia.inta.gov.ar/helminto/pdf%20alternativos/Sustastainable %20approaches%20for%20managing%20 haemonchosis%20in%20sheep%20and %20goats.pdf
5. Miller J, Waller P. Novel approaches to control of parasites - a Workshop. Veterinary Parasitology. Amsterdam, Holanda. 2004;125:59-68.
6. Arece J. La metodología FAMACHA©: una estrategia para el control de estrongilidos gastrointestinales de ovinos. Estudios preliminares. Rev Salud Anim. 2007;29(2):91-94.
7. Schalm OW, Jain NO, Carrol EJ. Veterinary Haematology, 3rd Edition, Lea and Febiger, Philadelphia 1975, pp. 144-56.
8. Arece J, Rojas F, González E, Cáceres O. Eficacia de LABIOMEC® en el parasitismo en ovinos, terneros y equinos en condiciones de producción. Pastos y Forrajes. 2002;25(3):223-229.
9. Valle María T. Contribución al estudio de los nematodos gastrointestinales del ganado bovino. Tesis para optar por el grado de Doctor en Ciencias Biológicas. Ciudad de La Habana. Cuba. 1978; 150 p.
10.Mahieu M, Arquet R, Kandassamy T. Mandonet N. Haemonchosis control in creole goats by using FAMACHA method. Memorias del Cuarto Seminario Internacional sobre métodos alternativos para el control de parásitos helmintos en la ganadería "Manejo o control de parásitos: nuevos paradigmas en el control integrado". Universidad Autónoma de Yucatán. Mérida, Yucatán, México 2005.
11.Pérez E, Rodríguez Diego JG. Extensión de invasión de nematodos gastrointestinales en un centro de la provincia de la Habana. Rev Salud Anim. 2005;27(5):62-65.
12.La O M, Fonseca N, Costa P, Carrión M, Vázquez J, Liranza E, et al. Infestación por nematodos gastrointestinales en un sistema de explotación caprina silvopastoril en condiciones de montaña. Pastos y Forrajes. 2003;26(1):53-59.
13.Aguirre DH, Cafrune MM, Viñabal AE, Salatin AO. Aspectos epidemiológicos y terapéuticos de la nematodiasis gastrointestinal caprina en un área subtropical de la Argentina. INTA, Argentina. 2001. (en línea) Consultado 3 Diciembre. 2007. Disponible en: http://cnia.inta.gov.ar/helminto/generales/Trabajos%20miembros.htm
14.Vatta AF, Letty BA, Van der Linde MJ, Van Wijk EF, Hansen JW, Krecek RC. Testing for clinical anaemia caused by Haemonchus spp. in goats farmed under resource-poor conditions in South Africa using an eye colour chart developed for sheep. Vet Parasitol. 2001;99(1-2):1-14.
15.Burke JM, Kaplan RM, Miller JE, Terrill TH, Getz WR, Mobini S, et al. Accuracy of the FAMACHA system for on-farm use by sheep and goat producers in the southeastern United States. Vet Parasitol. 2007;147(1-2):89-95.
16.Hansen J, Perry B. The epidemiology, diagnosis and control of helminth parasites of ruminants. ILRAD, Nairobi, Kenya. 1994; 171 pp.
17.Chartier C, Etter E, Hoste H, Pors I, Mallereau MP, Broqua C, et al . Effects of the initial level of milk production and of the dietary protein intake on the course of natural nematode infection in dairy goats. Vet Parasitol. 2000;92(1):1-13.
18.Hoste H, Torres-Acosta JF, Paolini V, Aguilar-Caballero A, Etter E, Lefrileux Y, et al. Interactions between nutrition and gastrointestinal infections with parasitic nematodes in goats. Small Ruminant Research. 2005;60(1-2):141-51.
(Recibido 10-4-2009; Aceptado 20-7-2009)














